ФАРМАКОПЕЙНАЯ СТАТЬЯ Капиллярный электрофорез
Капиллярный электрофорез – это физический метод анализа, основанный на миграции внутри капилляра заряженных частиц в растворе электролита под влиянием приложенного электрического поля.
Скорость миграции частиц определяется их электрофоретической подвижностью и электроосмотической подвижностью буферного раствора.
Электрофоретическая подвижность вещества (μэф) зависит от его характеристик (электрического заряда, размеров и формы) и от характеристик буферной среды, в которой происходит разделение (типа и ионной силы электролита, рН, вязкости и добавок):
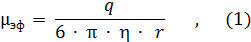
где q – эффективный заряд частицы;
η– вязкость раствора электролита;
r – стоксовский радиус частицы.
Электрофоретическую скорость ( 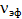 ) для вещества сферической формы определяют по формуле:
) для вещества сферической формы определяют по формуле:
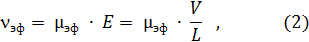
где E – сила электрического поля;
V – приложенное напряжение;
L – общая длина капилляра.
Когда к капилляру, заполненному буферным раствором, приложено электрическое поле, внутри капилляра образуется поток растворителя, называемый электроосмотическим потоком. Скорость и направление электроосмотического потока зависят от электроосмотической подвижности (μэо), определяемой знаком и плотностью заряда на внутренней стенке капилляра, а также характеристиками буфера:

где ε – диэлектрическая константа буфера;
ζ– дзета-потенциал поверхности капилляра.
Электроосмотическую скорость (  ) рассчитывают по формуле:
) рассчитывают по формуле:

Электрофоретическая и электроосмотическая подвижность ионов могут быть направлены в одну и ту же или в противоположные стороны в зависимости от заряда частиц; таким образом, скорость движения растворенного вещества будет определяться уравнением:

Если электроосмотическая скорость выше электрофоретической, можно одновременно разделить как положительно, так и отрицательно заряженные ионы. Время, затраченное ионом для миграции от конца, в котором вводится образец, до места детекции (l – эффективная длина капилляра), определяют по формуле:
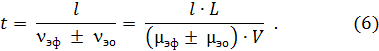
Как правило, капилляры из плавленого кварца без покрытия при pH выше 3 несут на внутренней поверхности отрицательный заряд из-за диссоциации силанольных групп. При этом электроосмотический поток направлен от анода к катоду.
В некоторых случаях необходимо уменьшить или изменить направление электроосмотического потока. Для этого различным образом модифицируют внутреннюю стенку капилляра или изменяют рН буферного раствора.
После введения образца в капилляр каждый анализируемый ион движется внутри фонового электролита в виде отдельной зоны в соответствии со своей электрофоретической подвижностью. Степень размывания каждой зоны растворенного соединения определяется совокупностью различных причин. В идеальном случае единственной причиной размывания зон является продольная молекулярная диффузия растворенного вещества вдоль капилляра. В этом, идеальном, случае эффективность разделения полосы, характеризуемая числом теоретических тарелок (N), выражается формулой:
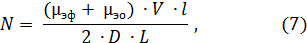
где D – молекулярный коэффициент диффузии растворенного вещества в буферном растворе.
На практике на размывание полос значительное влияние оказывают тепловое рассеяние, адсорбция образца на стенке капилляра, различная проводимость между образцом и буфером, длительность ввода пробы, размеры детектирующей ячейки и различия уровней жидкости в емкостях с буферными растворами.
Разделение между двумя полосами, называемое разрешением (Rs), определяют по формуле (8):

где μэфб и μэфа – электрофоретические подвижности каждого из двух разделенных ионов;
 – их средняя электрофоретическая подвижность.
– их средняя электрофоретическая подвижность.
Среднюю электрофоретическую подвижность определяют по формуле:
Оборудование
Система для капиллярного электрофореза состоит из высоковольтного источника напряжения; двух флаконов с буферными растворами и погруженными в них электродами; капилляра, заполненного соответствующим раствором и погруженного обоими концами во флаконы с буферными растворами; системы ввода образца; детектора, способного в режиме реального времени регистрировать вещества, проходящие мимо оптического окна капилляра; системы термостатирования; регистрирующего прибора или подключенного компьютера.
Для введения пробы могут использоваться три способа: гидростатический – за счет разного уровня буферных растворов, гидродинамический – с помощью прилагаемого давления или вакуума и электрокинетический – благодаря прилагаемому напряжению. В последнем случае степень ввода в капилляр каждого компонента пробы зависит от соответствующей электрофоретической подвижности. Электрокинетическая система ввода для многокомпонентной смеси с разной электрофоретической подвижностью ведет к изменению соотношения концентраций ее составляющих и в данном случае может адекватно применяться лишь для качественного анализа. При условии определения в многокомпонентной смеси одного или двух соединений этот метод может использоваться и для количественного анализа. Кроме того, такой способ введения может позволить увеличить чувствительность анализа.
Детектирование осуществляется с помощью абсорбционной спектрофотометрии в ультрафиолетовой и видимой областях, флуориметрии, кондуктометрии, амперометрии или масс-спектрометрии.
Для обнаружения не поглощающих в ультрафиолетовой области и не флуоресцирующих соединений используется непрямое детектирование. В этом случае в ведущий электролит вводится вещество, поглощающее ультрафиолетовое излучение и образующее выраженное фоновое поглощение. При этом зона определяемого вещества визуализируется в виде обратного пика. С использованием специального программного обеспечения электрофореграмме придают стандартный вид.
Применяемый раствор электролита фильтруют для того, чтобы удалить крупные частицы (размером более 0,45 мкм), и дегазируют для предотвращения образования пузырьков воздуха, которые могут быть помехой для детектирующей системы или могут нарушить электропроводность в капилляре во время проведения анализа. Для хорошей воспроизводимости времени миграции анализируемых компонентов проб для каждого определения должна быть разработана определенная процедура промывки капилляра.
Основными формами проведения капиллярного электрофореза являются: капиллярный зонный электрофорез, мицеллярная электрокинетическая хроматография, капиллярный гель-электрофорез, капиллярное изоэлектрическое фокусирование и капиллярный изотахофорез.
Дата добавления: 2016-01-30; просмотров: 4178;
