Сущность масс-спектрометрии
Масс-спектрометрия- это метод измерения отношения массы заряженных частиц к их заряду (m/z).
Для проведения масс-спектрометрического анализа образец переводят в ионизированную форму. После этого тем или иным способом производится разделение ионов по отношению их массы к зарядам и регистрация этих ионов, которые могут быть как положительными, так и отрицательными.
Масс-спектрометрический анализ дает важную информацию для определения молекулярной массы, молекулярной формулы или элементного состава и структуры молекул.
Масс-спектрометрию используют для определения относительной молекулярной массы Мг соединения, которую выражают в атомных единицах массы (а.е.м.) или дальтонах, Да, (1 Да = 1 а.е.м.=1,660541-10-27 кг, что равно 1/12 массы изотопа углерода с массовым числом 12). Масса основного изотопа углерода 12С выражается целым числом и равна 12,000000 Да. Массы всех изотопов любых других элементов будут выражаться нецелыми числами.
В масс-спектре пики или линии с определенным отношением m/z, соответствуют молекулярным фрагментам и также обозначаются целым числом, полученным при округлении точного значения m/z.
В масс-спектрометрии существует три различных понятия массы. Средняя молекулярная масса вычисляется на основании элементного состава и средних атомных масс. Средняя молекулярная масса важна при изучении больших молекул. Номинальная молекулярная масса вычисляется с учетом элементного состава и номинальных атомных масс наиболее распространенных в природе изотопов. Точная молекулярная масса вычисляется из значений точных масс наиболее распространенных изотопов.
С помощью масс-спектрометрии возможны: анализ органических соединений, неорганический анализ, исследования по выяснению механизмов реакций в органической химии и анализ поверхности.
С помощью масс-спектрометрии как аналитического метода решают громадное число качественных и количественных задач. Качественные исследования заключаются в определении структуры неизвестного соединения, в частности, природных веществ, метаболитов лекарственных препаратов и других ксенобиотиков, синтетических соединений. Для количественного анализа масс-спектрометрию используют при разработке арбитражных методов и методов сравнения. Масс-спектрометрия сегодня развивается очень быстро, охватывая все более широкие области применения. Объединение масс-спектрометрии с хроматографией значительно увеличило возможности метода и расширило круг изучаемых объектов.
5.12. Электрогравиметрия
В электрогравиметрическом анализе определяемое вещество количественно выделяют из раствора электролизом и по массе выделившегося металла или его оксида на электроде рассчитывают содержание определяемого элемента в пробе.
Электролизом называют химическое разложение вещества под действием электрического тока. На катоде происходит восстановление:
Cu2+ + 2e → Cu0
а на аноде – окисление:
2Cl- - 2e → Cl2 (г) и 2OH- - 2e → 1\2O2 + H2O
Под действием приложенного напряжения заряженные частицы (ионы) перемещаются к электродам. Однако их разряд, т. е. электролиз, начинается при достижении определенной величины напряжения, называемой напряжением разложения
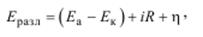 (5.2)
(5.2)
где Eа , Eк – ЭДС гальванического элемента;
iR – омическое падение напряжения;
η – перенапряжение анода и катода при выделении продуктов электролиза.
Схема установки для проведения электролиза приведена на рис. 5.14.
Электролиз чаще всего проводят при постоянном токе. Для получения постоянного тока обычно используют выпрямитель переменного тока или батарею аккумуляторов 1. Скользящий контакт 2 позволяет регулировать подаваемое напряжение, которое измеряют вольтметром V. Сила тока контролируется амперметром А. При выделении металлов катод 5 обычно используют в виде платиновой сетки, анод 4 – в виде платиновой спирали или пластинки. При выделении оксидов знаки электродов меняются: платиновая сетка становится анодом, а спираль – катодом. Раствор перемешивается механической или магнитной мешалкой 3.
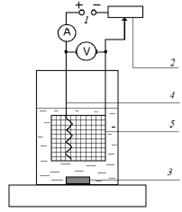
Рис. 5.14. Схема установки для проведения электролиза: 1 – источник постоянного тока; 2 – переменное сопротивление (реостат); 3 – магнитная мешалка;
4 – анод; 5 – катод
В электрогравиметрических методах анализа кроме потенциала, силы тока важно контролировать ряд экспериментальных условий.
5.13. Кулонометрия
В кулонометрических методах определяют количество электричества, которое расходуется в ходе электрохимической реакции. Различают прямую кулонометрию и кулонометрическое титрование.
В методах прямой кулонометрии анализируемое вещество непосредственно подвергается электрохимическому превращению в кулонометрической ячейке (процесс проводят при постоянном контролируемом потенциале) (Рис. 5.15.).
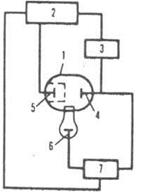
Рис. 5.15. Схема установки для прямой кулономeтрии при постоянном E:
1 - электролизер; 2 - источник постоянного токa с регулируемым напряжением: 3 - прибор для определения количества злектричества: 4 - рабочий электрод; 5 - вспомогательный электрод; 6 - электрод сравнения, относительно которого контролируют потенциал рабочего электрода: 7 - устройство, измеряющее разность потенциалов.
В методе кулонометрического титрования определяемое вещество реагирует с титрантом, который производится в кулонометрической ячейке посредством электролиза специально подобранного раствора.
Кулонометрическое титрование проводят при постоянном токе.
Кулонометрические методы основаны на законах Фарадея. Необходимым условием количественного определения является 100%-й выход по току. Выход по току определяется отношением количества вещества, выделившегося в процессе электролиза, к теоретическому количеству, вычисленному на основании закона Фарадея. Не 100%-й выход по току может быть обусловлен затратами тока на побочные процессы:
1) разложение воды на водород и кислород;
2) восстановление или окисление примесей, например, растворенного в воде кислорода;
3) реакция с участием продуктов электролиза;
4) реакция с участием материала электрода (окисление ртути и др).
При проведении кулонометрических определений нужно предусмотреть все условия, обеспечивающие 100%-й выход по току, контроль рН, выбор электродов, разделение катодного и анодного пространства.
5.14. Кондуктометрия
Кондуктометрический метод анализа основан на измерении удельной электропроводности анализируемого раствора.
Электропроводностью называют величину, обратную электрическому сопротивлению R. Единицей измерения электропроводности является сименс (См) или Ом-1. Растворы электролитов, являясь проводниками II рода, подчиняются закону Ома. По аналогии с сопротивлением проводников I рода сопротивление раствора прямо пропорционально расстоянию между электродами d и обратно пропорционально площади их поверхности A:
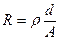 (5.3)
(5.3)
где р - удельное сопротивление , Ом · см.
При d =1 смиА =1 см2имеем R = р, следовательно, удельное сопротивление равно сопротивлению 1 см3 раствора.
Величину, обратную удельному сопротивлению, называют удельной электропроводностью:
æ = 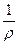 (5.4)
(5.4)
Удельная электропроводность (См ∙ см-1) численно равна току (А), проходящему через слой раствора с поперечным сечением, равным единице, под действием градиента потенциала 1 В на единицу длины.
Электропроводность разбавленных растворов электролитов зависит от числа ионов в растворе (т. е. от концентрации), числа элементарных зарядов, переносимых каждым ионом (т. е. от заряда иона), и от скорости движения одинаково заряженных ионов к катоду или аноду под действием электрического поля (Рис. 5.16.). С учетом всех этих факторов электропроводящие свойства ионов характеризуют эквивалентной ионной электропроводностью (подвижностью).
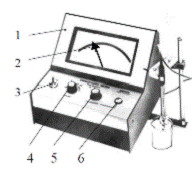
Рис. 5.16. Кондуктометр ОК 102/1: 1 – корпус прибора; 2 – измерительная
шкала; 3 – тумблер «Сеть»; 4 - переключатель пределов измерения «Range»; 5 – ручка калибровки потенциометра «Calibration»; 6 – кнопка калибровки «Calibration».
Различают прямую и косвенную кондуктометрию, или кондуктометр ическое титрование.
Прямая кондуктометриямало применяется в аналитической химии. Причина этого в том, что электропроводность является величиной аддитивной и определяется присутствием всех ионов в растворе. Прямые кондуктометрические измерения используют для контроля качества воды, применяемой в химической лаборатории, и современные установки для перегонки или деминерализации воды снабжаются кондуктометрическими датчиками - кондуктометрами для измерения удельной электропроводности растворов. Детекторы по электропроводности применяются в ионной хроматографии.
К достоинствам метода кондуктометрического титрования относится возможность высокоточных измерений даже в очень разбавленных растворах.
Для кондуктометрического титрованияпригодны кислотно-основные или осадительные реакции, сопровождающиеся заметным изменением электропроводности вследствие образования малодиссоциирующих или малорастворимых соединений.
5.15. Титриметрия
Титриметрический анализ (титрование) — метод количественного/массового анализа, который часто используется в аналитической химии, основанный на измерении объёма раствора реактива точно известной концентрации, расходуемого для реакции с определяемым веществом (Рис. 5.17.).

Рис. 5.17. Настольный электрохимический прибор
OHAUS Starter 2100
Титрование — процесс определения титра исследуемого вещества. Титрование производят с помощью бюретки, заполненной титрантом до нулевой отметки. Титровать начиная от других отметок не рекомендуется, так как шкала бюретки может быть неравномерной. Заполнение бюреток рабочим раствором производят через воронку или с помощью специальных приспособлений, если бюретка полуавтоматическая. Конечную точку титрования (не следует путать с точкой эквивалентности) определяют индикаторами или физико-химическими методами (по электропроводности, светопропусканию, потенциалу индикаторного электрода и т. д.). По количеству пошедшего на титрование рабочего раствора рассчитывают результаты анализа.
Методы титрования
Процесс титрования сопровождается изменением равновесных концентраций реагента, определяемого вещества и продуктов реакции. Это удобно изобразить графически в виде т. наз. кривой титрования в координатах концентрация определяемого.вещества (или пропорциональная ей величина)-объем (масса) титранта.
(1) Косвенное титрование, или титрование заместителя – титрование, которое применяют, когда нет подходящей реакции или индикатора для прямого титрования. В этом случае используют реакцию, в которой анализируемое вещество замещают эквивалентным количеством другого вещества и затем титруют рабочим раствором.
(2) Метод объемного (титрометрического) анализа - это метод количественного определения, основанный на измерении объема реагента, требуемого для проведения реакции с определяемым веществом.
(3) Обратное титрование – титрование, которое используют в тех случаях, когда прямое титрование невозможно или когда анализируемое вещество неустойчиво. При этом берут два рабочих раствора, один из которых добавляют в избытке, а вторым титруют избыток первого.
(4) Прямое титрование наиболее распространенный и удобный прием, когда к анализируемому раствору вещества непосредственно добавляют рабочий раствор известной концентрации.
(5) Титрование –процесс постепенного добавления раствора точно известной концентрации к исследуемому раствору.
(6) Точка эквивалентности – установление конечной точки титрования.
Объемные методы анализа. Титрование как метод количественного определения вещества: прямое, косвенное и обратное
Метод объемного (титрометрического) анализа (2) это метод количественного определения, основанный на измерении объема реагента, требуемого для проведения реакции с определяемым веществом.
Объемные методы анализа основаны на протекании реакций нейтрализации, осаждения, ионного обмена, комплексообразования, окисления-восстановления и др. Они должны удовлетворять следующим условиям:
- строгое соблюдение стехиометрических соотношений между веществами реакций;
- быстрое и количественное протекание реакций;
- точное и строгое фиксирование точки эквивалентности;
- посторонние вещества в анализируемой пробе не должны вступать в реакцию с добавляемым реагентом, что может помешать титрованию.
Титрованием(5)называют процесс постепенного добавления раствора точно известной концентрации к исследуемому раствору.
Одной из основных стадий этого процесса, во многом определяющей точность объемного метода, является установление конечной точки титрования, называемой точкой эквивалентности (6). Точку эквивалентности определяют визуально по изменению цвета раствора, индикатора, появлению помутнения либо инструментальными методами кондуктометрическое, потенциометрическое титрование.
Для титрования достаточно 1-3 капель раствора индикатора массовой долей 0,1-0,5 % на 10-100 см3 анализируемого раствора.
Титрометрическое определение осуществляют прямым, косвенным и обратным титрованием.
Прямое титрование (4)наиболее распространенный и удобный прием, когда к анализируемому раствору вещества непосредственно добавляют рабочий раствор известной концентрации.
Косвенное титрование, или титрование заместителя (1), применяют, когда нет подходящей реакции или индикатора для прямого титрования. В этом случае используют реакцию, в которой анализируемое вещество замещают эквивалентным количеством другого вещества и затем титруют рабочим раствором.
Обратное титрование (3) используют в тех случаях, когда прямое титрование невозможно или когда анализируемое вещество неустойчиво. При этом берут два рабочих раствора, один из которых добавляют в избытке, а вторым титруют избыток первого.
Расчет массовой доли определяемого вещества Х (в %) через массовую концентрацию рабочего раствора ведут по формуле
Х=100 VСМ /(1000т), (5.5)
где V - объем рабочего раствора, пошедшего на титрование, см3;
С -молярная концентрация рабочего раствора, моль/дм3;
М - молекулярная эквивалентная масса определяемого вещества, г/моль;
m - масса навески анализируемого вещества, г.
6. ВИДЫ ДЕФЕКТОВ МЕТАЛЛА
6.1. Классификация дефектов
Дефектом называют каждое отдельное несоответствие продукции требованиям, установленным нормативной документацией (ГОСТ, ОСТ, ТУ и т.д.). К несоответствиям относятся нарушение сплошности материалов и деталей, неоднородность состава материала: наличие включений, изменение химического состава, наличие других фаз материала, отличных от основной фазы, и др.
Дефектами являются также любые отклонения параметров материалов, деталей и изделий от заданных, таких, как размеры, качество обработки поверхности, влаго- и теплостойкость и ряд других физических величин.
Дефекты подразделяются на явные (те, что выявляются глазами) и скрытые (внутренние, подповерхностные, неразличимые глазом).
В зависимости от возможного влияния дефекта на служебные свойства детали дефекты могут быть:
- критическими (дефекты, при наличии которых использование продукции по назначению невозможно или исключается по соображениям безопасности и надёжности);
- значительными (дефекты, существенно влияющие на использование продукции и/или на её долговечность, но не являющиеся критическими);
- малозначительными (не оказывают влияния на работоспособность продукции).
По происхождению дефекты изделий подразделяют на производственно-технологические (металлургические, возникающие при отливке и прокатке, технологические, возникающие при изготовлении, сварке, резке, пайке, клепке, склеивании, механической, термической или химической обработке и т.п.); эксплуатационные (возникающие после некоторой наработки изделия в результате усталости материала, коррозии металла, изнашивания трущихся частей, а также неправильной эксплуатации и технического обслуживания) и конструктивные дефекты, являющиеся следствием несовершенства конструкции из-за ошибок конструктора.
C целью выбора оптимальных методов и параметров контроля производится классификация дефектов по различным признакам: по размерам дефектов, по их количеству и форме, по месту расположения дефектов в контролируемом объекте и т.д.
Размеры дефектов a могут изменяться от долей миллиметров до сколь угодно большой величины. Практически размеры дефектов лежат в пределах 0,01 мм ≤ a ≤ 1 см.
В ультразвуковой дефектоскопии, например, величина а влияет на выбор рабочей частоты.
При количественной классификации дефектов различают три случая (рис. 6.1): а – одиночные дефекты, б – групповые (множественные) дефекты, в – сплошные дефекты (обычно в виде газовых пузырей и шлаковых включений в металлах).
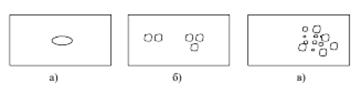
Рис. 6.1. Количественная классификация дефектов: а – одиночные;
б – групповые; в – сплошные
При классификации дефектов по форме различают три основных случая (рис. 6.2): а – дефекты правильной формы, овальные, близкие к цилиндрической или сферической форме, без острых краёв; б – дефекты чечевицеобразной формы, с острыми краями; в – дефекты произвольной, неопределённой формы, с острыми краями – трещины, разрывы, посторонние включения.
Форма дефекта определяет его опасность с точки зрения разрушения конструкции. Дефекты правильной формы, без острых краёв, наименее опасны, т.к. вокруг них не происходит концентрации напряжений. Дефекты с острыми краями, как на рис. 6.2, б и в, являются концентраторами напряжений. Эти дефекты увеличиваются в процессе эксплуатации изделия по линиям концентрации механических напряжений, что, в свою очередь, приводит к разрушению изделия.
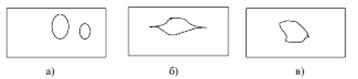
Рис. 6.2. Классификация дефектов по форме: а – правильная форма;
б – чечевицеобразная форма с острыми краями; в – произвольная,
неопределённая форма с острыми краями
При классификации дефектов по положению различают четыре случая (рис. 6.3): а – поверхностные дефекты, расположенные на поверхности материала, полуфабриката или изделия, – это трещины, вмятины, посторонние включения; б – подповерхностные дефекты – это дефекты, расположенные под поверхностью контролируемого изделия, но вблизи самой поверхности; в – объёмные дефекты – это дефекты, расположенные внутри изделия.
Наличие фосфовидных и нитридных включений и прослоек может привести к образованию дефектов четвертого вида – сквозных.
По форме поперечного сечения сквозные дефекты бывают круглые (поры, свищи, шлаковые включения) и щелевидные (трещины, непровары, дефекты структуры, несплошности в местах расположения оксидных и других включений и прослоек).
По величине эффективного диаметра (для дефектов округлого сечения) или ширине раскрытия (для щелей, трещин) сквозные дефекты подразделяются на обыкновенные (> 0,5 мм), макрокапиллярные (0,5…2·10-4 мм) и микрокапиллярные (< 2·10-4 мм).
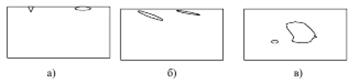
Рис. 6.3. Классификация дефектов по положению в контролируемом
объекте: а – поверхностные; б – подповерхностные; в – объёмные
По характеру внутренней поверхности сквозные дефекты подразделяются на гладкие и шероховатые. Относительно гладкой является внутренняя поверхность шлаковых каналов. Внутренняя поверхность трещин, непроваров и вторичных поровых каналов, как правило, шероховатая.
Положение дефекта влияет как на выбор метода контроля, так и на его параметры. Например, при ультразвуковом контроле положение дефекта влияет на выбор типа волн: поверхностные дефекты лучше всего определяются рэлеевскими волнами, подповерхностные – головными волнами, а объёмные – объёмными (продольными) волнами.
Опасность влияния дефектов на работоспособность зависит от их вида, типа и количества. Классификация возможных дефектов в изделии позволяет правильно выбрать метод и средства контроля.
6.2. Производственно-технические дефекты
Дефекты в металлах образуются главным образом при плавлении, при обработке металла давлением (ковка, штамповка и прокат) и при шлифовании.
По ГОСТ 19200-80 дефекты отливок из чугуна и стали подразделяют на пять основных групп. Необходимо отметить, что принятая терминология широко используется также для отливок из сплавов на основе алюминия, магния, титана и других и поэтому может рассматриваться как универсальная.
6.2.1. Литейные дефекты
Несоответствие по геометрии.
Эта группа объединяет 14 видов дефектов, обусловленных нарушением формы, неточностью размеров и массы отливки.
1. Недолил - дефект в виде неполного образования отливки вследствие незаполнения полости формы металлом (рис. 6.4. а). Одной из основных причин недолива является недостаточное количество жидкого металла.
2. Незалив - несоответствие конфигурации отливки чертежу вследствие износа модельной оснастки или дефектов формы (рис. 6.4. б). Причиной незалива может быть также нарушение технологических режимов заливки.
3. Неслитина - сквозная щель или отверстие в стенке отливки, образовавшееся вследствие неслияния встречных потоков металла (рис. 6.4. в). Неслитина характерна для сплавов с широким интервалом кристаллизации и наблюдается обычно в тонких стенках отливок. Эти дефекты легко обнаруживаются при визуальном осмотре отливок.
4. Обжим - это местное нарушение конфигурации отливки вследствие деформации формы при ее сборке или заливке (рис. 6.4. г). Обжим обычно образуется вблизи плоскости разъема в виде прилива или утолщения произвольной формы.
5. Подутость представляет собой местное утолщение отливки, возникшее вследствие расширения недостаточно уплотненной формы заливаемым металлом (рис. 6.4. д).

 6-8. Перекос и стержневой перекос - дефекты в виде смещения одной части отливки относительно осей или поверхностей другой части по разъему формы, модели вследствие их неточной установки (рис. 6.4. е) или в виде смещения отверстия, полости или части отливки, выполняемых с помощью стержня, вследствие его перекоса (рис. 6.4. ж). Эти дефекты вызваны неточной фиксацией опок или перекосом стержня при его установке. В последнем случае возникает также разностенность - увеличение или уменьшение толщины стенок отливки (рис. 6.4. з). Разностенность выявляется визуально или с помощью измерительных средств.
6-8. Перекос и стержневой перекос - дефекты в виде смещения одной части отливки относительно осей или поверхностей другой части по разъему формы, модели вследствие их неточной установки (рис. 6.4. е) или в виде смещения отверстия, полости или части отливки, выполняемых с помощью стержня, вследствие его перекоса (рис. 6.4. ж). Эти дефекты вызваны неточной фиксацией опок или перекосом стержня при его установке. В последнем случае возникает также разностенность - увеличение или уменьшение толщины стенок отливки (рис. 6.4. з). Разностенность выявляется визуально или с помощью измерительных средств.
9. Стержневой залив - дефект в виде залитого металлом отверстия или полости в отливке, возникающий из-за непроставленного в литейной форме стержня или его обрушения (рис. 6.4. и).
10. Коробление - искажение конфигурации отливки под влиянием напряжений, возникающих при охлаждении отливки или вследствие деформации модельной оснастки. Коробление может проявляться в различных формах, наиболее характерным является появление вогнутости или выпуклости на плоских поверхностях отливок (рис. 6.4. к). Дефект выявляется с помощью измерительных средств. Стрела прогиба 6 может служить мерой коробления.
11. Вылом и зарез - дефекты в виде нарушений конфигурации отливки при выбивке стержней, обрубке литников (рис. 6.4. л), зачистке отливок или их транспортировании.
12. Прорыв и уход металла - дефекты, вызванные вытеканием металл.* из формы вследствие ее недостаточной прочности или слабого крепления ее частей. При этом либо происходит неполное заполнение полости формы с одновременным образованием приливов произвольной формы, либо возникает дефект в виде пустоты в теле отливки, ограниченной тонкой коркой затвердевшего металла (рис. 6.4. м).
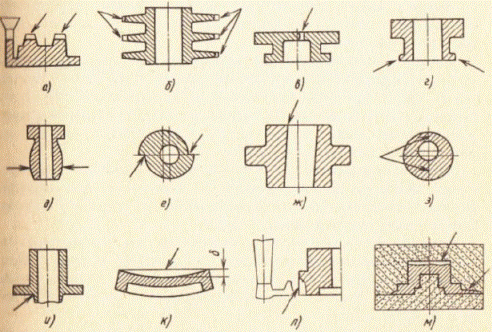
Рис. 6.4. Дефекты отливок - несоответствие по геометрии (стрелки указывают на расположение дефекта)
Дата добавления: 2016-01-26; просмотров: 5202;
