Декарбоксилирование аминокислот
| ||||||||||||
| NH2 | — | CH | — | COOH | 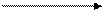
| CH3 | — | CH2 | — | NH2 | ||
| | | ||||||||||||
| CH3 | ||||||||||||
| аланин | этиламин |
| ||||||||||
| NH2 | — | CH | — | COOH | 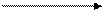
| NH2 | — | CH2 | ||
| | | | | |||||||||
| CH2 | CH2 | |||||||||

| 
| |||||||||
| гистидин | гистамин |
| ||||||||||||
| NH2 | — | CH | — | COOH | 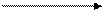
| NH2 | — | CH2 | ||||
| | | | | |||||||||||
| CH2 | 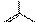
| CH2 | |||||||||
| тирозин | тирамин |
декарбоксилаза
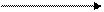 Аргинин агматин + СО2
Аргинин агматин + СО2
декарбоксилаза
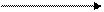 Лизин кадаверин + СО2
Лизин кадаверин + СО2
(Написать в виде уравнений реакций)
Гистамин снижает кровяное давление, усиливает деятельность желёз внутренней секреции. Тирамин повышает кровяное давление и при его распаде образуются токсичные фенолы. Агматин и кадаверин влияют на работу рибосом.
РЕАКЦИИ ПО РАДИКАЛУ
Радикалы аминокислот различны, поэтому для них характерны разные типы реакций:
1) Окисление
| NH2 | — | CH | — | COOH | ||||||||
| | | ||||||||||||
| CH2 | ||||||||||||
| 2NH2 | — | CH | — | COOH | | | |||||||
| | |
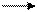
| S | ||||||||||
| CH2 | | | |||||||||||
| | | S | |||||||||||
| SH | | | |||||||||||
| CH2 | ||||||||||||
| | | ||||||||||||
| NH2 | — | CH | — | COOH | ||||||||
| цистеин | цистин (цис-цис) |
2) Декарбоксилирование
| NH2 | — | CH | — | COOH | 
| NH2 | — | CH | — | COOH |
| | | | | |||||||||
| CH2 | CH3 | |||||||||
| | | ||||||||||
| COOH | ||||||||||
| аспарагиновая кислота | аланин |
3) Одновременно несколько типов реакций

|
| 
| ||||||||||||||

| ||||||||||||||||
| ||||||||||||||||

| ||||||||||||||||
| CH2 | CH | — | OH | |||||||||||||
| | | | | |||||||||||||||
| NH2 | — | CH | — | COOH | CH3 | — | NH | — | CH2 | |||||||
| тирозин | адреналин |
3-й вопрос
Если в процессе вышеуказанных реакций образуется аминокислота, то можно считать, что эта реакция является реакцией синтеза данной аминокислоты. Амиды аминокислот аспарагин и глутамин синтезируются из аспарагиновой и глутаминовой кислот с присоединением аммиака.
Аммиак образуется при дезаминировании аминокислот, которое протекает четырьмя путями (окислительное, восстановительное, гидролитическое и внутримолекулярное дезаминирование). Аммиак только у некоторых животных гидросферы, в частности у речного рака, крабов, креветок, непосредственно выводится из организма в окружающую среду или в виде солей аммония. Для большинства растительных и животных организмов аммиак токсичен и даже в небольших количествах оказывает влияние на жизнедеятельность организма. Особенно чувствительна к аммиаку ЦНС животных.
Аминокислоты асп и глу тут же связывают образующийся аммиак, в результате образуются два амида асн и глн. В процессе образования амидов участвуют два фермента – аспарагинсинтетаза и глутаминсинтетаза. (Представить в виде уравнения реакции)
Асп + АТФ аспарагинсинтетаза Асн + АДФ + Ф(н)
 Глу + АТФ глутаминсинтетаза Глн + АДФ + Ф(н)
Глу + АТФ глутаминсинтетаза Глн + АДФ + Ф(н)
Установлено, что аммиак связывается не только свободными асп и глу, а также белком. Такой белок получил название амидированный белок. Связывание аммиака белком идет по месту радикалов этих же асп и глу, которые могут находится в молекулах белка в разных позициях.
Аммиак связывается в первую очередь белком мышц миозином. Этим обеспечивается немедленное связывание и обезвреживание аммиака в той точке, где он образуется в процессе обмена веществ. Т.о моноаминодикарбоновые кислоты асп и глу находятся в свободном состоянии, а также входящие в состав белков связывают аммиак. Образовавшиеся амиды – безвредная транспортная форма аммиака, из которой он освобождается и выделяется с мочой в виде солей аммония или мочевины. Свободные амины участвуют в синтезе специфических белков.
Синтез белков осуществляется на рибосоме клеток и уравнения реакции можно представить следующим образом:
О О
// //
 NH2 - СН – C – ОH + Н – N – СН – С – OH + Н – N – СН – С – OH ……
NH2 - СН – C – ОH + Н – N – СН – С – OH + Н – N – СН – С – OH ……
/ / / / / - nН2О
СН3 Н СН2 Н СН2
/ /
ОН SН
О О О
// // //
NH2 – СН – C – N – СН – С – N – СН – C – ……..
/ / / / /
СН3 Н СН2 Н СН2
/ /
ОН SН
Аланил-серил-цистеил….
Дата добавления: 2016-01-26; просмотров: 771;
