Аминокислоты. Пептиды
Аминокислоты — это производные органических кислот, получающиеся в результате замещения одного или нескольких атомов водорода в углеводородных радикалах на одну или несколько

аминогрупп (—NH2). Можно считать формулу H2N—R—COOH общей формулой простейших аминокислот.
Названия аминокислот производятся от названий соответствующих кислот с добавлением приставки амино-,например:

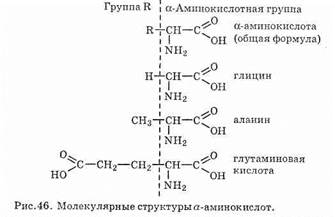
Аминокислоты, входящие в состав белков, имеют также исторически сложившиеся практические названия, например, аминоуксусная кислота иначе называется глицином (или гликоколом), аминопропионовая — аланином и т.д. (см. табл. 40).
В зависимости от взаимного расположения функциональных групп различают a-, b-, g-аминокислоты. В состав аминокислот может входить разное количество функциональных групп (см. табл. 40, рис. 46).
При образовании названий аминокислот указывается местоположение аминогруппы (a — 1, b — 2, g — 3 и т. п.) по отношению к —СООН группе.
Изомерия аминокислот зависит от:
1) строения углеродного скелета;
2) положения функциональных групп;
3) для некоторых аминокислот характерна оптическая изомерия, обусловленная наличием в молекуле аминокислоты асимметрических атомов углерода.
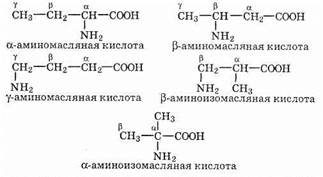
Рассмотрим в качестве примера формулы изомерных соединений состава C3H6(NH2)COOH:
1. Гидролиз белков. В результате гидролиза белковых веществ обычно образуются сложные смеси аминокислот. Затем из сложных смесей получают отдельные чистые аминокислоты.
2. Замещение галогена на аминогруппу в галогенкарбоновых кислотах. Этот способ получения аминокислот полностью анало-
гичен получению аминов из галогенопроизводных алканов и аммиака:

3. Присоединение аммиака к a-, b-непредельным кислотам, при этом образуются b-аминокислоты:
СН2=CH-СООН+NH3®H2N-CH2-CH2-COOH
Физические свойства
Аминокислоты — твердые кристаллические вещества, многие сладкие на вкус.
Аминокислоты существуют в форме внутренних солей (биполярных ионов):
[H2N-CH2-COOH]®Н3N+-СН2-СОO-
Такое строение приводит к высокой растворимости аминокислот в воде, причем не только низших, но и содержащих достаточно большой углеводородный радикал. Аминокислоты мало растворимы в органических растворителях. Они плавятся при высоких температурах, разлагаясь при этом. Аминокислоты не могут переходить в парообразное состояние.
Химические свойства и применение
Так как аминокислоты содержат в составе молекулы две функциональные группы противоположного характера (аминогруппу с основными свойствами и карбоксильную группу с кислотными свойствами), то их можно рассматривать по химическим свойствам как органические амфотерные соединения. Амфотерность аминокислот позволяет им реагировать как с кислотами, так и с основаниями:
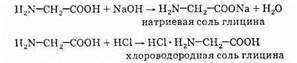
Таким образом, при повышении концентрации ионов ОН-аминокислоты реагируют в форме аниона (как кислота), а при повышении концентрации ионов Н+ в форме катиона (как основание), т.е.
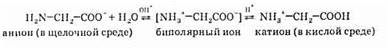
Аминокислоты взаимодействуют с металлами, оксидами металлов, образуя соли, а также со спиртами, образуя сложные эфиры.
Специфика свойств аминокислот приводит к тому, что две молекулы аминокислоты могут реагировать друг с другом с отщеплением молекулы воды и образованием продукта, в котором фрагменты связаны пептидной связью:
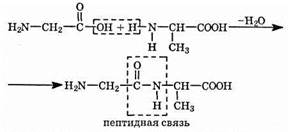
Соединения с пептидной связью относятся к классу амидов кислот. Полученное соединение называют дипептидом. Если продукт реакции содержит три остатка аминокислоты, то он будет называться трипептидом. Вещества, построенные из многих остатков аминокислот, называются полипептидами. Полипептидная цепь, которая содержит повторяющуюся последовательность аминокислот, является полимером. Примером может служить полиамид — капрон.
nH2N-(CH2)5-COOH®(-NH-(CH2)5-CO-)n+(n-1)H2O
Внутримолекулярное отщепление воды приводит к образованию циклических соединений, носящих название лактамов:
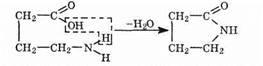
Особенно легко протекает образование пяти- и шестичленных циклических амидов.
При действии азотистой кислоты на аминокислоты из последних получаются оксикислоты:
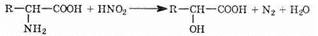
a-аминокислоты играют особую роль в природе, поскольку при их совместной поликонденсации в природных условиях образуются важнейшие для жизни вещества — белки. В состав белков входят лишь некоторые из возможных a-аминокислот. В боль-
шинстве белков встречаются лишь двадцать аминокислот, часть из которых приведена в табл. 40. Некоторые из этих аминокислот не могут быть синтезированы животными организмами и называются незаменимыми. Они поступают в организм с пищей.
Многие аминокислоты применяются в медицине как лечебные средства, а некоторые используются в сельском хозяйстве для подкормки животных.
Неразветвленные аминокислоты, как бифункциональные (содержащие две функциональные группы) мономеры, используются для производства синтетических волокон, в том числе капрона и энанта. Энант получают поликонденсацией w-аминоэнантовой кислоты: H2N-(CH2)6-COOH
Рассмотрим получение полимера, из которого производят капроновое волокно. Первым этапом является поликонденсация e-аминокапроновой кислоты:
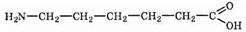
В производстве капронового волокна применяют не непосредственно e-аминокапроновую кислоту, а ее производное — капролактам, являющийся продуктом взаимодействия функциональных групп молекул кислоты:
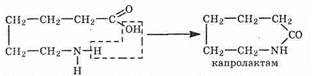
При синтезе под влиянием воды молекулы капролактама превращаются в молекулы e-аминокапроновой кислоты, которые подвергаются поликонденсации:
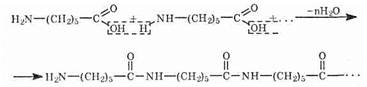
Как видно из формулы, молекула образующегося полимера состоит из многократно повторяющихся остатков e-аминокапроновой кислоты, а связи между остатками возникают в результате отщепления молекул воды.
Строение полученного полимера можно выразить формулой:
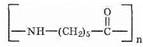
Он имеет вид смолы. Для получения волокон смолу плавят, продавливают через фильеры, затем волокна подвергают специальной обработке, после чего скручивают в нити. Изделия из капрона нашли широкое применение в быту. Капроновая смола используется для изготовления прочных и износоустойчивых деталей машин и механизмов.
Дата добавления: 2016-01-03; просмотров: 2894;
