Наджелудочковые нарушения ритма
Синусовая тахикардия
Синусовая тахикардия (СТ) — это увеличение ЧСС до 100 уд. в мин и более при сохранении правильного синусового ритма. СТ обусловлена повышением автоматизма СА-узла.
Диагностическое и прогностическое значение синусовой тахикардии определяется конкретной клинической ситуацией, при которой она возникает. Так, синусовая тахикардия является нормальным ответом сердечно-сосудистой системы на физическую нагрузку, психоэмоциональный стресс, употребление крепкого кофе и т.п. В этих случаях синусовая тахикардия носит временный характер и, как правило, не сопровождается неприятными ощущениями. Восстановление нормальной ЧСС происходит вскоре после прекращения действия факторов, вызывающих тахикардию.
Клиническое значение имеет синусовая тахикардия, сохраняющаяся в покое. Нередко она сопровождается неприятными ощущениями сердцебиений, чувством нехватки воздуха, хотя некоторые больные могут не замечать увеличения ЧСС. Причинами такой тахикардии могут быть как экстракардиальные факторы, так и собственно заболевания сердца. К числу экстракардиальных факторов, вызывающих синусовую тахикардию, относятся:
· гипертиреоз;
· лихорадка;
· острая сосудистая недостаточность;
· дыхательная недостаточность;
· анемии;
· некоторые варианты нейроциркуляторной дистонии, сопровождающиеся активацией САС;
· применение некоторых лекарственных препаратов (симпатомиметиков, эуфиллина, кофеина, глюкокортикоидов, периферических вазодилататоров, блокаторов медленных кальциевых каналов, a-адреноблокаторов, диуретиков, курантила и т.д.).
Характерно, что некоторые из перечисленных ЛС (например, антагонисты кальция дигидропиридиновой группы) не оказывают прямого влияния на функцию СА-узла, вызывая так называемую рефлекторную тахикардию.
Интракардиальные факторы. Возникновение синусовой тахикардии у больных с заболеваниями сердца в большинстве случаев (хотя и не всегда) свидетельствует о наличии сердечной недостаточности или дисфункции ЛЖ. В этих случаях прогностическое значение синусовой тахикардии может быть достаточно серьезным, поскольку она отражает реакцию сердечно-сосудистой системы на снижение ФВ или клинически значимые нарушения внутрисердечной гемодинамики. Наиболее частыми причинами интракардиальной формы синусовой тахикардии являются:
· хроническая СН;
· инфаркт миокарда;
· тяжелый приступ стенокардии у больных ИБС;
· острый миокардит;
· кардиомиопатии и др.
ЭКГ-признакиСТ(рис. 3.23, б):
1. ЧСС больше 90 в мин.
2. Сохранение правильного синусового ритма.
| Рис. 3.23. Номотопные нарушения ритма. а — ЧСС — 75 в мин; б — синусовая тахикардия (ЧСС — 150 в мин); в — синусовая брадикардия (ЧСС — 50 в мин); г — синусовая (дыхательная) аритмия | 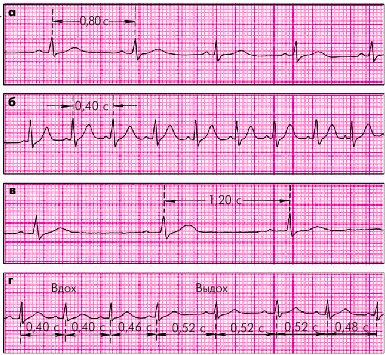
|
3. Положительный зубец РI, II, aVF, V4—.
4. При выраженной СТ наблюдаются:
- укорочение интервала P–Q(R) (но не меньше 0,12 с) и продолжительности интервала Q–T;
- увеличение амплитуды РI, II, aVF;
- увеличение или снижение амплитуды зубца Т;
- косовосходящая депрессия сегмента RS–T (но не более 1,0 мм ниже изолинии).
Следует помнить, что диагноз синусовой тахикардии может быть установлен только по данным ЭКГ, поскольку увеличение в покое ЧСС от 100 до 120–140 в мин с сохранением правильного ритма может встречаться при некоторых эктопических аритмиях:
- ускоренных ритмах (непароксизмальной тахикардии) из предсердий, АВ-соединения и желудочков (см. ниже);
- правильной форме трепетания предсердий (2 : 1; 3 : 1 и т.д.).
Синусовая брадикардия
Синусовая брадикардия (СБ) — это урежение ЧСС меньше 60 уд. в мин при сохранении правильного синусового ритма. Синусовая брадикрадия обусловлена понижением автоматизма СА-узла.
У здоровых людей синусовая брадикардия обычно свидетельствует о хорошей тренированности сердечно-сосудистой системы и часто встречается у спортсменов.
Причинами экстракардиальной формы синусовой брадикардии, обусловленной токсическими воздействиями на СА-узел или преобладанием активности парасимпатической нервной системы (вагусные воздействия), являются:
- гипотиреоз;
- повышение внутричерепного давления;
- передозировка ЛС (b-адреноблокаторов, сердечных гликозидов, веропамила и др.);
- некоторые инфекции (вирусный гепатит, грипп, брюшной тиф, сепсис);
- гиперкальциемия или выраженная гиперкалиемия;
- метаболический алкалоз;
- обтурационная желтуха;
- гипотермия и др.
Интракардиальная форма синусовой брадикардии возникает при органическом или функциональном повреждении СА-узла и встречается при ИМ, атеросклеротическом и постинфарктном кардиосклерозе и других заболеваниях сердца. Интракардиальная форма синусовой брадикардии нередко сопровождается другими признаками синдрома слабости синусового узла (СССУ — см. ниже).
ЭКГ-признаки(рис. 3.23, в):
1. Уменьшение ЧСС до 59 и ниже в мин.
2. Сохранение правильного синусового ритма.
3. Положительный зубец РI, II, aVF, V4—.
Для синусовой брадикардии экстракардиального происхождения, развившейся вследствие ваготонии, характерно увеличение ЧСС при физической нагрузке и введении атропина и частое сочетание с синусовой дыхательной аритмией. При органической синусовой брадикардии (интракардиальная форма) дыхательная аритмия отсутствует, после введения атропина ритм не учащается, а при физической нагрузке ЧСС увеличивается незначительно.
Синусовую брадикардию следует дифференцировать с другими нарушениями ритма, для которых также характерно уменьшение ЧСС и сохранение регулярных сердечных сокращений:
· медленный (замещающий) ритм из АВ-соединения;
· медленный (замещающий) идиовентрикулярный ритм;
· синоатриальная блокада II степени 2 : 1;
· АВ-блокада III степени.
Распознавание этих видов аритмий возможно только с помощью ЭКГ-исследования (см. ниже).
Синусовая аритмия
Синусовой аритмией (СА) называют неправильнй синусовый ритм, характеризующийся периодами учащения и урежения ритма. Синусовая аритмия вызывается нерегулярным образованием импульсов в СА-узле в результате: 1) рефлекторного изменения тонуса блуждающего нерва в связи с фазами дыхания; 2) самопроизвольного изменения тонуса n.vagi вне связи с дыханием; 3) органического повреждения СА-узла. Различают дыхательную и недыхательную формы синусовой аритмии.
ДыхательнаяСА часто встречается у молодых здоровых людей, детей, больных НЦД и реконвалесцентов. Она характеризуется учащением сердцебиений на вдохе и замедлением на выдохе, причем колебания интервалов R–R на ЭКГ превышают 0,15 с и ритм сердца становится неправильным (рис. 3.23, г).
Напомним, что у здорового взрослого человека также постоянно наблюдаются небольшие колебания ритма сердца, связанные с дыхательными движениями (рефлекс Бейера–Геринга) и обусловленные физиологическим изменением тонуса вегетативной нервной системы. Появление синусовой дыхательной аритмии (т.е. более выраженных дыхательных колебаний ЧСС) отражает некоторый дисбаланс вегетативной нервной системы с явным преобладанием активности парасимпатической нервной системы. Поэтому синусовая дыхательная аритмия нередко сочетается с синусовой брадикардией, также обусловленной преобладанием вагусных воздействий.
Наличие дыхательной формы СА у больных с органическими заболеваниями сердца в целом является неплохим признаком. Прогноз становится более тяжелым, если у больного с органическим поражением сердца исчезает дыхательная вариация вагусных влияний и начинает превалировать САС, гиперактивация которой, наряду со снижением ФВ ЛЖ, ассоциируется с более высоким риском ИМ и внезапной сердечной смерти.
ЭКГ-признаки дыхательной формы СА (рис. 3.23, г):
1. Дыхательные колебания длительности интервалов R–R, превышающие 0,15 с.
2. Сохранение синусового ритма.
3. Исчезновение аритмии при задержке дыхания.
Недыхательная формаСАобусловлена органическим повреждением СА-узла или прилегающего миокарда, что приводит к апериодичности образования импульсов, не зависящей от дыхательных движений.
ЭКГ-признаки недыхательной формы СА:
1. Постепенное (периодическая форма) или скачкообразное (апериодическая форма) изменение продолжительности R–R (больше 0,15 с).
2. Сохранение синусового ритма.
3. Сохранение аритмии при задержке дыхания.
 Запомните
1. Задержка дыхания ведет к исчезновению дыхательной формы СА, тогда как недыхательная форма СА сохраняется. 2. Синусовая дыхательная аритмия, обусловленная функциональной ваготонией, усиливается при приеме b-адреноблокаторов и прекращается под влиянием атропина. При органическом повреждении СА-узла, сопровождающемся недыхательной формой СА, эти фармакологические тесты оказываются отрицательными. Запомните
1. Задержка дыхания ведет к исчезновению дыхательной формы СА, тогда как недыхательная форма СА сохраняется. 2. Синусовая дыхательная аритмия, обусловленная функциональной ваготонией, усиливается при приеме b-адреноблокаторов и прекращается под влиянием атропина. При органическом повреждении СА-узла, сопровождающемся недыхательной формой СА, эти фармакологические тесты оказываются отрицательными.
|
Синдром слабости синоатриального узла
В основе синдрома слабости синусового узла (СССУ) лежит снижение функции автоматизма СА-узла и/или замедление проведения импульса от клеток СА-узла к ткани предсердий.
Различают первичный и вторичный СССУ. Первичный (“истинный”) СССУ развивается в результате органического повреждения СА-узла у больных ИБС, ИМ, миокардитом, кардиомиопатией и др., а также при выраженной интоксикации сердечными гликозидами, b-адреноблокаторами, хинидином. СССУ может возникнуть в результате гормонально-обменных нарушений, а также после купирования приступа пароксизмальной тахикардии или мерцательной аритмии.
Вторичный СССУ характеризуется снижением функции СА-узла, обусловленным, главным образом, выраженным нарушением вегетативной регуляции с преобладанием тонуса парасимпатической нервной системы (“вагусный” СССУ).
У больных СССУ, как правило, наблюдается стойкая синусовая брадикардия. Характерно, что при пробе с дозированной физической нагрузкой или после введения атропина у них отсутствует адекватное учащение сердечных сокращений. В результате значительного снижения функции автоматизма основного водителя ритма — СА-узла — создаются условия для периодической замены синусового ритма на ритмы из центров автоматизма II и III порядка. При этом возникают несинусовые эктопические ритмы (чаще предсердные, из АВ-соединения, фибрилляция и трепетание предсердий). Нередко при СССУ возникает также нарушение проведения электрического импульса из СА-узла к предсердиям — синоатриальная блокада. Наконец, весьма характерно для больных с СССУ чередование периодов выраженной брадикардии и тахикардии (синдром тахикардии–брадикардии) в виде периодического появления на фоне редкого синусового ритма приступов эктопической тахикардии, мерцания и трепетания предсердий (см. ниже).
Жалобы больных чаще связаны с недостаточностью мозгового кровообращения: периодически возникающие головокружения, кратковременная потеря сознания (синкопе), особенно при быстрой перемене положения тела. В тяжелых случаях могут возникнуть приступы Морганьи–Адамса–Стокса (см. ниже) с внезапной потерей сознания и эпилептиформными судорогами. Возникновение пароксизмов наджелудочковой тахикардии или фибрилляции предсердий сопровождается ощущением сердцебиений. Снижение систолической функции ЛЖ проявляется субъективными и объективными симптомами СН.
ЭКГ-признаки:
1. Стойкая синусовая брадикардия.
2. Пароксизмы эктопических ритмов (чаще в виде суправентрикулярной тахикардии, мерцания и трепетания предсердий).
3. Наличие СА-блокады.
4. Синдром тахикардии–брадикардии (возникновение на фоне синусовой брадикардии приступов суправентрикулярных тахиаритмий).
Наиболее полная диагностическая информация о нарушениях функции СА-узла у больных СССУ может быть получена только при применении дополнительных методов исследования:
· длительного мониторирования ЭКГ по Холтеру;
· пробы с дозированной физической нагрузкой;
· фармакологических проб;
· внутрисердечного ЭФИ;
· чреспищеводной электрической стимуляции предсердий (ЧПЭС).
Холтеровское мониторирование ЭКГ дает возможность выявить практически все возможные нарушения ритма и проводимости, характерные для СССУ (синусовую брадикардию, преходящие СА-блокады, короткие эпизоды наджелудочковой тахикардии, медленные замещающие ритмы и комплексы, миграцию суправентрикулярного водителя ритма и др.). Результаты мониторирования ЭКГ помогают, таким образом, получить объективное подтверждение диагноза СССУ.
Пробы с дозированной физической нагрузкой (тредмил-тест или велоэргометрия) и фармакологические пробы позволяют уточнить, связана ли синусовая брадикардия и другие проявления дисфункции СА-узла с повышением тонуса блуждающего нерва (вторичный СССУ) или имеются органические изменения СА-узла (первичный СССУ).
В отличие от пациентов с нормальной функцией СА-узла, у больных с первичным СССУ ЧСС на фоне физической нагрузки, сопровождающейся, как известно, значительной активацией САС, возрастает менее чем на 15–20% по сравнению с исходной величиной. У пациентов с вторичным СССУ физическая нагрузка приводит к значительному увеличению ЧСС.
Такой же результат может быть получен при внутривенном введении 1 мл 0,1% раствора атропина. При первичном СССУ после введения атропина ЧСС возрастает не более чем на 8–10 уд. в мин, тогда как у пациентов с вторичным (“вагусным”) СССУ, так же как и у здоровых лиц, ЧСС возрастает не менее чем на 25–30% по сравнению с исходным уровнем.
Внутрисердечное (эндокардиальное) ЭФИ или ЧПЭС дает более точное количественное представление о функциональном состоянии СА-узла. В клинике чаще используют метод ЧПЭС. При помощи электрода, установленного в пищеводе на уровне ЛП, проводят электрическую стимуляцию сердца. Вначале искусственный ритм, навязанный сердцу электрокардиостимулятором (ЭКС), на 5–10 уд. в мин превышает исходный собственный синусовый ритм. Стимуляцию проводят в течение 1–2 мин. Затем постепенно ступенеобразно каждые 3–5 мин повышают частоту искусственных стимулов, доводя ЧСС до 150–170 в мин. После этого отключают ЭКС и измеряют время, в течение которого происходит восстановление функции СА-узла (СА-узла ">ВВФСУ), которое соответствует первому самостоятельному возбуждению предсердий — первому зубцу Р (рис. 3.24).
 Запомните
Время восстановления функции СА-узла (СА-узла ">ВВФСУ) количественно характеризует функцию автоматизма СА-узла. В норме СА-узла ">ВВФСУ не превышает 1400 мс. Удлинение СА-узла ">ВВФСУ свидетельствует об угнетении автоматизма СА-узла и позволяет диагностировать СССУ. Запомните
Время восстановления функции СА-узла (СА-узла ">ВВФСУ) количественно характеризует функцию автоматизма СА-узла. В норме СА-узла ">ВВФСУ не превышает 1400 мс. Удлинение СА-узла ">ВВФСУ свидетельствует об угнетении автоматизма СА-узла и позволяет диагностировать СССУ.
|
| Рис. 3.24. Измерение длительности ВВФСУ при нормальной функции СА-узла (а) и при синдроме слабости СА-узла (б). Объяснение в тексте | 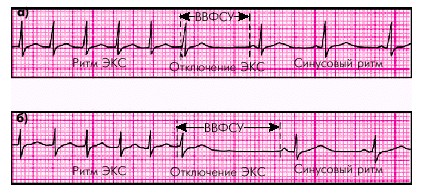
|
Обычно при увеличении СА-узла ">ВВФСУ исследование повторяют через 5 мин после внутривенного введения 1,0 мл 0,1% раствора атропина. При вторичном СССУ (“вагусном”) введение атропина приводит к нормализации СА-узла ">ВВФСУ и увеличению ЧСС, что доказывает экстракардиальную причину дисфункции СА-узла. При наличии органических изменений СА-узла СА-узла ">ВВФСУ после введения атропина практически не изменяется (первичный СССУ).
Следует заметить, что чувствительность описанного критерия диагностики СССУ (СА-узла ">ВВФСУ) колеблется в пределах 50–60%, хотя специфичность достигает 95%. В связи с этим для оценки степени угнетения автоматизма СА-узла используют и другие количественные показатели, получаемые при проведении ЧПЭС или внутрисердечного ЭФИ.
Медленные (замещающие) выскальзывающие ритмы и комплексы
Медленные (замещающие) выскальзывающие ритмы и комплексы — это несинусовые эктопические ритмы или отдельные сокращения, источником которых являются предсердия, АВ-соединение или желудочки.
Медленные (замещающие) выскальзывающие ритмы и комплексы относятся к пассивным эктопическим нарушениям ритма. Они возникают на фоне временного снижения функции СА-узла, синусовой и других форм брадикардии (СА- и АВ-блокады II и III степени и т.п.). В этих случаях синусовые импульсы или не доходят до центров автоматизма II и III порядка, или приходят к ним с большим опозданием, в связи с чем эти центры начинают функционировать самостоятельно, выходя (“выскальзывая”) из-под контроля СА-узла. Таким образом, медленные (замещающие) выскальзывающие ритмы и комплексы как бы защищают сердце от длительных периодов асистолии, вызванных угнетением синусовых функций.
Описанные нарушения ритма встречаются при самой различной функциональной или органической патологии сердца: выраженной ваготонии, НЦД, при органических поражениях СА-узла (кардиосклероз, острый ИМ и др.) и любых других причинах, ведущих к возникновению брадикардии, СА- и АВ-блокад и т.п.
ЭКГ-признаки: Медленные выскальзывающие комплексы (рис. 3.25):
1. Наличие на ЭКГ отдельных несинусовых комплексов, источником которых являются импульсы, исходящие из предсердий, АВ-соединения или желудочков.
2. Интервал R–R, предшествующий выскальзывающему эктопическому комплексу, удлинен, а следующий за ним R–R нормальный или укорочен.
| Рис. 3.25. ЭКГ больных с медленными (замещающими) выскальзывающими эктопическими комплексами. а, б — выскальзывающие комплексы из АВ-соединения; в — выскальзывающий комплекс из желудочка | 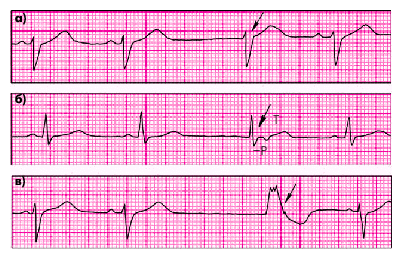
|
Медленные выскальзывающие ритмы (рис. 3.26):
1. Правильный ритм с ЧСС 60 ударов в мин и меньше.
2. Наличие в каждом комплексе P–QRS признаков несинусового (предсердного, из АВ-соединения или желудочкового) водителя ритма.
Чаще встречаются выскальзывающие ритмы и комплексы из АВ-соединения, обладающего более высоким автоматизмом, чем специализированные волокна системы Гиса– Пуркинье. Появление на ЭКГ желудочковых (замещающих) выскальзывающих комплексов и ритмов свидетельствует об угнетении автоматизма не только СА-узла, но и АВ-соединения.
| Рис. 3.26. ЭКГ больных с медленными (замещающими) выскальзывающими ритмами. а — предсердный ритм; б — ритм из АВ-соединения с одновременным возбуждением желудочков и предсердий; в — ритм из АВ-соединения с возбуждением желудочков, предшествующим возбуждению предсердий; г — желудочковый (идиовентрикулярный) ритм | 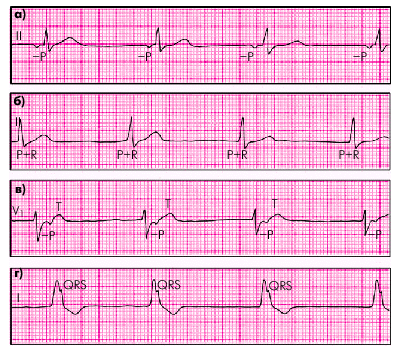
|
Ускоренные эктопические ритмы (непароксизмальная тахикардия)
Ускоренные эктопические ритмы, или непароксизмальная тахикардия — это неприступообразное учащение сердечного ритма до 100–130 в минуту, вызванное относительно частыми эктопическими импульсами, исходящими из предсердий, АВ-соединения или желудочков. Таким образом, ЧСС при ускоренных эктопических ритмах выше, чем при медленных замещающих ритмах, и ниже, чем при пароксизмальной тахикардии (см. ниже).
Возникновение ускоренных эктопических ритмов связано с усилением автоматизма центров II и III порядков (ускорение спонтанной диастолической деполяризации пейсмекеров) или с триггерной активностью АВ-соединения (появление поздних задержанных постдеполяризаций).
Основными причинами ускоренных эктопических ритмов являются:
- дигиталисная интоксикация (наиболее частая причина);
- острый ИМ (преимущественно первые 1–2 суток);
- хронические формы ИБС;
- легочное сердце;
- операции на сердце (в том числе протезирование клапанов) и др.
ЭКГ-признаки (рис. 3.27):
1. Неприступообразное постепенное учащение сердечного ритма до 100–130 в мин.
2. Правильный желудочковый ритм.
3. Наличие в каждом зарегистрированном комплексе P–QRS–T признаков несинусового (предсердного, из АВ-соединения или желудочкового) водителя ритма.
| Рис. 3.27. Ускоренные эктопические ритмы, или непароксизмальные тахикардии. а — ускоренный предсердный ритм; б — ускоренный ритм из АВ-соединения с одновременным возбуждением желудочков и предсердий; в — желудочковый (идиовентрикулярный) ускоренный ритм | 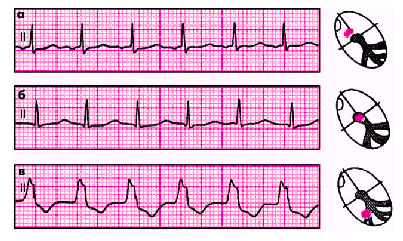
|
Миграция суправентрикулярного водителя ритма
Миграция суправентрикулярного водителя ритма характеризуется постепенным, от цикла к циклу, перемещением источника ритма от СА-узла к АВ-соединению и обратно. Последовательные сокращения сердца каждый раз обусловлены импульсами, исходящими из разных участков проводящей системы сердца: из СА-узла, из верхних или нижних отделов предсердий, из АВ-соединения. Такая миграция водителя ритма может встречаться у здоровых людей при повышении тонуса блуждающего нерва, а также у больных ИБС, рeвматическими пороками сердца, миокардитами, различными инфекционными заболеваниями. Нередко миграция водителя ритма встречается при синдроме слабости синусового узла (СССУ).
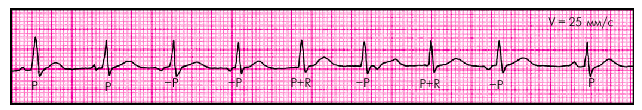
ЭКГ-признаки(рис. 3.28):
1. Постепенное, от цикла к циклу, изменение формы и полярности зубца Р.
2. Изменение продолжительности интервала P–Q(R) в зависимости от локализации водителя ритма.
3. Нерезко выраженные колебания продолжительности интервалов R–R (P–P).
|
| Рис. 3.28. ЭКГ больного с миграцией суправентрикулярного водителя ритма |
Наджелудочковая (суправентрикулярная) экстрасистолия
Экстрасистолия (ЭС) —это преждевременное возбуждение всего сердца или какого-либо его отдела, вызванное внеочередным импульсом, исходящим из предсердий, АВ-соединения или желудочков. Причины экстрасистолии разнообразны. Различают ЭС функционального, органического и токсического характера.
ЭС функционального (дисрегуляторного) характера возникают в результате вегетативной реакции на эмоциональное напряжение, курение, злоупотребление кофе, алкоголем, у больных НЦД или даже у здоровых лиц.
ЭС органического происхождения — это, как правило, результат глубоких морфологических изменений в сердечной мышце в виде очагов некроза, дистрофии, кардиосклероза или метаболических нарушений (ИБС, острый ИМ, “гипертоническое сердце”, миокардит, кардиомиопатии, застойная недостаточность кровообращения и др.).
ЭС токсического происхождения возникают при лихорадочных состояниях, дигиталисной интоксикации, при воздействии антиаритмических препаратов (проаритмический побочный эффект) и т.д.
Основными механизмами экстрасистолии являются: 1) повторный вход волны возбуждения (re-entry) в участках миокарда или проводящей системы сердца, отличающихся неодинаковой скоростью проведения импульса и развитием однонаправленной блокады проведения и 2) повышенная осцилляторная (триггерная) активность клеточных мембран отдельных участков предсердий, АВ-соединения или желудочков. Морфологическим субстратом ЭС (и некоторых других нарушений ритма) является электрическая негомогенность сердечной мышцы различного генеза.
Клиническая картина. Экстрасистолия далеко не всегда ощущается больными. В других случаях в момент возникновения ЭС появляется ощущение перебоев в работе сердца, “кувыркания”, “переворачивания сердца”. В некоторых случаях экстрасистолия воспринимается больными как “остановка” или “замирание” сердца, что соответствует длинной компенсаторной паузе, следующей за ЭС. Нередко после такого короткого периода “остановки” сердца больные ощущают сильный толчок в грудь, обусловленный первым после ЭС усиленным сокращением желудочков синусового происхождения. Увеличение ударного выброса (УО) в первом постэкстрасистолическом комплексе связано, в основном, с увеличением диастолического наполнения желудочков во время длинной компенсаторной паузы (увеличение преднагрузки).
При физикальном обследовании обычно легко устанавливают факт преждевременного сокращения сердца. При исследовании артериального пульса экстрасистоле соответствуют преждевременно возникающие пульсовые волны небольшой амплитуды, что указывает на недостаточное диастолическое наполнение желудочков во время короткого предэкстрасистолического периода. Пульсовые волны, соответствующие первому постэкстрасистолическому желудочковому комплексу, возникающему после продолжительной компенсаторной паузы, обычно имеют большую амплитуду (рис. 3.29).
Сходные данные получают при аускультации сердца. Во время экстрасистолического сокращения выслушиваются несколько ослабленные преждевременные I и II (или только один) экстрасистолические тоны, а после них — громкие I и II тоны сердца, соответствующие первому постэкстрасистолическому желудочковому комплексу (рис. 3.29).
При клиническом обследовании важно составить хотя бы ориентировочное представление об этиологии экстрасистолии (функциональные, органические или токсические ЭС).
| Рис. 3.29. Изменение артериального пульса и тонов сердца при экстрасистолии. СФ — сфигмограмма сонной артерии. Стрелками показан экстрасистолический комплекс (ЭС) | 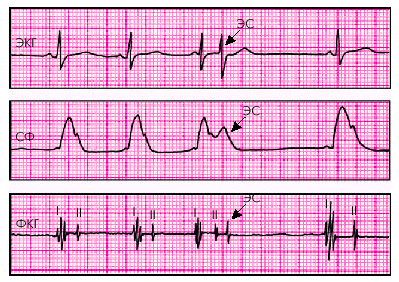
|
 Запомните
Для пациентов с функциональной, в частности нейрогенной, природой ЭС характерны следующие признаки (А.П.Мешков): отсутствие явной органической патологии сердца; наличие невротической симптоматики (психоэмоциональная лабильность, повышенная раздражительность и т.п.); связь ЭС с нервным напряжением; клинические признаки дисфункции вегетативной нервной системы; функциональные ЭС нередко исчезают во время физической нагрузки. Запомните
Для пациентов с функциональной, в частности нейрогенной, природой ЭС характерны следующие признаки (А.П.Мешков): отсутствие явной органической патологии сердца; наличие невротической симптоматики (психоэмоциональная лабильность, повышенная раздражительность и т.п.); связь ЭС с нервным напряжением; клинические признаки дисфункции вегетативной нервной системы; функциональные ЭС нередко исчезают во время физической нагрузки.
|
Более серьезное прогностическое значение имеет органическая экстрасистолия, развивающаяся у больных острым ИМ, миокардитом, кардиомиопатией, хронической СН, АГ и др. По сути прогноз экстрасистолии в большей степени зависит от наличия или отсутствия органического заболевания сердца и его тяжести, чем от характеристик самих ЭС.
Общие ЭКГ-признакиЭС:Основным электрокардиографическим признаком ЭС является преждевременность возникновения желудочкового комплекса QRST и/или зубца Р (рис. 3.30).
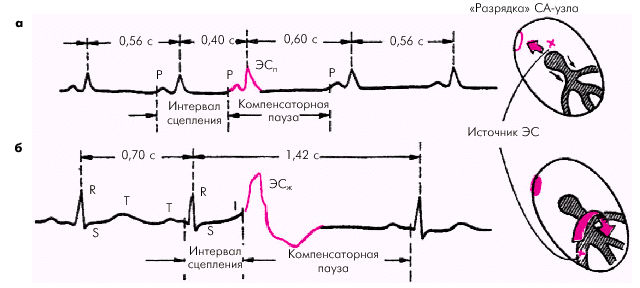
Интервал сцепления — это расстояние от предшествующего ЭС очередного цикла P–QRST основного ритма до ЭС.
|
| Рис. 3.30. Измерение интервала сцепления и длительности компенсаторной паузы при а — предсердной и б — желудочковой экстрасистолии |
Компенсаторная пауза —расстояние от ЭС до следующего за ней цикла P–QRST основного ритма. Неполная компенсаторная пауза — пауза, возникающая после предсердной ЭС или ЭС из АВ-соединения, длительность которой чуть больше обычного интервала P–P (R–R) основного ритма. Неполная компенсаторная пауза включает время, необходимое для того, чтобы эктопический импульс достиг СА-узла и “разрядил”его, а также время, которое требуется для подготовки в нем очередного синусового импульса. Полная компенсаторная пауза — пауза, возникающая после желудочковой ЭС, причем расстояние между двумя синусовыми комплексами P–QRST (предэкстрасистолическим и постэкстрасистолическим) равно удвоенному интервалу R–R основного ритма.
Аллоритмия —это правильное чередование экстрасистол и нормальных сокращений: 1) бигеминия (после каждого нормального сокращения следует ЭС); 2) тригеминия (ЭС следует после каждых двух нормальных сокращений); 3) квадригимения и др. Монотопные ЭС —экстрасистолы, исходящие из одного эктопического источника. Политопные ЭС —экстрасистолы, исходящие из разных эктопических очагов. Групповая (залповая) экстрасистолия —наличие на ЭКГ трех и более экстрасистол подряд.
Предсердная экстрасистолия
Предсердная экстрасистолия — это преждевременное возбуждение сердца под действием внеочередного импульса из предсердий.
ЭКГ-признаки(рис. 3.31):
1. Преждевременное внеочередное появление зубца P' и следующего за ним комплекса QRST'.
2. Деформация или изменение полярности зубца Р' экстрасистолы.
3. Наличие неизмененного экстрасистолического желудочкового комплекса QRST', похожего по форме на обычные нормальные комплексы QRST синусового происхождения (за исключением случаев аберрации комплекса QRS — см. ниже).
4. Наличие неполной компенсаторной паузы.
При ЭС из верхних отделов предсердий зубец Р' мало отличается от нормы. При ЭС из средних отделов — зубец Р' деформирован, а при ЭС из нижних отделов —отрицательный.
Блокированные предсердные экстрасистолы — это ЭС, исходяшие из предсердий, которые представлены на ЭКГ только зубцом Р', после которого отсутствует экстрасистолический желудочковый комплекс QRST' (рис. 3.32).
Предсердные ЭС нередко встречаются у здоровых людей и сами по себе еще не свидетельствуют о наличии болезни сердца. В то же время органические предсердные ЭС, возникающие у больных ИБС, острым ИМ, АГ на фоне выраженных морфологических изменений в предсердиях могут явиться предвестниками пароксизма фибрилляции предсердий или суправентрикулярной тахикардии.
Экстрасистолы из АВ-соединения
Эктопический импульс, возникающий в АВ-соединении, распространяется в двух направлениях: сверху вниз по проводящей системе желудочков и снизу вверх (ретроградно) по предсердиям (рис. 3.33).
ЭКГ-признаки:
1. Преждевременное внеочередное появление на ЭКГ неизмененного желудочкового комплекса QRS', похожего по форме на остальные комплексы QRS синусового происхождения (кроме случаев аберрации комплекса).
2. Отрицательный зубец Р' в отведениях II, III и aVF после экстрасистолического комплекса QRS' или отсутствие зубца Р' (за счет слияния P' и QRS').
3. Наличие неполной компенсаторной паузы.
Если эктопический импульс быстрее достигает желудочков, чем предсердий, отрицательный зубец Р' располагается после экстрасистолического комплекса P–QRST. Если предсердия и желудочки возбуждаются одновременно, зубец Р' сливается с комплексом QRS' и не выявляется на ЭКГ.
| Рис. 3.31. Предсердная экстрасистола (ЭС) | 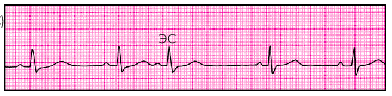
|
| Рис. 3.32. Блокированная предсердная экстрасистола (ЭС бл ) | 
|
| Рис. 3.33. Экстрасистолы из АВ-соединения с одновременным возбуждением предсердий и желудочков (а) и более ранним возбуждением желудочков (б) | 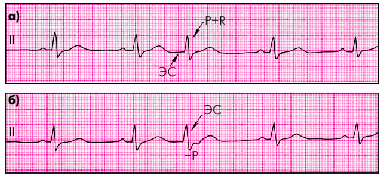
|
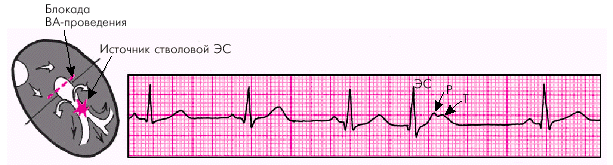
Своеобразной разновидностью ЭС из АВ-соединения с предшествующим возбуждением желудочков являются стволовые ЭС. Они отличаются возникновением полной блокады ретроградного ВА-проведения экстрасистолического импульса к предсердиям. Поэтому на ЭКГ регистрируется узкий экстрасистолический комплекс QRS, после которого отсутствует отрицательный зубец Р. Вместо него фиксируется положительный зубец Р. Это очередной пердсердный зубец Р синусового происхождения, который приходится обычно на сегмент RS–Т или зубец Т экстрасистолического комплекса (рис. 3.34).
Следует помнить, что иногда при предсердных и атриовентрикулярных ЭС желудочковый комплекс QRS может приобретать так называемую аберрантную форму за счет возникновения функциональной блокады правой ножки пучка Гиса или других его ветвей (рис. 3.35). При этом экстрасистолический комплекс QRS становится широким, расщепленным и деформированным, напоминающим комплекс QRS при блокадах ножек пучка Гиса или желудочковой ЭС. Отличия аберрантных суправентрикулярных ЭС от ЭС желудочковых описаны ниже.
|
| Рис. 3.34. Стволовая экстрасистола (ЭС). После экстрасистолического комплекса QRS заметен положительный зубец Р, наслаивающийся на зубец Т; имеется полная компенсаторная пауза |
| Рис. 3.35. Нижнепредсердная экстрасистола (ЭС) с аберрантной формой комплекса QRS, обусловленной преходящей блокадой правой ножки пучка Гиса. Экстрасистолический комплекс QRS расширен, перед ним в отведении III определяется отрицательный зубец Р. Компенсаторная пауза неполная | 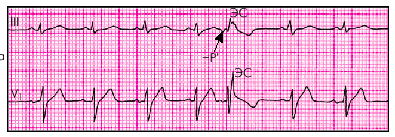
|
Синдромы преждевременного возбуждения желудочков
Термином синдром (феномен) преждевременного возбуждения желудочков обозначают аномальное распространение возбуждения от предсердий к желудочкам по так называемым дополнительным путям проведения, которые в большинстве случаев частично или полностью шунтируют АВ-узел. В результате часть миокарда желудочков или весь миокард начинают возбуждаться раньше, чем это наблюдается при обычном распространении возбуждения по АВ-узлу, пучку Гиса и его ветвям.
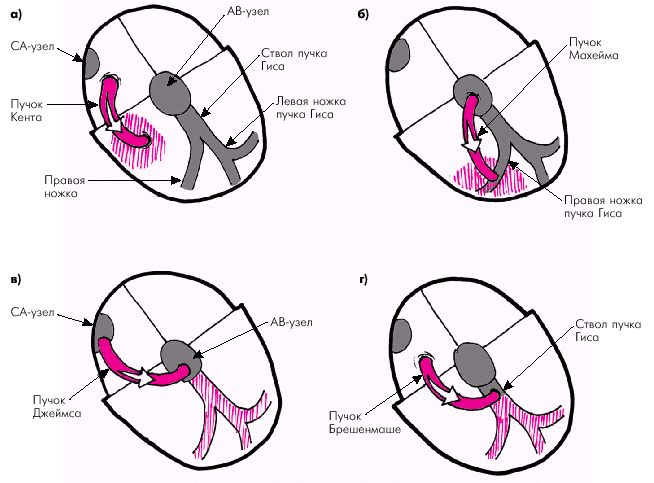
В настоящее время известны несколько дополнительных (аномальных) путей АВ-проведения (рис. 3.36).
1. Пучки Кента, связывающие предсердия и миокард желудочков (рис. 3.36, а).
2. Пучки Махейма, соединяющие АВ-узел с правой стороной МЖП или разветвлениями правой ножки пучка Гиса (рис. 3.36, б).
3. Пучки Джеймса, соединяющие СА-узел с нижней частью АВ-узла (рис. 3.36, в).
4. Пучок Брешенмаше, связывающий ПП с общим стволом пучка Гиса (рис. 3.36, г).
В настоящее время известны и другие аномальные пути проведения, в том числе так называемые скрытые пучки Кента, способные проводить электрический импульс ретроградно от желудочков к предсердиям.
Наличие дополнительных (аномальных) путей приводит к нарушению последовательности деполяризации желудочков. Однако основное клиническое значение дополнительных путей проведения состоит в том, что они нередко включаются в петлю кругового движения волны возбуждения (re-entry) и способствуют, таким образом, возникновению наджелудочковых пароксизмальных тахикардий (см. ниже).
По рекомендации группы экспертов ВОЗ (1980) преждевременное возбуждение желудочков, не сопровождающееся возникновением пароксизмальной тахикардии, называют “феноменом предвозбуждения”, а случаи, когда имеются не только ЭКГ-признаки предвозбуждения, но и развиваются пароксизмы наджелудочковой тахикардии — “синдромом предвозбуждения”.
В клинической практике наиболее часто встречаются 2 синдрома (феномена) предвозбуждения:
· синдром (феномен) WPW, названный так по имени исследователей, описавших клинико-электрокардиографическую картину предсердно-желудочковых дополнительных путей (L. Wolff, J. Parkinson, P. White, 1930);
· синдром (феномен) укороченного интервала Р–Q(R) или синдром СLС.
|
| Рис. 3.36. Дополнительные (аномальные) пути АВ-проведения: а — пучок Кента; б — пучок Махейма; в — пучок Джеймса; г — пучок Брешенмаше. Объяснение в тексте |
Синдром (феномен) WPW
Синдром WPW — это комплекс ЭКГ-изменений, обусловленных наличием дополнительных аномальных путей проведения электрического импульса от предсердий к желудочкам (пучков Кента). Синдром WPW является врожденной аномалией, но клинически может проявиться в любом возрасте, спонтанно или после какого-либо заболевания.
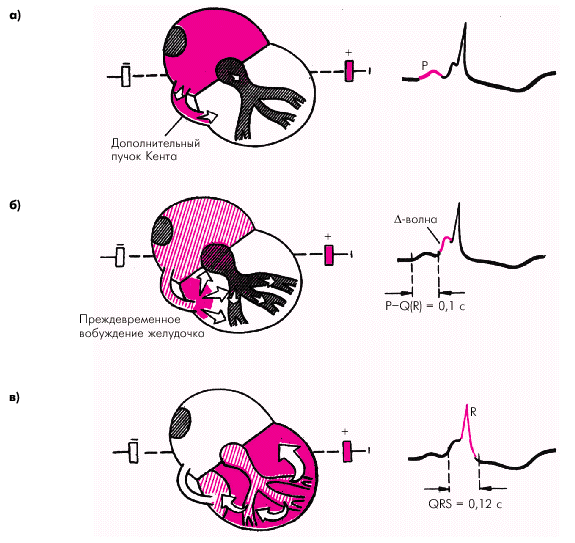
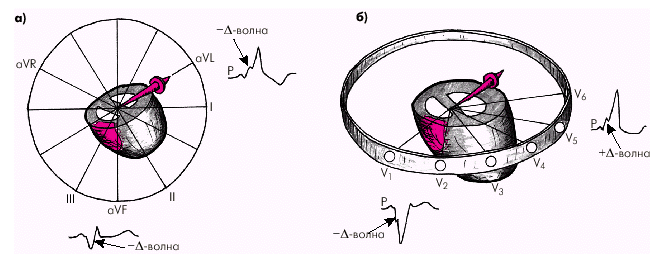
Синдром WPW характеризуется наличием в сердце двух (или больше) независимых путей предсердно-желудочкового проведения, причем по дополнительному пути электрический импульс распространяется быстрее, чем по АВ-узлу и системе Гиса–Пуркинье. Поэтому почти сразу после деполяризации предсердий электрический импульс проводится по аномальному пучку Кента и вызывает активацию части миокарда одного из желудочков (рис. 3.37). Остальные участки желудочков возбуждаются за счет импульса, распространяющегося по обычному пути (по АВ-узлу, пучку Гиса и его ветвям). Комплекс QRS при этом приобретает характер сливного комплекса: начальная D-волна отражает возбуждение миокарда, обусловленное импульсом, пришедшим по дополнительному (аномальному) пучку, а основная часть QRS — по обычному пути. Описанная последовательность возбуждения желудочков определяет три главных электрокардиографических признака синдрома WPW.
|
| Рис. 3.37. Формирование ЭКГ при синдроме WPW. Возбуждение по дополнительному пучку Кента проводится к желудочкам быстрее, чем по АВ-узлу, образуя дополнительную волну деполяризации базальных отделов желудочков — .-волну. Интервал P–Q(R) укорочен, а длительность QRS увеличена. В данном примере P–Q(R) составляет 0,1 с; QRS (вместе с .-волной) 0,15 с. а, б, в — последовательные этапы распространения волны возбуждения по дополнительному пучку Кента и желудочкам. Объяснение в тексте |
ЭКГ-признаки синдрома WPW:
1. Интервал P–Q(R) меньше 0,12 с.
2. Комплекс QRS сливной, в его составе имеется дополнительная волна возбуждения — D-волна.
3. Имеется увеличение продолжительности и деформация комплекса QRSТ.
Определение локализации дополнительного пути при синдроме WPW. В связи с распространением в последние годы хирургических методов лечения больных с синдромом WPW (деструкция аномального пучка) постоянно совершенствуются способы точного определения его локализации. Наиболее эффективными являются методы внутрисердечного ЭФИ, в частности эндокардиальное (предопреационное) и эпикардиальное (интраоперационное) картирование. При этом с помощью сложной методики определяют область наиболее ранней активации (предвозбуждения) миокарда желудочков, которая соответствует локализации дополнительного (аномального) пучка.
В последние годы с этой целью применяют методику поверхностного многополюсного ЭКГ-картирования сердца, которая в 70–80% случаев также позволяет ориентировочно определить местоположение пучков Кента (И.И. Полякова, Е.З. Голухова, А.В. Струтынский). Это существенно сокращает время интраоперационного выявления дополнительных (аномальных) пучков.
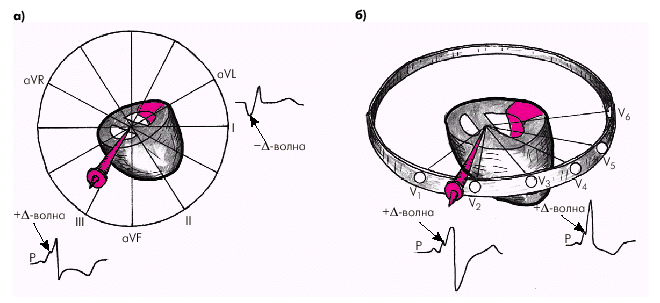
На ЭКГ12 местоположение пучка Кента обычно определяют по направлению начального моментного вектора деполяризации желудочков (0,02–0,04 с), который соответствует времени формирования аномальной D-волны. В тех отведениях, активные электроды которых располагаются непосредственно над участком миокарда, возбуждающимся аномально, за счет пучка Кента, регистрируется отрицательная D-волна. Это указывает на распространение раннего аномального возбуждения в сторону от активного электрода данного отведения. Например, если пучок Кента локализуется в заднебазальных отделах ЛЖ, вектор преждевременного возбуждения этого участка миокарда направлен вперед, вниз и несколько вправо, т.е. в сторону от отведения I, в котором формируется отрицательная D-волна, иногда имитирующая увеличенный зубец Q (рис. 3.38).
|
| Рис. 3.38. Схема, поясняющая образование отрицательной и положительной -волн при синдроме WPW (тип А): а — фронтальная плоскость; б — горизонтальная плоскость. Заднебазальная область ЛЖ, возбуждающаяся первой, обозначена красным цветом. Стрелки соответствуют направлению начального моментного вектора деполяризации желудочков (0,04 с) |
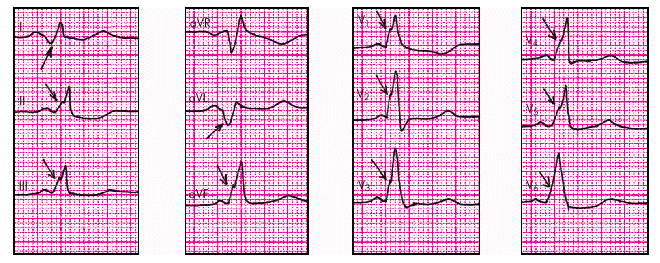
В отведениях III, аVF, V1–6 регистрируется положительная D-волна, поскольку ее вектор направлен в сторону активных электродов этих отведений. Это так называемый тип А синдрома WPW (рис. 3.39).
|
| Рис. 3.39. Электрокардиограмма при синдроме WPW (тип А). Стрелками показаны отрицательные и положительные дельта -волны |
При локализации пучка Кента в боковой стенке ПЖ вектор Δ-волны направлен влево, вниз и несколько кзади, в сторону от активных электродов отведений III, аVF и правых грудных отведений, где регистрируется отрицательная Δ-волна. Наоборот, в отведениях I, аVL, V4–6, в сторону активных электродов которых направлен вектор аномальной деполяризации (предвозбуждения) желудочков, фиксируется положительная Δ-волна (рис. 3.40). Это так называемый тип В синдрома WPW (рис. 3.41).
Таблица 3.5
Полярность Δ-волны в зависимости от локализации пучка Кента
| Пучки Кента | 12 электрокардиографических отведений | |||||||||||
| I | II | III | аVR | аVL | аVF | V1 | V2 | V3 | V4 | V5 | V6 | |
| + | + | +(±) | – | ±(+) | + | ± | ± | +(±) | + | + | + | |
| + | + | –(±) | – | +(±) | ±(–) | ± | +(±) | +(±) | + | + | + | |
| + | ±(–) | – | – | + | –(±) | ± | ± | ± | + | + | + | |
| + | – | – | – | + | – | ±(+) | ± | + | + | + | + | |
| + | – | – | –(+) | + | – | ± | + | + | + | + | + | |
| + | – | – | – | + | – | + | + | + | + | + | + | |
| + | – | – | ±(+) | + | – | + | + | + | + | + | –(±) | |
| –(±) | ± | ± | ±(+) | –(±) | ± | + | + | + | + | –(±) | –(±) | |
| –(±) | + | + | – | –(±) | + | + | + | + | + | + | + | |
| + | + | +(±) | – | ± | + | ±(+) | + | + | + | + | + |
Примечание: (+) — положительные значения начальных 40 мс Δ-волны; (–) — отрицательные значения; (±) — значения изоэлектричны.
На рис. 3.42 и в таблице 3.5 можно найти сведения по более точному определению локализации дополнительного пучка на основании определения полярности Δ-волны (по J. Gallagher с соавт., 1978).
|
| Рис. 3.40. Схема, поясняющая образование отрицательной и положительной дельта -волн при синдроме WPW (тип В). Обозначения те же, что и на рис. 3.38 |
| Рис. 3.41. ЭКГ при синдроме WPW | 
|
| Рис. 3.42. Десять локализаций дополнительных (аномальных) пучков Кента (по J. Gallagher с соавт., 1978). 1 — правый передний парасептальный пучок; 2 — правый передний; 3 — правый боковой; 4 — правый задний; 5 — правый парасептальный; 6 — левый задний парасептальный; 7 — левый задний; 8 — левый боковой; 9 — левый передний; 10 — левый передний парасептальный | 
|
Синдром укороченного интервала Р–Q(R) [синдром CLC]
Синдром CLC (Клерка–Леви–Кристеско) обусловлен наличием дополнительного аномального пути проведения электрического импульса (пучка Джеймса) между предсердиями и пучком Гиса. Иногда этот синдром называют синдромом LGL (Лауна–Ганонга–Левине). Дополнительный пучок Джеймса как бы шунтирует АВ-узел, поэтому волна возбуждения, минуя последний, быстро, без нормальной физиологической задержки, распространяется по желудочкам и вызывает их ускоренную активацию (рис. 3.43). Синдром CLC также является врожденной аномалией. У больных с этим синдромом имеется повышенная склонность к возникновению пароксизмальных тахиаритмий.
| Рис. 3.43. Формирование ЭКГ при синдроме укороченного интервала Р–Q(R): а — возбуждение предсердий (зубец Р) и пучка Джеймса; б — возбуждение ситемы Гиса–Пуркинье и миокарда желудочков (без нормальной АВ-задержки) | 
|
ЭКГ-признаки (рис. 3.44):
1. Укорочение интервала P–Q(R), продолжительность которого не превышает 0,11 с.
2. Отсутствие в составе комплекса QRS дополнительной волны возбуждения — D-волны.
3. Наличие неизмененных (узких) и недеформированных комплексов QRS (за исключением случаев сопутствующей блокады ножек и ветвей пучка Гиса).
| Рис. 3.44. ЭКГ при синдроме укороченого интервала P–Q(R) (синдроме CLC) | 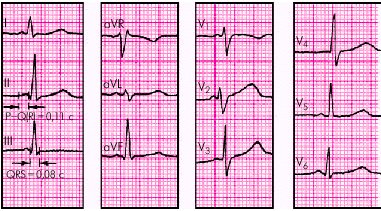
|
Пароксизмальные наджелудочковые (суправентрикулярные) тахикардии
Пароксизмальная тахикардия (ПТ) — это внезапно начинающийся и так же внезапно заканчивающийся приступ учащения сердечных сокращений до 140–250 в минуту при сохранении в большинстве случаев правильного регулярного ритма.
Основными механизмами ПТ являются: 1) повторный вход и круговое движение волны возбуждения (re-entry) и 2) повышение автоматизма клеток проводящей системы сердца — эктопических центров II и III порядка. Оба механизма реализуются в условиях существования выраженной электрической негомогенности различных участков сердца и его проводящей системы. Причинами последней являются:
- органические локальные повреждения сердечной мышцы и проводящей системы сердца при остром ИМ, хронической ИБС, миокардитах, кардиопатиях, пороках сердца и других заболеваниях;
- дополнительные аномальные пути проведения (синдром WPW);
- выраженные вегетативно-гуморальные расстройства, например у больных НЦД;
- наличие висцеро-кардиальных рефлексов и механических воздействий (дополнительные хорды, пролапс митрального клапана, спайки и т.п.).
В зависимости от локализации эктопического центра повышенного автоматизма или постоянно циркулирующей волны возбуждения (re-entry) различают предсердную, атриовентрикулярную и желудочковую формы ПТ. Предсердные и атриовентрикулярные формы ПТ объединяются термином наджелудочковая (суправентрикулярная) пароксизмальная тахикардия.
Предсердная пароксизмальная тахикардия
Предсердная ПТ — относительно редкая форма ПТ; ее частота не превышает 10–15% от общего числа наджелудочковых ПТ. В зависимости от того, какова локализация аритмогенного очага и какой из перечисленных механизмов лежит в основе предсердной ПТ, различают:
· синоатриальную реципрокную ПТ, обусловленную механизмом re-entry в синоатриальной зоне, где ткань СА-узла переходит в миокард предсердий;
· реципрокную предсердную ПТ, также обусловленную механизмом re-entry, локализованном в миокарде предсердий;
· очаговые (фокусные) или эктопические предсердные ПТ, в основе которых лежит анормальный автоматизм предсердных волокон.
Причинами предсердных ПТ являются:
1. Органические заболевания сердца (ИБС, ИМ, легочное сердце, АГ, ревматические пороки сердца, пролапс митрального клапана, дефект межпредсердной перегородки и др.).
2. Дигиталисная интоксикация, гипокалиемия, сдвиги КЩС.
3. Рефлекторное раздражение при патологических изменениях в других внутренних органах (язвенная болезнь желудка и двенадцатиперстной кишки, желчнокаменная болезнь и др.), а также злоупотребление алкоголем, никотином и другие интоксикации. Предсердные ПТ, развивающиеся вследствие этих причин, часто называют идиопатической формой наджелудочковой ПТ, так как при этом в сердце обычно не обнаруживают органической патологии.
Клинические проявления зависят от частоты сердечных сокращений во время приступа, а также от характера и тяжести заболевания сердца. При синоатриальной форме предсердной ПТ, при которой ЧСС обычно не превышает 120–130 в мин (редко более 160 в мин), больные сравнительно легко переносят приступ тахикардии. В более тяжелых случаях, например при предсердной реципрокной или очаговой (фокусной) ПT с ЧСС до 170–180 в мин во время приступа появляется одышка, боль в области сердца и ощущение сердцебиений.
ЭКГ-признаки предсердныхПТ(рис. 3.45):
1. Внезапно начинающийся и так же внезапно заканчивающийся приступ учащения сердечных сокращений до 140–250 ударов в минуту при сохранении правильного ритма.
2. Наличие перед каждым желудочковым комплексом QRS' сниженного, деформированного, двухфазного или отрицательного зубца Р'.
3. Нормальные неизмененные желудочковые комплексы QRS', похожие на QRS, регистрировавшиеся до возникновения приступа ПТ.
4. В некоторых случаях (рис. 3.46) наблюдается ухудшение АВ-проводимости с развитием АВ-блокады I степени (удлинение интервала P–Q(R) более 0,02 с) или II степени с периодическими выпадениями отдельных комплексов QRS' (непостоянные признаки).
| Рис. 3.45. Предсердная пароксизмальная тахикардия. Зубцы Р наслаиваются на зубцы Т | 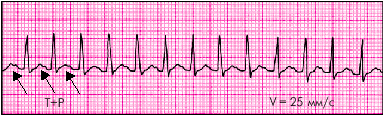
|
| Рис. 3.46. Предсердная пароксизмальная тахикардия с преходящей АВ-блокадой II степени и выпадением отдельных комплексов QRS | 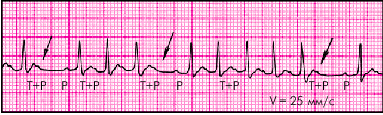
|
Следует добавить, что каждая из перечисленных форм предсердной ПТ имеет некоторые особенности. Так, при синоатриальной форме предсердной тахикардии ЧСС обычно не превышает 120–130 в мин, а зубцы Р практически не изменены (положительные Р в отведениях II, III и аVF). Для реципрокной тахикардии характерно острое внезапное начало и такое же внезапное прекращение пароксизма, а также некоторое удлинение интервала Р–Q(R), в связи с чем зубец Р часто накладывается на зубец Т предшествующего комплекса.
Для очаговой (фокусной) предсердной ПТ, обусловленной повышением автоматизма или триггерной активностью предсердий, характерно постепенное нарастание ЧСС (феномен “разогрева”) в начале приступа и постепенное уменьшение ЧСС — в конце. Для этой формы ПТ характерна также функциональная неустойчивость эктопического центра, что отражается на регулярности QRS и длительности интервала Р–Р.
Иногда в клинической практике встречается еще одна форма предсердной тахикардии — многофокусная (“хаотическая”) предсердная ПТ. Она характеризуется наличием нескольких очагов эктопической активности в предсердиях, что определяет некоторые особенности этой формы ПТ. При увеличении ЧСС до 100–250 в мин на ЭКГ выявляется неправильный ритм с разными интервалами Р–Р. Морфология зубцов Р и продолжительность интервала Р–Q(R) непрерывно изменяются (рис. 3.47). Наиболее частой причиной многофокусной предсердной ПТ является легочное сердце (см. главу 13).
Следует отметить, что в ряде случаев при любой форме предсердной ПТ желудочковый ритм становится нерегулярным за счет функциональной блокады АВ-соединения II степени, что ведет к периодическим выпадениям желудочкового комплекса QRS.
| Рис. 3.47. Многофокусная («хаотическая») предсердная пароксизмальная тахикардия. Имеются колебания продолжительности интервалов Р–Р, R–R (неправильный ритм), интервалов Р–Q(R) и изменение морфологии зубцов Р | 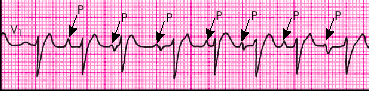
|
АВ-реципрокные (re-entry) пароксизмальные тахикардии
АВ-реципрокные ПТ обусловлены повторным входом волны возбуждения, возникающим в результате:
· продольной диссоциации АВ-узла (АВ-узловая реципрокная ПТ) или
· наличия внеузлового добавочного пути (пучков Кента, Джеймса или скрытых аномальных путей проведения).
АВ-реципрокные ПТ составляют около 85–90% всех наджелудочковых ПТ. Причинами этих форм ПТ являются ИБС, пролапс митрального клапана, синдром WPW, скрытые дополнительные (аномальные) пути АВ-проведения. Во всех случаях сохраняются три важнейших условия возникновения повторного входа волны возбуждения (см. выше):
- наличие двух путей проведения, отличающихся скоростью проведения электрического импульса и длительностью рефрактерных периодов;
- наличие однонаправленной антероградной блокады проведения по так называемому “быстрому” каналу;
- возможность ретроградного проведения импульса по “быстрому” каналу.
С практической точки зрения важно различать два варианта АВ-реципрокной ПТ:
1. ПТ с узкими комплексами QRS, к которой относятся:
- АВ-узловая реципрокная ПТ;
- ортодромная АВ-реципрокная (круговая) ПТ при синдроме WPW.
2. ПТ с широкими комплексами QRS, например антидромная АВ-реципрокная (круговая) ПТ при синдроме WPW.
Следует заметить, что существуют и другие, более редкие варианты АВ-реципрокной ПТ, которые подробно описываются в специальных руководствах по аритмологии.
АВ-узловая реципрокнаяПТ относится кчислу ПТ с узкими комплексами QRS. Она возникает при наличии анатомического или функционального расщепления АВ-узла, в котором существует 2 пути (канала) проведения (рис. 3.48): медленный a-канал и быстрый (b-канал). Последний отличается более продолжительным рефрактерным периодом и возможностью ретроградного проведения импульса.
| Рис. 3.48. Механизм АВ-реципрокной узловой пароксизмальной тахикардии. Стрелками обозначено круговое движение волны возбуждения в пределах АВ-узла (re-entry) | 
|
Во время нормального синусового ритма электрические импульсы проводятся от предсердий к пучку Гиса по быстрому b-каналу. При возникновении суправентрикулярной ЭС или при искусственной преждевременной стимуляции предсердий (чреспищеводная или эндокардиальная стимуляция) в тот момент, когда b-канал еще находится в рефрактерном состоянии, электрический импульс распространяется антероградно по медленному a-каналу, который уже восстановил свою возбудимость. Медленное проведение по a-каналу завершается после того, как быстрый b-канал вышел из состояния рефрактерности. Поэтому электрический импульс проводится по быстрому b-каналу в ретроградном направлении и замыкает, таким образом, круг re-entry. В дальнейшем возможно повторение этого процесса и возникновение пароксизма АВ-узловой тахикардии.
ЭКГ-признаки АВ-узловой реципрокной ПТ (рис. 3.49):
1. Внезапно начинающийся и так же внезапно заканчивающийся приступ учащения сердечных сокращений до 140–250 ударов в минуту при сохранении правильного ритма.
2. Отсутствие в отведениях II, III и aVF зубцов Р', которые сливаются с желудочковым комплексом QRS.
3. Нормальные неизмененные (неуширенные и недеформированные) желудочковые комплексы QRS', похожие на QRS, регистрировавшиеся до возникновения приступа ПТ
| Рис. 3.49. Пароксизмальная тахикардия из АВ-соединения с одновременным возбуждением предсердий и желудочков | 
|
Исключение составляют случаи аберрантного проведения импульса по системе Гиса– Пуркинье), которые возникают примерно у 8–10% больных во время приступа ПТ за счет функциональной блокады правой ножки пучка Гиса. В этих случаях аберрантные желудочковые комплексы QRS становятся похожими на таковые при желудочковой ПТ или блокаде ножки пучка Гиса.
При осмотре больных с АВ-узловой реципрокной ПТ в большистве случаев в момент возникновения пароксизма можно заметить усиленную пульсацию шейных вен, причем с той же частотой, что и сокращения желудочков (совпадение частоты венного и артериального пульса).
Ортодромная АВ-реципрокная (круговая)ПТпри синдромеWPW возникает при наличии дополнительных (аномальных) путей АВ-проведения. В этих случаях круг macro-re-entry, являющийся морфологическим субстратом ПТ, охватывает не только АВ-узел, но и пучок Гиса, одну из ножек пучка Гиса, волокна Пуркинье, миокард желудочков (антероградное проведение внеочередного импульса), а также дополнительный пучок Кента, по которому возбуждение ретроградно распространяется к предсердиям (рис. 3.50).
| Рис. 3.50. Механизм ортодромной АВ-реципрокной (круговой) пароксизмальной тахикардии при синдроме WPW. Объяснение в тексте | 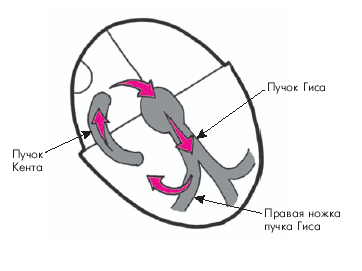
|
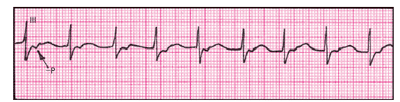
ЭКГ-признаки ортодромной АВ-реципрокной ПТ напоминают таковые, описанные ранее для АВ-узловой ПТ (рис. 3.51):
1. Внезапное начало пароксизма с быстрым установлением максимальной частоты сердечного ритма.
2. Сохранение на протяжении всего пароксизма устойчивого регулярного ритма с ЧСС в пределах 120–240 в мин.
3. Наличие в отведениях II, III и аVF отрицательных зубцов Р, располагающихся позади комплекса QRS, поскольку возбуждение, распространяющееся по большой петле re-entry, гораздо позже достигает предсердий, чем желудочков.
4. Наличие узких комплексов QRS, за исключением случаев, когда на фоне тахикардии возникает функциональная блокада одной из ножек пучка Гиса, и комплексы QRS становятся аберрантными.
5. Внезапное окончание пароксизма.
|
| Рис. 3.51. Электрокардиограмма при ортодромной АВ-реципрокной (круговой) пароксизмальной трахикардии при синдроме WPW. Отрицательные зубцы P следуют за узкими комплексами QRS |
Диагностика этого вида ПТ значительно облегчается, если у больного ранее (хотя бы раз в жизни) регистрировался синдром WPW (анамнестические данные).
Антидромная АВ-реципрокная (круговая)ПТпри синдромеWPW относится к числу ПТ с широкими комплексами QRS. У больных с синдромом предвозбуждения желудочков она встречается гораздо реже, чем ортодромная АВ-узловая ПТ. Этот вариант ПТ обычно провоцируется предсердной ЭС, которая блокируется в АВ-узле и распространяется к желудочкам через дополнительный (аномальный) путь проведения, имеющий более короткий рефрактерный период (рис. 3.52). При этом на ЭКГ регистрируются широкие сливные комплексы QRS с наличием типичной для синдрома WPW D-волны (рис. 3.53). Позади комплекса QRS можно заметить (не всегда) отрицательные зубцы Р, отражающие ретроградное возбуждение предсердий. ЧСС во время пароксизма обычно достигает 170–250 в мин.
| Рис. 3.52. Механизм антидромной АВ-реципрокной (круговой) пароксизмальной трахикардии при синдроме WPW. Объяснение в тексте | 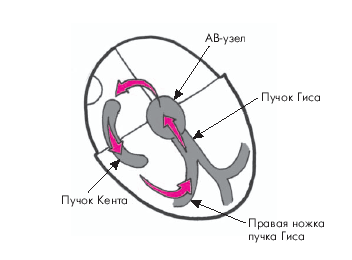
|

|
| Рис. 3.53. Электрокардиограмма при антидромной АВ-реципрокной (круговой) пароксизмальной трахикардии при синдроме WPW. Отрицательные зубцы P расположены позади широких (сливных) комплексов QRS |
Очаговые (фокусные) ПТ из АВ-соединения
Очаговые (фокусные) ПТ, обусловленные усилением автоматизма эктопического очага, расположенного в АВ-соединении или в стволе пучка Гиса, в клинической практике встречаются гораздо реже, чем АВ-реципрокные (re-entry) ПТ. Их чаще выявляют у новорожденных и детей первых 2–3 лет жизни. На ЭКГ при этом определяют узкие комплексы QRS, позади которых регистрируют отрицательные зубцы Р. ЧСС обычно достигает 120–160 в мин, а у новорожденных — 220–300 в мин. В отличие от АВ-реципрокной (re-entry) ПТ приступы очаговых (фокусных) тахикардий, обусловленных повышенным автоматизмом эктопического очага, устойчивы к сверхчастой и программированной электрической стимуляции. При инвазивном ЭФИ у этих больных обнаруживают и
Дата добавления: 2016-01-20; просмотров: 2100;
