Некоторые указания по выполнению аналитических операций и их важнейшие характеристики
Способы и правила выполнения отдельных аналитических операций описаны в ряде руководств по аналитической химии. Ниже приводятся сведения о некоторых наиболее важных моментах анализа, почерпнутые из вышеуказанных учебной литературы, а также [12].
Необходимость в химическом анализе возникает при решении или интерпретации (объяснении) проблем, связанных с надежными измерениями, поэтому первая ступень химического анализа – это определение цели. Проблема может заключаться, например, в контроле производственного процесса, в опустошениях, наносимых непарным шелкопрядом, во фторировании водопроводной воды, в регуляции подачи машинного масла в мотор. Если хотя бы часть проблемы решается с помощью анализа, то это должен сознавать каждый независимо от того, химик он или нет. После адекватного (правильного) определения аналитических аспектов проблемы им можно дать оценку с позиций аналитической химии.
Чтобы решать аналитические проблемы, химик должен быть достаточно подготовленным, уметь пользоваться всем арсеналом химических знаний и приборами. Нужно владеть не только методами измерений химических и физических свойств атомов, ионов и молекул, но также и современными методами разделения, отбора проб, обработки статистических данных. Одной из привлекательных сторон аналитической химии является ее необычайно широкое поле деятельности, от испытанных временем методов осаждения и титрования до сложных современных теорий, инструментальных методов и технологии. Недостаточные знания любого аспекта аналитической химии сделают невозможным решение возникающих задач.
Рассмотрим последовательно эти аспекты.
Отбор пробы. Практическая ценность результатов анализа прежде всего зависит от правильности отбора средней пробы, в особенности если анализируется неоднородное вещество: какой-нибудь сплав, отход, горная порода, технический материал. Обратим внимание на то, что, пользуясь малыми навесками (2—4 мг), нужно так тонко измельчать анализируемое вещество, чтобы размер частиц не превышал 0,02 мм. Анализируемая проба должна полноценно представлять собой состав интересующего материала. Отбор проб – это сложная проблема, лишь частично поддающаяся теоретическому описанию. Поскольку по самой своей природе операция отбора проб требует статистической обработки, здесь, как и в последующем анализе необходимо правильное понимание аспектов статистики.
Пробоподготовка. Другой важной стадией анализа во многих случаях является вышеназванное разделение. Если разделения не требуется в связи с выбранным методом или в связи с природой вещества, то задача значительно упрощается. Например, при титровании этилендиаминтетрауксусной кислоты (ЭДТА) разделения можно избежать благодаря применению маскирующего агента, связывающего в комплекс мешающие ионы металлов. Если разделение необходимо, есть возможность выбора из нескольких методов. В общих чертах, разделение заключается в образовании двух физически отделенных фаз, одна из которых содержит целевое вещество, а другая – мешающее. Любая из этих фаз может быть газообразной, жидкой или твердой. Таким образом, возможны шесть основных типов процессов разделения. После того как разделение и другие операции пробоподготовки (концентрирование, маскировка примеси, стабилизация пробы и т.д.) выполнено, можно приступать к количественному определению соответствующими методами.
Выбор метода анализа. О квалификации химика-аналитика можно судить по его умению критически выбирать методы анализа. Аналитику необходимо знание всех аспектов (и направлений) современной аналитической химии. При исследованиях, связанных со многими отраслями наук, очень важны рекомендации химика-аналитика относительно выбора наилучших методов измерений. Рекомендация должна быть основана на глубоком знании всех существующих методов и на умении применить их для специальных целей. Это имеет решающее значение для квалифицированного выполнения анализа.
При выборе метода анализа следует исходить из требуемой в данном случае чувствительности, точности и производительности определений. Наметив подходящие по чувствительности методы, следует, конечно, отдать предпочтение более простым, не требующим сложного оборудования и при прочих равных условиях более производительным методам.
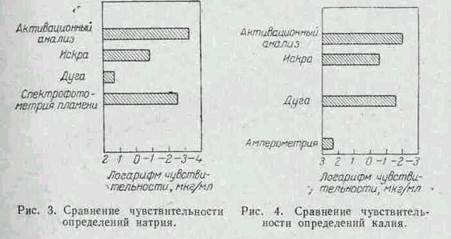
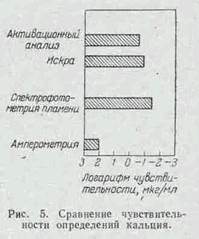
Рассмотрим в качестве примера графики, на которых сравнивается чувствительность определения ряда элементов несколькими методами.
Нетрудно заключить, что следы цинка и кадмия (рис. 1 и 2) следует определить при помощи химических реакций, следы натрия, кальция (рис. 3 и 5) – методом спектрофотометрии пламени, а следы калия (рис. 4) – в пламени дуги.

Метод же активационного анализа, несмотря на его более высокую чувствительность, в подобных случаях применять нецелесообразно, так как для использования этого метода необходимо сложное и дорогое оборудование – атомный реактор.
Обратим внимание на то, что при определении основного элемента в чистых веществах точность определения высока, она, например, составляет 0,01%. При анализе же примесей, например серы и фосфора в сталях, точность определений понижается до +10% (относительных). Следует иметь в виду, что чем меньше концентрация определяемого элемента, тем чувствительнее должен быть метод анализа. На практике при особо высоких требованиях к чувствительности требования к точности определений могут быть сильно снижены. Так, при определении примесей в предельно чистых веществах, т. е. содержащих минимально возможное количество посторонних элементов, допускается относительная ошибка до 100%, а иногда больше. Таким образом, определяется только порядок концентрации примесей, что в таких случаях достаточно для контроля производства.
Для выполнения массовых однородных определений следует выбирать метод, допускающий автоматизацию определений. Но если предстоит выполнять только единичные определения, нет смысла останавливаться на автоматических анализаторах.
Вообще выбор нужного метода анализа не труден, если имеется хотя бы небольшой опыт использования различных методов анализа. Именно для приобретения некоторого опыта студентам и предлагается выполнить ряд лабораторных работ.
Точность результатов анализа. Нужно иметь в виду, что при тщательном выполнении повторных аналитических определений каким-либо общепринятым методом должна наблюдаться хорошая воспроизводимость результатов анализа.
Если же при выполнении одинаковых определений не удается каждый раз получать достаточно близкие друг к другу результаты, то это указывает на какую-то систематическую ошибку, допущенную при выполнении аналитических операций или вследствие несоблюдения условий определения (см. ниже). Причиной неточности результатов анализа часто бывают посторонние вещества, присутствие которых не предусмотрено ходом анализа, или неточное соблюдение условий нагревания, охлаждения, перемешивания и т. п.
Анализируя в учебной лаборатории смеси чистых веществ, конечно, нетрудно добиться хорошей воспроизводимости результатов анализа. Анализ различных технических продуктов и природных веществ, представляющих собой иной раз неожиданные смеси элементов при самых различных их соотношениях, – дело более трудное, требующее, кроме специальных знаний и навыков, также творческого, исследовательского подхода. В этом случае единственным основанием для уверенности в результатах анализа может быть проверка их точности при анализе ряда образцов анализируемого вещества. Не следует никогда ограничиваться единичными определениями, если можно получить ряд проб анализируемого вещества. Во всех случаях необходимо определять точность результатов анализа. Методы обработки результатов аналитических определений указаны в специальных руководствах.
Знания статистики необходимы для выполнения последней стадии аналитической работы – оценки и представления данных. Даже теперь многие аналитики не выходят за пределы вычисления стандартного отклонения ряда повторных определений. Многие ошибочно полагают, что для применения более прогрессивных статистических методов требуется получение колоссального числа данных. При этом часто не учитывают того, что относительно небольшое число правильно запланированных наблюдений может дать значительно более ценную информацию, чем большое число повторных идентичных наблюдений. Например, вместо трехкратного проведения анализа пробы лучше взять три пробы разного размера. Результаты могут вскрыть ошибку определения, которая осталась бы незамеченной в случае анализа одинаковых по размеру проб.
Предосторожности при приготовлении растворов. При приготовлении эталонов и стандартных растворов нужно иметь в виду, что на стекле могут происходить обменные процессы, в результате которых очень малые количества элементов могут полностью исчезнуть из раствора, а вместо них появятся ионы натрия, кремневая кислота и другие примеси, перешедшие из стекла. Такое же явление может происходить и при выпаривании очень разбавленных нейтральных растворов. Поэтому для длительного хранения следует приготовлять более концентрированные растворы и обязательно их подкислять. Следует выпаривать также кислые растворы. Если возможно, надо пользоваться посудой не из стекла, а из полиэтилена, фторопласта и других химически инертных материалов.
При анализе любая из операций может оказаться очень важной. Общей целью анализа является быстрое получение данных при возможно меньших затратах. Если проба имеется в достаточном количестве и нет никаких помех, то анализ не представляет значительных трудностей, и зачастую можно переходить от отбора пробы непосредственно к измерению.
В случае сложных смесей близких по свойствам веществ можно рекомендовать два пути. Первый заключается в использовании специфичного метода измерения; этот способ позволяет зачастую обойтись без стадии разделения. Другой путь – отделить нужные вещества и потом уже измерить каждое в отдельности простым методом. В случае сложной пробы может оказаться необходимым предварительное разделение ее на классы соединений и определение последних специфичными методами.
Рассмотрев самые общие подходы а аналитической химии и ее важнейшему разделу – физико-химическим (и другим) методам анализа, мы убедились, что для правильного понимания процессов и применения соответствующих методов, прежде необходимо усвоить несколько десятков важнейших терминов, многие из которых приведены в справочном издании [13].
Контрольные вопросы (для самоподготовки):
1. На какие крупнейшие группы подразделяются методы анализа (в химии) ?
2. Почему сегодня название «физико-химические методы анализа» условно ?
3. Каков универсальный принцип определения химического состава (поясните, как он действует) ?
4. Что такое «химический анализ» и какое значение он имеет для изучения окружающей среды ?
5. Какие вы знаете методы анализа и какие из них относятся к наиболее распространенным ?
6. Перечислите важнейшие области применения физических и физико-химических методов анализа ?
7. В каких областях деятельности очень важна высокая чувствительность аналитических методов и на каком уровне (доли процента) она должна быть ?
8. Для чего сегодня нужны и широко применяются химические методы, а также в чем заключается их преимущество ?
9. В каких случаях приходится применять разделение веществ и для чего ?
10. В каких случаях прибегают к обогащению (концентрированию) пробы и во сколько раз ?
11. Перечислите важнейшие методы концентрирования (разделения) пробы.
12. От чего прежде всего зависит ценность (правильность) результата и без чего он вообще не может быть получен ?
13. Что такое пробоподготовка и для чего она нужна ?
14. Из чего должен исходить аналитик, выбирая подходящий метод анализа ?
15. С увеличением чувствительности анализа его точность растет или падает и почему ?
16. Что такое воспроизводимость анализа и чем она отличается от точности и его правильности ?
17. Чем завершается любой анализ ?
18. Каковы должны быть предосторожности при приготовлении растворов ?
1. Будьте готовы дать определение следующих терминов:
· количественный анализ;
· принцип, метод и методика анализа;
· аналитический сигнал;
· единичное и параллельное определение;
· динамический анализ и экспрессное определение;
· селективное определение;
· элементный, многоэлементный и функциональный анализ;
· молекулярный, компонентный и вещественный;
· субъективные и объективные методы;
· инструментальные методы анализа;
· неразрушающие методы анализа;
· метод (одной и серии) добавок;
· градуировочная характеристика;
· косвенный и прямой метод;
· макро–, полумикро–, микро–, ультрамикро–, субмикроанализ;
· определение «следов»;
· арбитражный анализ;
· хемометрика и экометрия;
· гибридные и комбинированные методы.
Литература
1. Другов Ю.С., Родин А.А. Экологическая аналитическая химия. С.-Перетбург: 2002. – 464 с.
2. Другов Ю.С. Экологическая аналитическая химия. С.-Пб.: Анатолия, 2000. – 432 с.
3. Израэль Ю.А. Экология и контроль состояния природной среды. М.: Гидрометеоиздат., 1984. – 560 с.
4. Майстренко В.Н.. Хамитов Р.З., Будников Г.К. «Эколого-аналитический мониторинг супертоксикантов. – М.: Химия, 1006. – 319 с.
5. Золотов Ю.А., Кузьмин Н.М., Кимстач В.А. и др. //Журн. Российского хими об-ва им. Д.И. Менделеева, 1993, №4, С. 8-20.
6. Кузьмин Н.М., Нейман Е.Я., Попов А.А.. Системы эколого-аналитического контроля в действии.. М., 1994. – С. 6-11.
7. Лайтинен Г.А., Харрис В.Е. Химический анализ. /Пер. с англ.. Под ред. Ю.А. Клячко. – 2-е изд., перераб. – М.: Химия, 1979. – с. 13-16.
8. Гильманишина С.И. Основы аналитической химии. Курс лекций. 2-е изд.. СПб.: Питер, 2006. – 224 с.: ил.
9. Основы аналитической химии. Учеб. для вузов. В 2 кн. /Под общ. ред. Ю.А. Золотова. – 2-е изд., перераб. и доп. М.: Высш. шк., 2002.
10. Основы аналитической химии. Практическое руководство: учеб. пособие для вузов. /Под общ. ред. Ю.А. Золотова. М.: Высш. шк., 2001.
11. Харитонов Ю.Я. Аналитическая химия (аналитика). В 2 кн. Учеб. для вузов. М.: Высш. шк., 2001.
12. Коренман И.М. Методы количественного химического анализа. М.: Химия, 1989. – 128 с.
13. Контроль химических и биологических параметров окружающей среды. /Под ред. Исаева Л.К. СПБ., Эколого-аналитический центр «Союз», 1998. – 896 с.
Лекция 2
КОЛИЧЕСТВО И КОНЦЕНТРАЦИЯ ВЕЩЕСТВА:
Дата добавления: 2016-01-09; просмотров: 2147;
