Термодинаміка – розділ молекулярної фізики, який вивчає теплові процеси без вияснення внутрішніх чинників структури речовини.
Тема 7: Основи термодинаміки
План
Тепловий рух. Внутрішня енергія і способи її зміни
2. Закон збереження енергії в теплових процесах (перший закон термодинаміки)
Принцип дії теплових двигунів
Термодинаміка – розділ молекулярної фізики, який вивчає теплові процеси без вияснення внутрішніх чинників структури речовини.
Термодинаміка була створена в середині ХІХ століття. Після відкриття закону збереження енергії. В її основі лежить поняття внутрішньої енергії U. У середині ХІХ століття. було доведено, що поряд з механічною енергією макроскопічні тіла мають ще й енергію всередині цих тіл. Ця внутрішня енергія входить до балансу енергетичних перетворень у природі. Після відкриття внутрішньої енергії був сформульований закон збереження і перетворення енергії в теплових процесах, у результаті якого внутрішня енергія може переходити в механічну і навпаки. З погляду МКТ речовини внутрішня енергія макроскопічного тіла термодинамічної системи дорівнює сумі кінетичних енергій неперервного теплового руху всіх молекул (атомів) відносно центра мас тіла і потенціальних енергій взаємодії всіх молекул одна з одною. Обчислити U, враховуючи мікропараметри майже неможливо, тому для її вираження використовують макропараметри термодинамічної системи.
Найбільш простий за властивостями – одноатомний газ. До одноатомних можна віднести інертні гази: гелій, неон, аргон та ін. Обчислимо внутрішню енергію одноатомного ідеального газу. Оскільки молекули цього газу одна з одною не взаємодіють, то потенціальна енергія Еп = 0. Уся внутрішня енергія складається із кінетичної енергії руху Ек. За формулою Больцмана для одного атома 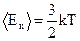 (де k = 1,38∙10-23 Дж/К – стала Больцмана). А оскільки кількість атомів дорівнює
(де k = 1,38∙10-23 Дж/К – стала Больцмана). А оскільки кількість атомів дорівнює 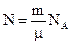 (див. лекцію 5), то внутрішня енергія одноатомного ідеального газу
(див. лекцію 5), то внутрішня енергія одноатомного ідеального газу 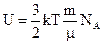 , де kNA = R.
, де kNA = R.
Остаточно маємо 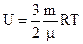 або
або 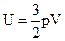 ,
,
де m – маса всього газу; μ – молярна маса; R = 8,31 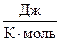 – універсальна газова стала; T – термодинамічна температура; p – тиск газу; V – об’єм газу.
– універсальна газова стала; T – термодинамічна температура; p – тиск газу; V – об’єм газу.
Дата добавления: 2015-10-26; просмотров: 802;
