ПРЕПАРАТИВНЫИ ЭЛЕКТРОФОРЕЗ БЕЛКОВ
Электрофорез в ПААГ не получил широкого распространения
в качестве препаративного метода фракционирования и очистки
белков. Одна из причин этого, по-видимому, состоит в трудности
осуществления равномерного теплоотвода из большой массы ге-
ля любой конфигурации (цилиндрической, кольцевой или плос-
кой). Неравномерность теплоотвода и возникающие в геле гра-
диенты температуры приводят, как уже отмечалось, к резкому
ухудшению качества разделения белков.
Вторая трудность связана с необходимостью создания удоб-
ной и надежной камеры элюции для сбора белков по мере их
последовательного выхода из геля. В многочисленных конструк-
циях, предлагавшихся в начале 70-х годов, такую камеру соз-
давали под вертикально расположенным гелем, отделяя ее от
нижнего электродного буфера диализной пленкой. Для сохране-
ния качества разделения белков камера элюции очень малого
объема должна быстро и полно, без застойных зон, промываться
элюирующим буфером, а выходящие из геля белки не должны
сорбироваться на ее поверхностях, в частности на диализной
пленке. Удачного решения этих проблем найдено не было. Столб
геля, деформируясь под собственной тяжестью, сползал в каме-
ру, застойные зоны при элюции приводили к смешиванию белков
из разных полос, сорбция на пленке оставалась значительной.
Недавно появилось сообщение об еще одной попытке преодо-
леть указанные трудности. Препаративное фракционирование
белков вели в кольцевом 2,3%-ном ПААГ с ДДС-Na. Диализную
мембрану, отделяющую камеру элюции от нижнего электродного
резервуара, заменили слоем 10%-ного ПААГ. Во избежание
сползания рабочего геля в камеру элюирующий буфер в нее по-
давался под гидростатическим давлением, уравновешивающим
вес геля, а скорость элюции задавалась перистальтическим на-
сосом, стоящим на выходе из камеры. Сама камера имела форму
незамкнутого кольца. Элюирующий буфер подавался с одного
ее конца и выходил с другого. Сообщается о хорошем разделе-
нии ряда белковс молекулярными массами 100—500 тыс. при за-
грузке в гель 4 мг белка [Hardman, Kane, 1980].
Из-за его оригинальности стоит упомянуть об одном решении
проблемы камеры элюции [Marceau et al., 1975]. ПААГ полиме-
ризуют в цилиндре из плексигласа, закрытом внизу диализной
мембраной, лежащей на пористой подложке. Над самой мембра-
ной в цилиндр открываются отверстия двух трубочек. Одна из
них используется для подкачки, вторая — для слива элюирую-
щего буфера. ПААГ не прилипает к плексигласу, и весь столб
геля может перемещаться вверх внутри цилиндра. Такое пере-
мещение на очень малое расстояние вызывается кратковремен-
ной подкачкой буфера под гель при закрытом сливе. Так созда-
ется камера элюции: она существует только то время, которое
необходимо для выхода в нее очередной полосы белка. Затем
открывают кран трубочки для слива буфера. Гель под действием
собственного веса оседает, и камера полностью опоражнивается.
Процесс повторяют либо регулярно, по заданной программе, ли-
бо при подходе к нижнему концу геля очередной окрашенной
маркером белковой полосы. Перед опорожнением камеры поляр-
ность напряжения на несколько секунд сменяют на обратную,
что помогает десорбции белков с мембраны.
Проще и надежнее вести элюцию заранее окрашенных белко-
вых полос последовательно, одну за другой, в сменные диализ-
ные мешочки [Sun, Hall, 1974]. В цитируемой работе ПААГ по-
лимеризовали тоже в цилиндре из плексигласа диаметром 3 см,
по оси которого проходила трубка для дополнительного охлаж-
дения геля циркулирующей водой. Гель высотой 21 см поддержи-
вался снизу найлоновой сеткой. Сменные диализные мешочки
легко одевались на нижний конец цилиндра с помощью поли-
этиленовых переходников. Перед снятием очередного мешочка
полярность напряжения на короткое время реверсировали. Та-
ким образом авторам удалось выделить из 6 мг исходного бел-
кового препарата три компонента, относительно мало различаю-
щиеся между собой по молекулярной массе (43, 47 и 53 тыс.
яальтон).
Возможно построить препаративную систему электрофореза
с последовательной элюцией белковых полос с нижнего края
пластины ПААГ. Фирма «Bio-Rad» предлагает для этой цели
специальные прокладки, используемые при полимеризации геля.
Конструкция прокладок позволяет подвести к нижнему краю ра-
бочего геля толщиной до 6 мм по обеим его сторонам две тру-
бочки, через которые потом и осуществляют элюцию белков.
Сначала между стеклянными пластинками формы полимеризуют
пробку из плотного ПААГ, затем, как раз на уровне трубочек и
на высоту их диаметра, заливают слой раствора сахарозы, а над
этим слоем уже полимеризуют рабочий гель. Сахарозу потом за-
мещает элюирующий буфер.
Для препаративного фракционирования белков нередко ис-
пользуют систему ступенчатого электрофореза, хотя иной раз и
из несколько других соображений, чем создание узкой началь-
ной полосы. Наличие дополнительного формирующего геля при
большой загрузке предохраняет от преципитации белка на гра-
нице рабочего геля, позволяет увеличить объем препарата, обес-
печивает удаление из него остатков соли до начала процесса
рабочего разделения и, наконец, снимает необходимость преэлек-
трофореза, так как основная часть персульфата успевает уйти
из рабочего геля к аноду до того, как в этот гель вступают бел-
ки. Максимальная загрузка ПААГ при препаративном фракцио-
нировании белков может достигать 5 мг на 1 см2 сечения геля.
Общим недостатком любых устройств с последовательной
элюцией белков в конце пути их миграции через весь гель явля-
ется продолжительность этого процесса и, в силу этого, диффу-
зия белковых зон (особенно для белков, выходящих последни-
ми), поэтому сейчас на практике отдают предпочтение обычному
(хотя и с увеличенной загрузкой) фракционированию белков в
трубках диаметром до 1,7 см или в толстых пластинах. Фракцио-
нирование ведут с примесью окрашенных «свидетелей», как было
описано выше. Аликвоту разделяемой смеси белков окрашивают
ремазолом [Sun, Hall, 1974] или посредством данзилирования
[Tijssen, Kurstak, 1979; Schetters, McLeod, 1979]; окрашенные
полосы вырезают и белки элюируют из геля за счет диффузии
или электрофореза (см. выше).
Следует иметь в виду, что при элюции белков из геля может
выходить большое количество линейного полиакриламида, не
вошедшего в состав матрицы геля. Он не обнаруживается при
оценке чистоты белка аналитическим электрофорезом. Между
тем аналитическое ультрацентрифугирование показывает, что
количество элюированного полиакриламида может быть таким
же, как и самого белка. Дополнительную очистку белка в этом
случае можно провести его сорбцией на ионообменную смолу
[Brooks, Sander, 1980].
Недавно был предложен оригинальный способ электрофоре-
тической элюции белков одновременно из нескольких полос ге-
ля, вырезанных из пластины после препаративного электрофоре-
за [Judd, 1979]. На прямоугольный поднос наносят ровный слой
.пропитанного буфером сефадекса Г-25 «суперфайн» толщиной
2—3 мм. С интервалом в 1—1,5 см перпендикулярно длинной
стороне подноса в сефадексе выскребают канавки, куда укла-
дывают полоски геля (рис. 30). По концам подноса на сефадекс
через смоченную буфером фильтровальную бумагу кладут уголь-
ные электроды и подают напряжение. Под действием электриче-
ского поля белки из каждой полоски геля мигрируют в прилежа-
щий слой сефадекса. Эти слои затем снимают, переносят в мик-
роколонки и белки из них элюируют.
Кстати, можно просто заполнить сефадексом вертикальную
колонку и использовать его в качестве антиконвекционной среды
для препаративного электрофореза белков. Это, конечно, уже не
электрофорез в геле, и качество фракционирования будет заве-
домо хуже, но для грубого разделения смеси белков оно может
быть вполне приемлемым.
Отметим также успешное фракционирование до 1 г белковой
смеси электрофорезом в градиенте концентрации раствора саха-
розы (10—45%) в буфере с рН 8,5. Электрофорез вели в цилиндре
диаметром 12 см и высотой 17 см [Walters, Bont, 1979]. Тонкость
метода — в наслаивании препарата на раствор сахарозы с по-
мощью металлического сита, которое поднимается по мере уве-
личения объема препарата, оставаясь сцепленным с мениском
жидкости силами поверхностного натяжения. Это позволяет на-
|
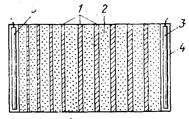
Рис. 30. Схема электрофоретиче-
ской элюции белков из геля в се-
фадекс [Judd, 1979]
1—полоски, вырезанные из геля; 2—
сефадекс Г-25 «суперфайн»; 3 — уголь-
ные электроды; 4 — смоченная буфе-
ром фильтровальная бумага
нести 30 мл исходного белкового препарата совершенно ровным
слоем толщиной 3 мм. Электрофорез во избежание разогрева
жидкости ведут при малой плотности тока (0,2 мА/см2) в тече-
ние 15 ч. Фракции собирают, сливая содержимое колонки через
воронку, расположенную в ее нижней части. Препаративный
электрофорез в 5—25%-ном градиенте сахарозы в 0,1 М Трис-
боратном буфере (рН 8) с 6 М мочевиной был недавно исполь-
зован для очистки фотохимически сшитого комплекса тРНК и
тРНК-синтетазы [Renaud et al., 1979].
К электрофорезу в геле эти методы, разумеется, прямого от-
ношения не имеют, так как являются примерами электрофореза
в свободной жидкости. Именно с этого начиналось применение
электрофореза для фракционирования биополимеров. Однако за
последнее десятилетие, во всяком случае для аналитических це-
лей, электрофорез в свободной жидкости был полностью вытеснен
электрофорезом в гелях или на твердых носителях (бумаге, раз-
личных производных целлюлозы, полиамидных пленках и т. д.),
который широко применялся при фракционировании пептидов,
аминокислот и других сравнительно низкомолекулярных биоло-
гически важных молекул, в том числе и в высоковольтных ва-
риантах. В свое время, например, очень важную роль сыграл
метод фракционирования олигонуклеотидов гидролизата РНК
двумерным электрофорезом. В первом направлении разделение
вели на полосках ацетатцеллюлозы в пиридин-ацетатном буфе-
ре (рН 3,5) с добавлением 7 М мочевины, во втором — на ДЭАЭ-
бумаге в 7%-ной НСООН [Brownlee, 1972]. Ввиду малой емко-
сти ацетатцеллюлозы общая загрузка не превышала 0,1 мг гид-
ролизата РНК, поэтому использовали препараты, меченные ра-
диоактивным фосфором.
Сейчас методы фракционирования низкомолекулярных био-
логических объектов электрофорезом на твердых носителях на-
столько энергично и успешно вытесняет жидкостная хроматогра-
фия под высоким давлением (ЖХВД), что рассматривать их
уже не имеет смысла. Впрочем, изредка электрофорез на твер-
дом носителе еще используют и для фракционирования белков.
Так, сравнительно недавно было описано очень хорошее разде-
ление девяти модификаций казеина молока электрофорезом на
полосках ацетатцеллюлозы. Эти модификации различались уров-
нем фосфорилирования белка, и разделение шло по величине
электрического заряда [West, Towers, 1976].
Дата добавления: 2015-10-21; просмотров: 1511;
