Примеры решения задач. Пример 41. Золь оксалата серебра образуется при медленном приливании водного раствора оксалата аммония к водному раствору нитрата серебра
Пример 41. Золь оксалата серебра 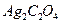 образуется при медленном приливании водного раствора оксалата аммония
образуется при медленном приливании водного раствора оксалата аммония 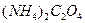 к водному раствору нитрата серебра
к водному раствору нитрата серебра 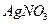 . Напишите формулу мицеллы и укажите знак электрического заряда коллоидной частицы этого золя.
. Напишите формулу мицеллы и укажите знак электрического заряда коллоидной частицы этого золя.
Решение:Образование золя 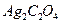 происходит по реакции:
происходит по реакции:
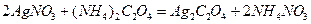 .
.
Строение мицеллы и заряд коллоидной частицы зависят от способа получения коллоидного раствора. Поскольку раствор 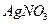 взят в избытке, то на поверхности агрегата
взят в избытке, то на поверхности агрегата 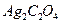 будут адсорбироваться ионы
будут адсорбироваться ионы 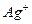 . Противоионы
. Противоионы 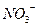 будут образовывать адсорбционный и диффузный слои. Формула мицеллы будет следующая:
будут образовывать адсорбционный и диффузный слои. Формула мицеллы будет следующая:
 .
.
Коллоидная частица приобретает положительный заряд.
Пример 42. Золь гидроксида магния получен путем смешивания 0,02 л 0,01 н. раствора 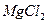 и 0,028 л 0,005 н. раствора
и 0,028 л 0,005 н. раствора  . Определите заряд частиц полученного золя и напишите формулу его мицеллы.
. Определите заряд частиц полученного золя и напишите формулу его мицеллы.
Решение:При смешивании растворов 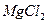 и
и  протекает реакция:
протекает реакция:
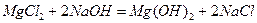 .
.
Количество моль-эквивалентов (nэк) 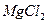 и
и  , участвующих в реакции, определяем по формуле:
, участвующих в реакции, определяем по формуле:
 .
.
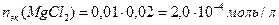
 .
.
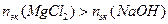 .
.
Из этого следует, что в избытке будет раствор 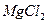 . Он будет ионным стабилизатором. На ядре коллоидной частицы золя
. Он будет ионным стабилизатором. На ядре коллоидной частицы золя 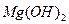 будут адсорбироваться ионы
будут адсорбироваться ионы  и частица золя приобретет положительный заряд. Противоионами являются ионы
и частица золя приобретет положительный заряд. Противоионами являются ионы 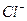 .
.
Формула мицеллы золя гидроксида магния имеет вид:
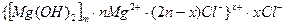
Пример 43. В каждую из трех колб налито по 0,01 л золя хлорида серебра. Для коагуляции золя в первую колбу добавлено 0,002 л 1М раствора  , во вторую - 0,012 л 0,01 М
, во вторую - 0,012 л 0,01 М  , в третью - 0,007 л 0,001 М
, в третью - 0,007 л 0,001 М  . Вычислите пороги коагуляции электролитов, определите знак заряда частиц золя.
. Вычислите пороги коагуляции электролитов, определите знак заряда частиц золя.
Решение:Порог коагуляции вычисляется по формуле:
.
Вычисляем пороги коагуляции добавляемых электролитов:
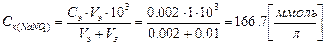 ;
;
 ;
;
.
Добавляемые электролиты содержат анион 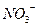 и катионы
и катионы 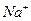 ,
,  и
и 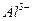 разной зарядности. Наименьший порог коагуляции у
разной зарядности. Наименьший порог коагуляции у  , следовательно, частицы золя хлорида серебра заряжены отрицательно.
, следовательно, частицы золя хлорида серебра заряжены отрицательно.
Пример 44. Порог коагуляции раствора  для золя гидроксида алюминия, частицы которого заряжены положительно, равен 60,0 ммоль/л. Рассчитайте порог коагуляции
для золя гидроксида алюминия, частицы которого заряжены положительно, равен 60,0 ммоль/л. Рассчитайте порог коагуляции 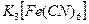 для этого золя.
для этого золя.
Решение:
Коагуляцию золя вызывает тот из ионов прибавленного электролита, заряд которого противоположен заряду коллоидной частицы. Коагулирующая способность иона определяется его зарядом: чем больше заряд иона, тем выше его коагулирующая способность. Значение порогов коагуляции электролитов с одно-, двух- и трехзарядными ионами относятся как числа 729:11:1. Следовательно, порог коагуляции 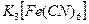 , будет в 729 раз меньше, чем у
, будет в 729 раз меньше, чем у  , т.е.:
, т.е.:
 .
.
КОНТРОЛЬНЫЕ ЗАДАНИЯ ДЛЯ САМОСТОЯТЕЛЬНОЙ РАБОТЫ
Задача 29
Составьте формулу мицеллы золя, полученного путем смешивания растворов 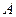 и
и 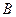 указанных объемов
указанных объемов 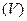 и концентраций
и концентраций  .
.
| Вар. | Золь | Раствор А | VА, мл | C, моль/л | Раствор В | VВ, мл | C, моль/л |
| PbSO4 | Pb(NO3)2 | 0,001 н. | K2SO4 | 0,04 М | |||
| AgCl | KCl | 0,02 М | AgNO3 | 0,005 М | |||
| Zn(OH)2 | NaOH | 0,05 М | ZnCl2 | 0,04 н. | |||
| BaSO4 | BaCl2 | 0,002 н. | H2SO4 | 0,005 М | |||
| As2S3 | H2S | 0,06 н. | AsCl3 | 0,001 н. | |||
| Ni(OH)2 | NaOH | 0,001 М | NiCl2 | 0,004 н. | |||
| CuS | CuCl2 | 0,002 н. | H2S | 0,0 М | |||
| AgBr | AgNO3 | 0,008 М | NaBr | 0,009 М | |||
| SrSO4 | Sr(NO3)2 | 0,0005 н. | K2SO4 | 0,004 н. | |||
| Al(OH)3 | AlCl3 | 0,06 н. | NaOH | 0,08 М | |||
| PbCl2 | KCl | 0,05 М | Pb(NO3)2 | 0,01 н. | |||
| CaSO4 | CaCl2 | 0,002 н. | Al2(SO4)2 | 0,01 н. | |||
| H2SiO3 | K2SiO3 | 0,001 М | HCl | 0,05 М | |||
| AgI | AgNO3 | 0,04 М | KI | 0,01 М | |||
| Fe(OH)3 | NaOH | 0,002 н. | Fe2(SO4)3 | 0,0001 н. | |||
| ZnS | ZnCl2 | 0,001 н. | (NH4)2S | 0,003 н. | |||
| PbI2 | KI | 0,0023 М | Pb(NO3)2 | 0,003 н. | |||
| AgCl | HCl | 0,05 М | AgNO3 | 0 004 М | |||
| Hg2SO4 | Hg2(NO3)2 | 0,001 н. | H2SO4 | 0,001 н. | |||
| Co(OH)2 | NaOH | 0,04 М | CoCl2 | 0,004 М | |||
| AgI | KI | 0,01 М. | AgNO3 | 0,1 М | |||
| MnS | MnCl2 | 0,05 н. | (NH4)2S | 0,1 н. | |||
| Ag2CrO4 | K2CrO4 | 0,05 н. | AgNO3 | 0,04 М | |||
| PbSO4 | K2SO4 | 0,001 н. | Pb(NO3) | 0,02 н. | |||
| H2SiO3 | HCl | 0,003 М | K2SiO3 | 0,1 н. | |||
| Co(OH)2 | Co(NO3)2 | 0,02 н. | KOH | 0,05 М |
Дата добавления: 2015-10-19; просмотров: 6290;
