Химия меди и ее соединений
В природе медь находится в основном в виде соединений: халькозина Cu2S, ковелина CuS, куприта Cu2O, малахита (CuOH)2CO3 и других соединений, но встречается и в самородном состоянии. Получение обычно складывается из нескольких этапов: обжига сульфидов, восстановления полученных оксидов углем и рафинирования меди:
2CuS + 3O2 ® 2SO2 + 2CuO
CuO + СО ® Cu + СО2
Медь - мягкий красный металл, хорошо проводит тепло и электрический ток. Медь образует сплавы: латунь (60-90% Cu и 10-40% Zn), бронзы (например, 80% Cu, 15%Sn, 5% Zn), мельхиор (80% Cu, 20% Ni) и другие сплавы.
Медь расположена в ряду напряжений после водорода и не реагирует с обычными кислотами в отсутствии окислителей:
Cu + H2SO4 (разб.) ¹
Cu + HСl ¹
Однако медь реагирует с кислотами окислителями:
Cu + 2H2SO4 (конц.) ® CuSO4 + SO2 + 2H2O
Cu + 4HNO3 (конц.) ® Cu(NO3)2 + 2NO2 + 2H2O
3Cu + 8HNO3 (разб.) ® 3Cu(NO3)2 + 2NO + 4H2O
Красный оксид меди(I) Cu2O образуется при нагревании до 200оС меди на воздухе при недостатке кислорода. Соответствующий оксид CuOH нестоек, распадаясь на оксид и воду, и легко окисляется до Cu(OH)2. Из соединений меди(I) устойчивы лишь комплексные соединения, например, [Cu(NH3)2]OH или H[Cu(CN)2], или малорастворимые вещества, например белый CuI.
Черный оксид меди(II) CuO получается при нагревании меди на воздухе выше 300оС при избытке кислорода. При нагревании выше 1000оС CuO распадается на Cu2O и кислород.
Голубой осадок гидроксида меди(II) Cu(OН)2 получают действием щелочей на соли меди(II):
CuSO4 + 2NaOH ® Cu(OН)2¯ + Na2SO4
При нагревании этот осадок чернеет вследствие образования черного оксида меди(II):
Cu(OН)2¯ 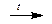 СuO + H2O
СuO + H2O
Гидроксид меди(II) Cu(OН)2 имеет амфотерные свойства с преобладанием основных свойств. Кислотные свойства Cu(OН)2 не наблюдаются в растворах, но проявляются при сплавлении или действии концентрированных щелочей:
Cu(OН)2¯ + Н2SO4 ® CuSO4 + 2H2O
Cu(OН)2¯ + NaOH ¹ не идет в растворе
Cu(OН)2¯ + 2NaOH (конц.) ® Na2[Cu(OH)4]
Ионы меди(II) образуют комплексные соединения. Так, образование интенсивно-синего тетраммина меди(II) используется для обнаружения ионов меди(II) в растворе:
CuSO4 + 4NH4OH ® [Cu(NH3)4]SO4 + 4H2O
Соли меди(II) имеют вследствие гидролиза кислую среду:
2CuSO4 + 2H2O  (CuOH)2SO4 + H2SO4
(CuOH)2SO4 + H2SO4
Cu2+ + SO42- + H2O  CuOH+ + H+ + SO42-
CuOH+ + H+ + SO42-
Cu2+ + H2O  CuOH+ + H+ (pH<7)
CuOH+ + H+ (pH<7)
Окислительные свойства для ионов меди(II) мало характерны, но проявляются при взаимодействии с иодид-ионом:
2CuSO4 + 4KI ® 2CuI¯ + I2 + 2K2SO4
Медь является микроэлементом. В больших концентрациях соединения меди токсичны и используются как пестициды.
Дата добавления: 2015-09-07; просмотров: 1378;
