Основные направления реакционной способности углеводородов в зависимости от их
Электронного строения
| Класс углеводородов | Общая формула | Гибридизация | Орбитали | Связи | Механизм и направление реакции |
| Алканы | СnH2n+2 | sp3 | 4sp3 | 4s | SR |
| Алкены | CnH2n | sp2 | 3sp2, p | 3s, p | AE |
| Алкадиены (сопряженные) | CnH2n-2 | sp2 | 3sp2, p | 3s, сопряженная p-система | AE (1,2;1,4;3,4) |
| Арены | CnH2n-6 | sp2 | 3sp2, p | 3s, замкнутая сопряженная p-система | SE |
Алканы
Алканами называются углеводороды, общая формула которых СnH2n+2
| Название | Структурная формула | Брутто-формула |
| Метан | СH4 | CH4 |
| Этан | CH3-CH3 | C2H6 |
| Пропан | CH3-CH2-CH3 | C3H8 |
| Бутан | CH3-CH2-CH2-CH3 | C4H10 |
| Пентан | CH3-(CH2)2-СH2-CH3 | С5Н12 |
| Гексан | СН3-(СН2)4-СН3 | С6Н14 и т.д. |
Низшие представители алканов при вдыхании обладают наркотическим действием, в более высоких концентрациях вызывают остановку дыхания. Токсичность и сила наркотического действия возрастают с увеличением количества углеродных атомов до 5–7. При дальнейшем изменении цепи активность снижается вследствие уменьшения летучести и растворимости в воде. Высшие представители почти инертны. Алканы физиологически менее активны, чем алкены или арены, что объясняется их строением.
Алканы содержат атомы углерода в sp3 – гибридизации. 1s – и 3р – орбитали образуют 4 sp3 – гибридизованные орбитали, направленные в пространстве к вершинам тетраэдра под углом 109°. Эти орбитали участвуют в образовании 4-х прочных неполярных s- связей.

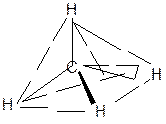 |
Строение метана (СН4):
а) электронное б) пространственное
(тетраэдрическое)
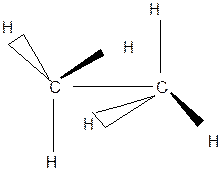
Строение этана (СН3-СН3):
 | |||
 | |||
а) электронное б) пространственное
Изомерия.Для алканов характерна
1. Структурная изомерия: Например,





 СН3 СН2 СН2 СН3 СН3 СН СН3
СН3 СН2 СН2 СН3 СН3 СН СН3
бутан
СН3
изобутан (2–метилпропан)
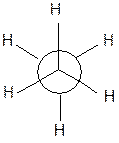
2. Пространственная (конформационная) изомерия. Этот вид изомерии является результатом свободного вращения вокруг одинарной s С-С связи. Геометрические формы молекулы, образующиеся при этом, называются конформациями. Среди множества конформаций этана выделяют экстремальные конформации – наименее (а) и наиболее (б) устойчивые:
 |  | ||||||
 | |||||||
 | |||||||
а) заслоненная б) заторможенная
В заслоненной конформации атомы водорода сближены и отталкиваются друг от друга. Это энергетически невыгодно (энергия молекулы максимальна).
В заторможенной конформации атомы водорода наиболее удалены друг от друга. Это наиболее выгодная конформация (энергия молекулы минимальна).
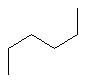
Для 5- и 6-членных углеводородных цепей можно выделить три основные конформации:
 | |||||
 | |||||
 | |||||
а) зигзагообразная б) нерегулярная в) клешневидная
Клешневидная конформация дает нам представление о возможности образования 5- и 6-членных циклов. Более длинные углеводородные цепи по данным рентгеноструктурного анализа имеют, в основном, зигзагообразную конформацию.
Дата добавления: 2015-09-28; просмотров: 654;
