Сопряженные системы
Если 2 p связи разделены одной простой s- связью или рядом с p- связью расположен атом с р-орбиталью (занятой 1 или 2р- электронами или вакантной), то имеет место частичное перекрывание (взаимодействие) формально не связанных р-орбиталей.
Возникает общая p- электронная система с делокализованной электронной плотностью, энергетически стабильная и реагирующая на внешнее влияние как единое целое.
Такие системы называются сопряженными системами. Они могут быть открытыми или замкнутыми и содержать не только атомы углерода, но и гетероатомы.
В зависимости от принадлежности р- орбиталей к двум p-связям или к p-связи и одному атому с р-орбиталью различают p,p- или р,p- сопряженные системы.
·
·
· ·
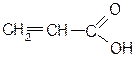
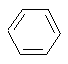
акриловая кислота бензол
p,p - сопряженные системы
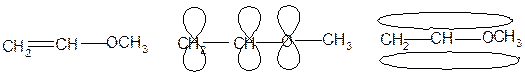
·· ·-------·- ---·· · · ··
·· ---------------------
метилвиниловый эфир
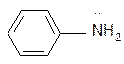 | |||
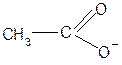 | |||
анилин ацетат ион
р,p - сопряженные системы
 вакантная р-орбиталь
вакантная р-орбиталь
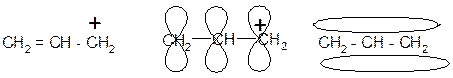 |
· · · · . .
аллил-катион
Передача электронного влияния по системе сопряжения называется эффектом сопряжения и обозначается символом [M].
Заместители – доноры проявляют [+M] эффект. Например, NH2, OH, Сl, OR и другие. Заместители – акцепторы – [-M] эффект. Например, NO2, COOH, >C=O, SO3H и др.
В зависимости от характера связи углеводороды делятся на классы: алканы, циклоалканы, алкены, алкадиены, арены и др.
Таблица 1
Дата добавления: 2015-09-28; просмотров: 611;
