Атты денелер.
Қатты денелердің атомдарының арасындағы тартылыс және тербеліс күштері олардың сыртқы пішінін сақтауға жауапты болып табылады. Бұл күштер электрондар мен ядролардың өзара әсерлесулерінен пайда болады. Атомдар арасындағы әсерлесу күштерінің жеке-жеке табиғатына тоқталмай тұрып, бұл күштердің барлығына ортақ жалпы сипаттамаларына тоқталайық.
Ол үшін атомдар арасындағы тартылыс (1) және тебіліс (2) күштерінің потенциалдық энергиясының атомдар арақашықтығына 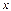 байланысты қалай өзгеретіндігін (4-сурет) қарастырайық. Өйткені потенциалдық энергия осы келтірілген күштерді жеңу үшін жұмсалатын күштің жұмысын береді. Суретте келтірілген (3) қисық екі атомнан тұратын жүйенің потенциалдық энергиясының қорытқы өзгерісін көрсетеді. Атомдар арасындағы тартылыс (1) тебіліс (2) және қорытқы (3) күштің өзгерісін сызба түрінде көрсетуге болады. Бұл жерде тартылыс күшін шартты түрде теріс деп алуға келісілген. Атомдар арасындағы тартылыс күші қысқа аралықта әсер ететіндіктен, ол атомдардың арақашықтығы өзгергенде тартылыс күшіне қарағанда тезірек азаяды. Сондықтан атомдардың арақашықтығы бір
байланысты қалай өзгеретіндігін (4-сурет) қарастырайық. Өйткені потенциалдық энергия осы келтірілген күштерді жеңу үшін жұмсалатын күштің жұмысын береді. Суретте келтірілген (3) қисық екі атомнан тұратын жүйенің потенциалдық энергиясының қорытқы өзгерісін көрсетеді. Атомдар арасындағы тартылыс (1) тебіліс (2) және қорытқы (3) күштің өзгерісін сызба түрінде көрсетуге болады. Бұл жерде тартылыс күшін шартты түрде теріс деп алуға келісілген. Атомдар арасындағы тартылыс күші қысқа аралықта әсер ететіндіктен, ол атомдардың арақашықтығы өзгергенде тартылыс күшіне қарағанда тезірек азаяды. Сондықтан атомдардың арақашықтығы бір 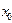 шамасына жеткенде тартылыс және тебіліс күштерінің шамалары теңесіп, қорытқы күштің шамасы нөлге тең болады. Мысалы, жылулық қозғалыстың арқасында атомдардың арақашықтығы үлкейетін
шамасына жеткенде тартылыс және тебіліс күштерінің шамалары теңесіп, қорытқы күштің шамасы нөлге тең болады. Мысалы, жылулық қозғалыстың арқасында атомдардың арақашықтығы үлкейетін 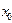 болса, онда атомдардың арасында оларды бір-біріне жақындататын тартылыс күші пайда болады. Егер де атомдардың арақашықтығы кішірейетін болса, онда қорытқы күш оларды бір-бірінен қашықтатуға тырысады.
болса, онда атомдардың арасында оларды бір-біріне жақындататын тартылыс күші пайда болады. Егер де атомдардың арақашықтығы кішірейетін болса, онда қорытқы күш оларды бір-бірінен қашықтатуға тырысады.
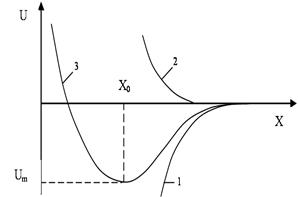
4-сурет
Күштердің тепе-теңдік шартына сәйкес келетін аралықта 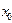 потенциалдық энергия ең үлкен мәніне ие болады. Күш пен оның потенциалдық энергиясының арасындағы арақашықтыққа байланысты тәуелділікті мынадай өрнек арқылы көрсетуге болады.
потенциалдық энергия ең үлкен мәніне ие болады. Күш пен оның потенциалдық энергиясының арасындағы арақашықтыққа байланысты тәуелділікті мынадай өрнек арқылы көрсетуге болады.
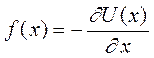
Сонда 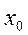 нүктесінде
нүктесінде 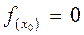 болса, онда потенциалдық энергия
болса, онда потенциалдық энергия 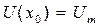 ең үлкен мәнін қабылдайды. Бұл потенциалдық энергияның шамасы атомдар арасындағы байланысты жоюға жұмсалатын жұмыстың шамасына тең болады. Сондықтан
ең үлкен мәнін қабылдайды. Бұл потенциалдық энергияның шамасы атомдар арасындағы байланысты жоюға жұмсалатын жұмыстың шамасына тең болады. Сондықтан 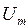 атомаралық байланыс энергиясы деп аталады.
атомаралық байланыс энергиясы деп аталады. 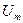 мен атомаралық күштерді сипаттайтын шамалар бір-бірлерінен айырылатындығына қарамастан, потенциалдық энергия және атомдардың өзара әсерлесу күшінің олардың арқашықтығына тәуелділігі үшін жоғарыда келтірілген тұжырымдар екі атом үшін де, оңашаланған молекула үшін де, тіпті қатты денедегі бірнеше көршілес атомдар мен қоршалған екі атом жұптары үшін де бірдей сипатталады.
мен атомаралық күштерді сипаттайтын шамалар бір-бірлерінен айырылатындығына қарамастан, потенциалдық энергия және атомдардың өзара әсерлесу күшінің олардың арқашықтығына тәуелділігі үшін жоғарыда келтірілген тұжырымдар екі атом үшін де, оңашаланған молекула үшін де, тіпті қатты денедегі бірнеше көршілес атомдар мен қоршалған екі атом жұптары үшін де бірдей сипатталады.
Атомдар аралығындағы тебіліс күші. Алғаш қарағанда атомдар арасындағы тебіліс күші әсерлесуші екі атомдар ядроларының арасындағы электростатикалық тебіліс күші сияқты болып көрінеді. Шындығында ядролар арасындағы кулондық тебіліс күші оған өзінің аз ғана үлесін қосады. Бұл күштің шамасы атом нөмірі өскен сайын азая береді. Өйткені ядро өрісін, атомның ішкі электрондық қабатындағы электрондар өрісі көлегейлейді.
Тебіліс күшінің пайда болуын атомның сыртқы электрондық қабатындағы электрондардың үлесі көп болады. Мысал ретінде екі атомнан тұратын жүйені қарастырайық. Егер атомдардың арақашықтығы Бор орбитасының радиусынан көп үлкен болса, ондағы электрондар бір-бірімен әсерлеспейді. Өйткені бір атомға тиісті электрондар екінші атомның электрондар орналасқан орбитасына түспейді. Онда бұл екі атомды байланысқан жүйе деп қарастыруға болмайды. Сондықтан көршілес атомдардың электрондары бірдей кванттық күйде қалады. Олар бірдей кванттық сандармен сипатталады.
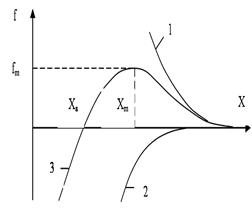
5-сурет
Егер көршілес екі атомның арақашықтығы Бор орбитасының радиусынан кіші болса, онда көршілес атомдардың электрондары бірінің өрісінде бірі жатады. Енді олар өздерінің алғашқы күйлерін сақтай алмайды. Ол Паули принципіне қайшы келеді. Сондықтан атомдар бір-біріне жақындаған кезде электрондар өздерінің алғашқы күйлері мен энергияларын өзгертуге мәжбүр болады. Осындай шарт орындалған кезде жеке атомның қорытқы энергиясына қарағанда, жүйеге біріккен атомдардың энергиясы анағұрлым жоғары болады. Сонда электрондардың ішкі энергиясының өзгерісі мен ядролардың кулондық өзара әсерлесу күшінің потенциалдық энергиясы, атомдардың өзара тебіліс күштерінің потенциалдық энергиясын құрайды. Тебіліс күшінің потенциалдық энергиясын есептеу үлкен теориялық дайындықты қажет ететін болғандықтан, тәуелділікті дәрежелі немесе экспоненциальды функциялар түрінде жуықтау жүргізіп, былай жазуға болады.
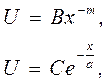
мұндағы: 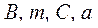 - тәжірибеден анықталатын тұрақты сандар.
- тәжірибеден анықталатын тұрақты сандар.
Инертті газдар үшін  тең болады.
тең болады.
Атомдар аралығындағы тартылыс күші. Атомдар арасындағы тартылыс күші байланыс күші деп аталады. Ол атомдардың сыртқы электрондық орбиталарын толтыратын электрондардың өзара әсерлесу күштерінен құралады. Байланыс күштерін жалпы түрде мынадай түрлерге:
- валенттілік,
- металдық,
- иондық,
-сутегілік,
- Ван-дер-Вальстық деп бөледі.
Дата добавления: 2015-09-21; просмотров: 2039;
