Тема: Біологічна роль Карбону
План
1. Особливості будови атома Карбону.
2. Ступені окиснення атому Карбону у сполуках.
3. Властивості неорганічних сполук Карбону.
4. Біологічна роль сполук Карбону.
Час виконання - 2 години.
Мета роботи: ознайомитися з біологічною роллю Карбону та його неорганічних сполук.
Карбону належить головна роль в утворенні біосистем. Атоми Карбону, завдяки особливій будові верхнього енергетичного рівня (чотири валентні електрони в збудженому стані розміщені на 2s12p3 орбіталях, здатних до
sp3-, sp2- i sp –гібридизації), утворюють міцні зв’язки – прості, подвійні або потрійні. Вони сполучаються між собою у лінійні, розгалужені та циклічні структури, причому можуть замикатися в цикли як між собою, так і за участю гетероатомів (N, P, O, S), утворюючи карбоциклічні та гетероциклічні сполуки.
У хімічних сполуках Карбон може виявляти різні ступені окиснення: -4 (СН4, SiC), -1 (CaC2, Ag2C2), 0 ( Cграфіт, Салмаз), +2 (СО, HCN), +4 (СО2, Н2СО3), причому в складі однієї молекули можуть знаходитися атоми з різними ступенями окиснення. Це також є причиною багатоманітності сполук даного елемента.
Неорганічними сполуками Карбону є його бінарні сполуки з металами (карбіди – СаС2, АІ4С3 та ін.) та неметалами (CS2, CF4, SiC), оксиди (СО і СО2), карбонатна кислота та її солі (карбонати і гідрогенкарбонати), ціанідна і тіоціонатна кислоти та солі цих кислот – ціаніди, тіоціанати (роданіди) та ін.
Карбон (ІІ) оксид, або чадний газ СО – це безбарвний, дуже отруйний газ, який одержують при неповному згорянні різних видів палива
2С + О2 = 2СО.
У хімічному відношенні це несолетворний оксид, який за звичайних умов не реагує з водою, кислотами, лугами. Тільки при пропусканні його крізь розплав лугів утворюються солі метанової кислоти:
СО + КОН 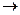 НСООК.
НСООК.
З гемвмісними білками, зокрема гемоглобіном крові, карбон (ІІ) оксид утворює карбоксигемоглобін – стійку комплексну сполуку, яка на відміну від гемоглобіну не може зв’язувати і переносити кисень від легень до тканин. Тому вже при незначній концентрації СО в повітрі (0,07 % об.) наступає отруєння людини. Для захисту організму від чадного газу використовують спеціальні протигази, обладнані гопкалітовим патроном. Цей патрон заповнюють сумішшю оксидів MnO2 i CuO, які можуть реагувати з карбон (ІІ) оксидом. Антидотом при отруєннях чадним газом є кисень, надлишкову концентрацію якого створюють у спеціальній барокамері (метод оксигенобаротерапії).
Гідроген ціанід HCN (стара назва – ціаністий водень) за звичайних умов існує у вигляді рідини, яка добре змішується з водою, утворюючи ціанідну або синильну кислоту. Ця кислота та її солі (ціаніди) – дуже отруйні сполуки. Навіть у мізерних дозах (ГДК – 0,01 мг/м3) вони смертельно діють на організм, що пояснюється їх високою здатністю до комплексоутворення, особливо з d – елементами. Ціанід – йони легко зв’язуються з катіонами Феруму (ІІ), що входять до складу цитохромів – групи ферментів ланцюга дихання. Оскільки вміст цитохромів в організмі менший , ніж гемоглобіну, то стає зрозумілою причина більшої токсичності синильної кислоти порівняно з чадним газом (смертельна доза – 0,05 г).
Проте у мікрокількостях ціанід – йони утворюються в організмі і використовуються ним для побудови деяких біоструктур, зокрема ціанокобаламіну (вітаміну В12). У молекулі цього вітаміну ціанід – йони виконують роль лігандів у складі хелатного комплексу.
Ціанідна кислота та її солі як продукти обміну виділяються з організму з повітрям та сечею у вигляді неотруйного роданід – йона SCN -, який утворюється за реакцією:
CN - + S = SCN –
При отруєнні ціанідами застосовують кисень, метгемоглобіноутворювачі (амілнітрат, натрію нітрит) або натрію тіосульфат, який реагує з калій ціанідом за рівнянням:
KCN + Na2S2O3 = KSCN + Na2CO3.
Важливою сполукою Карбону (ІV) є діоксид карбону СО2 (вуглекислий газ), який є кінцевим продуктом біологічного окиснення в клітинах різних біосубстратів – глюкози, ліпідів та, меншою мірою, білків.
У хімічному відношенні СО2 - кислотний оксид, який відповідає карбонатній кислоті Н2СО3. Це слабка кислота, яка утворює середні та кислі солі – відповідно карбонати та гідрогенкарбонати. У розчині вона дисоціює ступінчасто:

 Н2СО3
Н2СО3 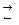 Н + + НСО3- І стадія
Н + + НСО3- І стадія
НСО3- 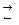 Н + + СО32- ІІ стадія
Н + + СО32- ІІ стадія
Процес дисоціації практично відбувається за першою стадією, тому в плазмі крові присутні гідрогенкарбонат – йони НСО3-, які в суміші з карбонатною кислотою утворюють карбонатну буферну систему крові.
Отже, одна частина вуглекислого газу зв’язується (гідратується), а інша – виділяється з організму шляхом дифузії. З клітин СО2 спочатку дифундує в міжклітинну рідину, а потім у плазму, де частково розчиняється у воді. Решта його проникає в еритроцити, в яких СО2 зв’язується з білковою частиною молекули гемоглобіну – глобіном, утворюючи нестійкий карбамін
R – NH2 + CO2 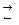 R – NH – COOH
R – NH – COOH
Зв’язаний вуглекислий газ виноситься еритроцитами до альвеол легень, де він виділяється з повітрям, яке ми видихаємо.
Вміст вуглекислого газу в атмосфері становить близько 0,03 % за об’ємом. Він відіграє важливу роль у підтриманні певного температурного режиму на поверхні Землі, оскільки молекули вуглекислого газу здатні вбирати УФ – випромінювання, запобігаючи витоку тепла за її межі. Проте, через активну виробничу діяльність людства спостерігається постійне збільшення концентрації вуглекислого газу в атмосфері, що призводить до глобальних кліматичних змін („парникового ефекту”).
Дата добавления: 2015-09-18; просмотров: 7898;
