Химические свойства. Большинство фенолов – бесцветные твердые вещества
Большинство фенолов – бесцветные твердые вещества. Простейший фенол C6H5OHобладает характерным запахом,плавится при 42оС. Температура плавления фенола сильно понижается от примеси небольших количеств воды (кристаллогидрат C6H5OH•H2O плавится при 16оС). Фенол гигроскопичен, кристаллы его при стоянии на воздухе расплываются. Раствор фенола в воде обладает антисептическими свойствами. Пары фенола токсичны, а сам он вызывает ожоги кожи.
Химические свойства фенола определяются наличием гидроксигруппы и бензольного кольца, взаимно влияющих друг на друга
Сопряжение неподеленной электронной пары атома кислорода гидроксильной группы приводит к смещению электронной плотности в сторону бензольного кольца, что усиливает подвижность атома водорода. Фенолы являются более сильными кислотами, чем предельные одноатомные спирты (pКа =10). Кислотность фенолов зависит также от характера заместителей в ядре. Введение в ядро электроноакцепторных заместителей (нитрогруппы, атомов галогенов) приводит к увеличению кислотных свойств.
С другой стороны, являясь заместителем I рода, гидроксигруппа приводит к повышению электронной плотности в о- и п-положениях бензольного кольца, что облегчает реакции электрофильного замещения.
Двух- и трехатомные фенолы во многих химических реакциях обнаруживают сходство с одноатомными фенолами, участвуя одной, двумя или тремя гидроксигруппами. Двухатомные фенолы более сильные кислоты, чем одноатомный фенол. Они легко окисляются и являются сильными восстановителями. Пирокатехин при окислении образует о-бензохинон:
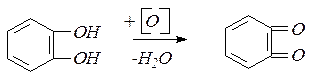
Две структуры – бензоидная и хиноидная – легко переходят друг в друга. Хиноидные группировки относятся к важным хромофорным системам в молекулах красителей.
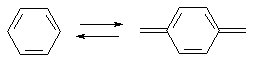
К наиболее характерным химическим свойствам можно отнести следующие.
1. Проявляя кислотные свойства, фенол реагирует с гидроксидом натрия, образуя феноляты:
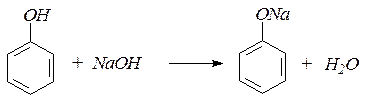
2. Фенолы легко алкилируются при действии на феноляты галогенпроизводных, особенно в присутствии порошка меди, а также при действии на фенол алкилсульфатов, эфиров сульфокислот или диазометана:
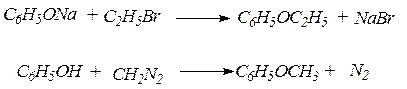
3. Фенол конденсируется с окисью этилена с образованием фенилового эфира полиэтиленгликоля:
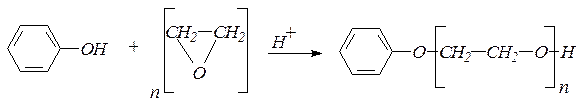
4. фенолы не этерифицируются непосредственно карбоновыми кислотами. Эфиры фенолов могут быть получены действием ангидридов или галогенангидридов кислот на феноляты или растворы фенолов в пиридине:

5. Гидроксильная группа в фенолах с большим трудом замещается на галоген:

6. При перегонке фенолов с цинковой пылью гидроксильная группа замещается на водород:
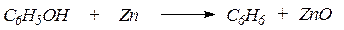
7. Галогенирование фенола действием растворов галогеновили галогенирующих средств идет с большой скоростью и преимущественно в пара-положение. Конечным продуктом галогенирования в ядро являются тригалогенофенолы. Возможно дальнейшее галогенирование:
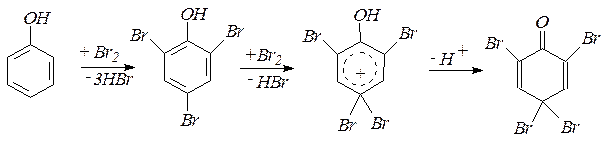
8. Нитрование фенола идет уже при действии разбавленной азотной кислоты.При дальнейшем нитровании концентрированной азотной кислотой получается тринитрофенол – пикриновая кислота:

9. При сульфировании фенолов получаются о- и п-фенолсульфокислоты:
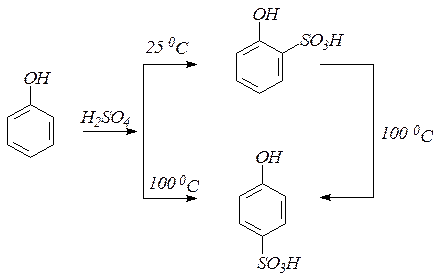
10. Фенолы легко конденсируются с альдегидами:
а) при действии щелочных или кислых катализаторов на смесь фенола и какого-либо альдегида жирного ряда происходит конденсация в о- и п-положениях при обычной температуре рост молекулы за счет конденсации фенола с альдегидом идет в линейном направлении:
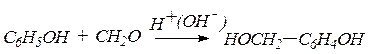
11. При действии на фенол перекиси водорода в присутствии железного катализатора получается с небольшим выходом пирокатехин:
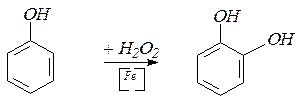
При действии на фенол хромовой смесью образуется п-бензохинон и продукты его дальнейших изменений:

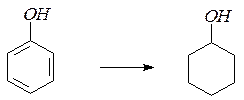
12. При гидрировании водородом в присутствии катализатора фенолы превращаются в спирты ряда циклогексана:
Дата добавления: 2015-09-11; просмотров: 1690;
