ПРОЦЕСС КРИСТАЛЛИЗАЦИИ
Цель работы: ознакомиться с теорией кристаллизации реальных металлов и сплавов на примере изучения процесса кристаллизации солей.
Приборы, материалы, инструменты:
1) биологический микроскоп МБС-10;
2) стекло;
3) растворы солей К2Cr2O7, Pb(NO3)2.
Кристаллизацией называется процесс образования кристаллов как из жидкой фазы (первичная кристаллизация), так и из твердой фазы (вторичная кристаллизация).
При затвердевании могут получаться кристаллы самой разнообразной формы и размеров. Это зависит от условий охлаждения слитка, от того, с какой температурой металл попадает в изложницу и какова была температура перегрева сплава, а также от ряда других факторов.
На рис. 5 представлен график изменения свободной энергии жидкого и твердого состояния в зависимости от температуры. Видно, что любое фазовое состояние вещества (жидкого и твердого) характеризуется определенным значением свободной энергии, зависящей от температуры. Согласно законам термодинамики устойчивым фазовым состоянием вещества при определенных внешних условиях будет то, которое обладает наименьшей свободной энергией, поэтому при температурах ниже 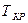 устойчивым будет жидкое состояние, а при температурах ниже
устойчивым будет жидкое состояние, а при температурах ниже 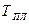 – твердое. При температуре
– твердое. При температуре 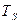 обе фазы оказываются устойчивыми. При некотором охлаждении жидкого вещества ниже
обе фазы оказываются устойчивыми. При некотором охлаждении жидкого вещества ниже 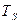 начнется процесс первичной кристаллизации, протекающий в две стадии – образование центров кристаллизации и рост кристаллов.
начнется процесс первичной кристаллизации, протекающий в две стадии – образование центров кристаллизации и рост кристаллов.
Установлено, что число центров кристаллизации, самопроизвольно зарождающихся в металле, и скорость роста кристаллов зависят от скорости охлаждения. При отсутствии переохлаждения, что соответствует температуре 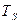 (рис. 5), число центров кристаллизации и скорость роста кристаллов равны нулю и процесс кристаллизации не идет. Чтобы начался процесс кристаллизации, необходимо некоторое переохлаждение.
(рис. 5), число центров кристаллизации и скорость роста кристаллов равны нулю и процесс кристаллизации не идет. Чтобы начался процесс кристаллизации, необходимо некоторое переохлаждение.
Для металлов, вследствие слабой переохлаждаемости жидкостей, на опыте удалось определить лишь восходящие ветви кривых числа центров кристаллизации и скорости роста (рис. 6).
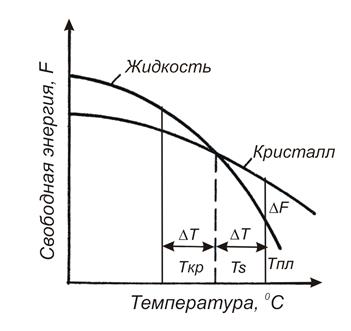
Рис. 5. График изменения свободной энергии жидкого
и твердого состояния в зависимости от температуры.
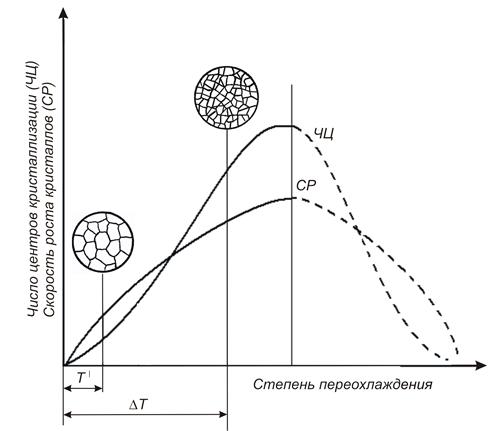
Рис. 6. Влияние степени переохлаждения на число центров
кристаллизации ЧЦ и скорость роста кристаллов СР.
С изменением степени переохлаждения изменяются соотношения числа центров получившихся кристаллов. Так, для двух возможных степеней переохлаждения увеличение скорости роста при увеличении степени переохлаждения меньше, чем увеличение числа центров. При кристаллизации с большими степенями переохлаждения это приводит к получению мелкозернистого кристалла. Значение скорости переохлаждения подтверждается практикой.
В технических металлах и сплавах большое влияние на размер зерна оказывают мельчайшие неметаллические взвеси, образующиеся при взаимодействии жидкого металла с материалом печи или изложницы, окислы металлов, а также окислы, вводимые специально. Все эти нерастворимые включения играют роль центров кристаллизации, способствуя получению мелкозернистого кристалла.
Процесс искусственного регулирования размеров зерна получил название модифицирование, а вещество, которое для этой цели используют, модификатор.
При затвердении стального слитка в изложнице слиток получается неоднородным. Жидкая сталь попадает в изложницу при температуре 1540-1560 0С и сразу же соприкасается со стенками изложницы, имеющими низкую температуру (20-80 0С). Поэтому у стенки изложницы происходит очень быстрое охлаждение металла и образуется плотный слой мелких, различно ориентированных кристаллов. В дальнейшем скорость охлаждения стали уменьшается и рост кристаллов происходит по направлению, перпендикулярному к охлаждению поверхности изложницы. Здесь образуются вытянутые столбчатые кристаллы.
Внутренняя часть слитка охлаждается медленнее, чем наружная, отдача тепла идет в разных направлениях, поэтому во внутренней центральной зоне слитка кристаллы расположены беспорядочно, с произвольным направлением главных осей (рис. 7).
Чаще всего при кристаллизации солей образуется дендритная структура. Дендрит – древовидный кристалл.
Целью данной работы является изучение процесса кристаллизации из жидкого состояния в твердое.
Наблюдение за процессом кристаллизации солей Pb(NO3)2 и K2Cr2O7 ведут с помощью микроскопа и изучают их кристаллизацию, вызванную испарением растворителя капли, откуда и начинается кристаллизация.
Процесс кристаллизации растворителем соли можно условно разделить на три периода.
1. По мере испарения жидкости концентрация раствора изменяется, раствор постепенно переходит в состояние насыщения. Наибольшее испарение будет у краев капли.
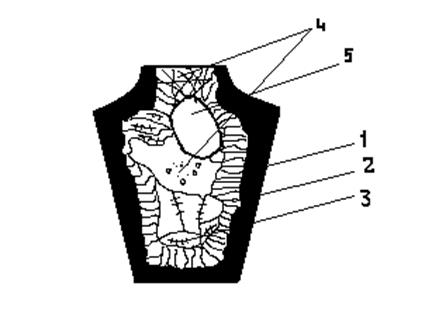
Рис. 7. Схема строения слитка:
1 – мелкозернистая структура; 2 – столбчатые кристаллы; 3 – различно ориентированные кристаллы; 4 – ликвационная зона; 5 – усадочная раковина.
Поэтому в течение первого периода кристаллизации у краев капли образуется корка, состоящая из мелких кристаллов правильной формы, поскольку сильное переохлаждение вызывает большое число зародышей кристаллизации (А) (рис. 8).
2. Во второй период кристаллизации растут крупные, так называемые столбчатые кристаллы (Б). Направление их нормально к краям капли. Здесь мы имеем большую скорость кристаллизации и ограниченное число зародышей.
3. В третий период кристаллизации, когда капля становится тонкой и испарение из середины идет значительно быстрее, возникают новые кристаллы, беспорядочно ориентированные и имеющие ясно выраженную форму дендритов (В).

Рис. 8. Строение затвердевающей капли раствора соли Pb(NO3)2, х 50
Процесс кристаллизации соли весьма схож с процессом затвердения металлического слитка. На аналогии затвердения соли и металлического слитка основана данная лабораторная работа.
Дата добавления: 2015-09-11; просмотров: 3269;
