Розчини електролітів.
Було виявлено речовини, властивості розчинів яких значно відхилялися від законів Рауля і Вант – Гоффа. До таких речовин належать кислоти, основи, солі. Експериментально отримані значення осмотичного тиску, зниження тиску насиченої пари розчинника над розчином, підвищення температури кипіння, зниження температури замерзання для розчинів цих речовин виявилися значно більшими від обчислених за законами Вант – Гоффа та Рауля для розчинів відповідних концентрацій. Молярні маси кислот, основ та солей, визначені на основі результатів експериментальних вимірювань, виявилися меншими, ніж справжні.
Вант – Гофф запропонував ввести емпіричний поправочний множник – ізотонічний коефіцієнт 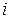 , який визначав би, у скільки разів реальний осмотичний тиск даного розчину
, який визначав би, у скільки разів реальний осмотичний тиск даного розчину 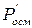 перевищує його значення, обчислене за законом Вант – Гоффа
перевищує його значення, обчислене за законом Вант – Гоффа 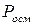 :
:
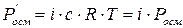
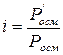
Введення ізотонічного коефіцієнта в рівняння законів Рауля також дає змогу застосувати їх для розбавлених розчинів кислот, основ,солей:
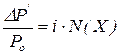
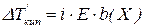
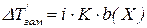
Ізотонічний коефіцієнт обчислюють за співвідношенням:
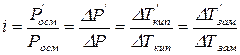
значення 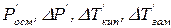 отримані експериментально,
отримані експериментально,
значення  обчислені за законами Вант – Гоффа та Рауля для заданих концентрацій розчинених речовин.
обчислені за законами Вант – Гоффа та Рауля для заданих концентрацій розчинених речовин.
Електроліти – речовини, розчини яких проводять електричний струм. Це розчини кислот, основ, солей. Для їхніх розчинів  .
.
Неелектроліти – речовини, розчини яких не проводять електричний струм. Це розчини сахарози, глюкози, карбаміду, гліцерину, етиленгліколю, тощо. Для їхніх розчинів 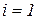 .
.
За однакової молярної концентрації розчиненої речовини осмотичний тиск, зниження тиску насиченої при, підвищення температури кипіння та зниження температури замерзання розчинів електролітів завжди більші, ніж розчинів неелектролітів.
Дата добавления: 2015-09-02; просмотров: 886;
