ГЛАВА 18. измененная форма гена токсина
измененная форма гена токсина. Такой ген содержал кодоны, чаще используемые растениями по сравнению с теми, которые «предпочитают» грамположительные бактерии. Были внесены также изменения, предотвращающие образование вторичной структуры у мРНК или исключающие появление сайтов полиаденилирования, характерных для растений, что могло бы снизить уровень экспрессии. GС-содержание «полностью» измененного гена было равно 49% (для гена дикого типа эта величина составляла 37%), а нуклеотидная последовательность была только на 78,9% гомологична таковой гена дикого типа.
Трансгенные растения, трансформированные сильно измененным геном протоксина, синтезировали в 100 раз больше токсина, чем растения, трансформированные геном дикого типа, при этом наблюдалась прямая корреляция с увеличением инсектицидной активности. Полученные данные позволяют надеяться, что аналогичным образом удастся повысить уровень экспрессии в растениях множества других чужеродных генов.
Количество синтезируемого в растениях протоксина попытались увеличить, осуществив экспрессию «полностью» измененного гена протоксина под контролем промотора гена малой субъединицы рибулозобисфосфат-карбоксилазы, помещенного после хлоропластной сигнальной последовательности этого фермента, таким образом, чтобы сверхпродуцируемый протоксин был локализован в хлоропластах. Эта стратегия привела к радикальному повышению уровня экспрессии гена протоксина, так что на долю протоксина стало приходиться до 1 % всех белков листа. В другом эксперименте ген протоксина вводили непосредственно в хлоропластную ДНК растения-хозяина. Это дает следующие преимущества. Во-первых, вводимый ген не нужно модифицировать, поскольку транскрипционный и трансляционный аппараты хлоропластов относятся к прокариотическому типу. Во-вторых, на одну клетку приходится много хлоропластов, а на один хлоропласт — много копий хлоропластной ДНК, поэтому ген протоксина присутствует в большом числе копий, и эффективность его экспрессии повышается. В-третьих, хлоропласты передаются только через яйцеклетку, а не через пыльцу, так что растения наследуют хлоропластную ДНК по материнской линии и нет никакого риска нежелательного переноса гена лротоксина с пыльцой на другие растения.
Одна из форм гена протоксина уже введена и экспрессируется в таких растениях, как томаты, табак, картофель, рис, кукуруза, яблоня, баклажан, канола, люцерна, орех, тополь, ель, клюква и хлопок. Перспективы применения этого метода защиты растений кажутся весьма обнадеживающими. Так, в трансгенных растениях картофеля осуществлена эффективная экспрессия синтетического гена на основе гена инсектицидного токсина В. thuringiensis ssp. tenebrionis с кодовым словарем, используемым растениями. Полученные растения оказались высокоустойчивыми к колорадскому жуку, основному вредителю картофеля. Уже проведены успешные полевые испытания культуры в течение нескольких лет и получено разрешение на коммерческое ее использование в США. Следует помнить, однако, о необходимости постоянного контроля популяции насекомых-вредителей, с тем чтобы вовремя обнаружить устойчивые организмы. Возможно, в будущем для защиты трансгенного картофеля придется использовать более мощный протоксин В. thuringiensis или, что более вероятно, идентифицировать и клонировать в растениях другие инсектицидные гены в дополнение к генам протоксинов В. thuringiensis.
В настоящее время разрабатываются способы сниженияь селективного давления со стороны трансгенных растений, экспрессирующих ген протоксина В. thuringiensis, на устойчивых насекомых-вредителей. В одном случае экспрессию гена В. thuringiensis в трансгенном растении ограничивали по времени. Для этого его помешали под контроль промотора гена табака PR-la (от англ, pathogenesis-related), экспрессия которого представляет собой часть естественного механизма защиты табака от болезнетворных организмов. Ген PR-la индуцируется любым патогенным организмом или химическим агентом типа салициловой или полиакриловой кислоты. Обработав трансгенные растения, несущие ген протоксина В. thuringiensis под контролем PR-la-промотора, химическим индуктором, обнаружили, что они синтезируют инсектицид в
Генная инженерия растений: применение 393
заметном количестве в течение 1 сут после обработки, и этого достаточно для последующей защиты растений от насекомых-вредителей. Таким образом, можно индуцировать синтез протоксина, обработав трансгенное растение недорогим и безопасным химическим веществом в определенный момент вегетационного периода. Такая периодичность синтеза протоксина приводит к снижению селективного давления на устойчивых насекомых. Аналогичные системы могут оказаться полезными для регуляции синтеза самых разных чужеродных белков в трансгенных растениях.
Ни один из конкретных типов протоксина В. thuringiensis не может быть эффективным в отношении всех видов насекомых, В ходе эволюции растения выработали общие механизмы защиты от насекомых, обеспечивающие их выживание, однако степень этой защиты не всегда достаточна. Некоторые растения синтезируют ингибиторы протеиназ, которые, попадая в кишечник насекомого, блокируют гидролиз растительных белков. Разумно было предположить, что если выделить растительный ген ингибитора протеиназ и снабдить его сильным промотором, то можно будет создать трансгенные сельскохозяйственные культуры, способные синтезировать ингибитор протеиназ в количестве, достаточном для защиты от насекомых-вредителей. В одном из таких экспериментов с помощью химически синтезированного ДНК-зонда из банка клонов комплементарной ДНК (кДНК) был выделен клон, кодирующий ингибитор трипсина вигны китайской. (При синтезе ДНК-зонда руководствовались аминокислотной последовательностью этого белка.) Полноразмерную кДНК субклонировали в бинарном векторе на основе Ti-плазмиды (рис. 18.2) и ввели в штамм A. tumefaciens, содержащий неонкогенную Ti-плазмиду с активными vir-генами. После инфицирования листовых дисков табака A. tumefaciens этим вектором клетки, содержащие комплементарную ДНК, отбирали по способности к росту в присутствии канамицина и регенерировали из них трансгенные растения. Ущерб, наносимый личинками Heliothis virescens (совки) трансгенным растениям, синтезирующим более 2 мкг ингибитора трипсина на 1 мг растительного белка, был значительно меньше, чем в случае обычных растений.
|
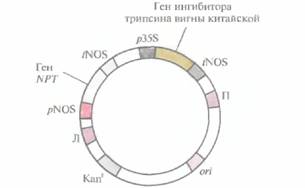
| Рис. 18.2. Бинарный клонирующий вектор, несуший ген ингибитора трипсина вигны китайской. Вектор содержит сайт инициации репликации ДНК для широкого круга хозяев (ori) и ген устойчивости к канамицину (Kanr), который функционирует как в Е. coli, так и в A. tumefaciens. Между правой (П) и левой (Л) фланкирующими последовательностями Т-ДНК находятся: 1) ген неомицинфосфогрансферазы (NPT) под контролем элементов регуляции транскрипции гена нопалинсинтазы (pNOS и tNOS), что позволяет проводить отбор канамицинустойчивых трансформированных растительных клеток; 2) ген ингибитора трипсина вигны китайской, находящийся под контролем 35S-промотора (p35S) вируса мозаики цветной капусты и сигнала терминации транскрипции/полиаденилирования гена нопалинсинтазы (tNOS). |
Семена вигны китайской, содержащие указанное выше количество ингибитора, нетоксичны для животных и человека. Впрочем, если бы такая опасность и существовала, можно было бы ограничить экспрессию гена ингибитора теми тканями растения, которыми предпочитают питаться основные насекомые-вредители, но которые не используют в пищу человек и животные. Так, клонированный ген ингибитора протеиназ мог бы «работать» в листьях и корнях растения, но не в его плодах.
Введение гена ингибитора 11протеиназы картофеля в растения риса защищает их от розового стеблевого точильщика (Sesamia inferens), основного насекомого-вредителя для этой культуры; заражение приводит к образованию полых стеблей и мертвых метелок без семян. Была сконструирована плазмида, содержащая ген ингибитора II протеиназы картофеля под контролем его собственного промотора и сигнала терминации транскрипции. Между промотором и кодирующей областью гена ингибитора был
394 ГЛАВА 18
|
| Рис. 18.3. Плазмидный вектор, несущий ген ингибитора II протеиназы картофеля. Обозначения: Pin2— ген ингибитора II протеиназы картофеля; 5'-конец - сегмент ДНК, предшествующий данному гену; 3'-конец - сегмент ДНК, следующий за геном; интрон Act1 — первый интрон гена актина 1 риса; 35S 5'-конец — 35S-промотор вируса мозаики цветной капусты; bar- бактериальный ген фосфинотрицин-ацетилтрансферазы; nos 3'-конец - сегмент ДНК, следующий за геном нопалинсинтазы. Ген bar служит селективным маркером для трансгенных растений, обусловливая устойчивость к гербициду Basta (глюфозинату аммония). |
встроен первый интрон гена актина риса. Эту конструкцию ввели в суспендированные клетки риса методом бомбардировки микрочастицами (рис, 18,3) и регенерировали из них трансгенные растения. Когда личинок розового стеблевого точильщика наносили на полученные таким образом растения, только от 15 до 20% последних оказывались поврежденными, в то время как для растений дикого типа эта величина составляла 70—100%. Поскольку растительные ингибиторы протеиназ являются обычными компонентами рациона человека и животных и в процессе приготовления пищи быстро инактивируются, их введение в новые зерновые культуры можно считать безопасным.
Другой подход к увеличению эффективности защиты растений с помощью токсина В. thuringiensis основан на параллельном использовании этого токсина и ингибитора сериновой протеиназы. Показано, что смесь очищенного токсина В, thuringiensis вколичестве, обеспечивающем минимальную смертность насекомых, и ингибитора протеиназ в низких концентрациях обладает в 20 раз большей инсектицидной активностью, чем один протоксин В. thuкingiensis. Чтобы проверить, будет ли эта система функционировать в трансгенных растениях, был сконструирован фрагмент ДНК, кодирующий гибридный белок «ингибитор протеиназ/укороченный токсин». Трансгенные растения табака, которые синтезировали небольшие количества такого рекомбинантного белка, были в значительной мере защищены от насекомых-вредителей.
Еще один способ защиты растений предполагает введение в них гена, кодирующего ингибитор α-амилазы. Большой ущерб зерновым приносят такие насекомые, как зерновка (Callosobruchus maculatus) и долгоносик лучистой фасоли (С. chinensis), шггающиеся семенами. Если в рацион личинок этих насекомых включить обычную фасоль (Phaseolus vulgaris), то рост насекомых замедляется. Это связано с присутствием в семенах обычной фасоли ингибитора α-амилазы. Ген ингибитора α-амилазы, выделенный из обычной фасоли, был помещен под транскрипционный контроль сильного семяспецифичного промотора гена фитогемагглютинина бобов и использован для трансформации гороха (Pisum sativum), обычно весьма чувствительного к упомянутым выше насекомым. Трансгенные растения гороха, которые синтезировали ингибитор α-амилазы, были устойчивы к обоим насекомым, при этом в случае зерновки эффект оказался пропорциональным количеству ингибитора, синтезированному растением (рис. 18.4).
Альтернативный подход к выведению трансгенных растений, устойчивых к насекомым, основан на использовании бактериального гена холестеролоксидазы. Этот фермент, синтезируемый различными бактериями, катализирует окисление 3-гидроксистероидов с образованием кетостероидов и пероксида водорода. Его часто используют при определении уровня холестерола в сыворотке крови у человека, а в небольших количествах он проявляет высокую инсектицидную активность против личинок хлопкового долгоносика (Anthonomus grandis grandis) (рис. 18.5). Это широко распространенное насекомое отряда жесткокрылых наносит ощутимый ущерб хлопковым плантациям. В отношении насекомых-вредителей отряда чешуекрылых холестеролоксидаза менее эффективна. Действие фермента, по-видимому, заключается в разрушении мембраны эпителиальных клеток средней кишки насекомого, что приводит к его гибели. Ген
Генная инженериярастений: применение 395
| Рис. 18.4. Зависимость смертности личинок зерновки, развивающихся на трансгенных растениях гороха, от количества ингибитора α-амилазы, синтезируемого растениями. | 
|
| Рис. 18.5. Зависимость смертности личинок хлопкового долгоносика от концентрации холестеролоксилазы. (Corbin et al., Appl. Environ. Microbiol. 60: 4239-4244, 1994.) | 
|
холестеролоксидазы, кодирующий белок мол. массой 55 000 Да (504 аминокислотных остатка) и лидерный пептид мол. массой 5000 Да (43 аминокислотных остатка), был выделен из штамма Streptomyces и встроен в вектор вместе с промотором вируса мозаики норичника шишковатого и сигналом терминации из 3'-области гена нопалинсинтазы A. tumefaciens. Когда такую конструкцию ввели в протопласты клеток табака, трансформированные клетки стали активно экспрессировать холестеролоксидазу. В будущем, вероятно, этот ген будет введен в растения хлопка, и тогда — либо самостоятельно, либо в комбинации с генами других биологических инсектицидов -он станет эффективным инструментом защиты растений от насекомых-вредителей.
Растения, устойчивые к вирусам
Вирусы растений часто причиняют значительный ущерб растениям и существенно снижают урожай. Чтобы не прибегать к обработке культур химическими препаратами, селекционеры попытались перенести природные гены устойчивости к вирусам от одной линии растений к другой. Однако устойчивые растения часто вновь становятся чувствительными, а устойчивость к одному вирусу не гарантирует устойчивости к другим. Природный иммунитет к вирусным инфекциям обусловливается разными причинами: блокированием проникновения вируса в растение, предотвращением его распространения, подавлением симптомов вирусной инфекции.
Дата добавления: 2015-07-14; просмотров: 923;
