Атомное ядро. Дефект массы. Энергия связи атомного ядра
Атомное ядро – это центральная часть атома, в которой сосредоточен весь положительный заряд и почти вся масса.
Ядра всех атомов состоят из частиц, которые называются нуклонами. Нуклоны могут быть в двух состояниях – в электрически заряженном состоянии и в нейтральном состоянии. Нуклон в заряженном состоянии называется протоном. Протон (р) – это ядро самого легкого химического элемента – водорода. Заряд протона равен элементарному положительному заряду, который по величине равен элементарному отрицательному заряду qe = 1,6 ∙ 10-19 Кл., т.е. заряду электрона. Нуклон в нейтральном (незаряженном) состоянии называют нейтроном (n). Массы нуклонов в обоих состояниях мало отличаются друг от друга, т.е. mn ≈ mp.
Нуклоны не являются элементарными частицами. Они обладают сложной внутренней структурой и состоят из еще более мелких частиц материи – кварков.
Основными характеристиками атомного ядра являются заряд, масса, спин и магнитный момент.
Заряд ядра определяется количеством протонов (z), входящих в состав ядра. Заряд ядра (zq) для разных химических элементов различен. Число z называют атомным номером или зарядовым числом. Атомный номер является порядковым номером химического элемента в периодической системе элементов Д.Менделеева. Заряд ядра определяет и количество электронов в атоме. От количества электронов атома зависит их распределение по энергетическим оболочкам и подоболочкам и, следовательно, все физико-химические свойства атома. Заряд ядра определяет специфику данного химического элемента.
Масса ядра Масса ядра определяется количеством (А) нуклонов, которые входят в состав ядра. Число нуклонов в ядре (А) называется массовым числом. Число нейтронов (N) в ядре можно найти если от общего числа нуклонов (А) отнять число протонов (z), т.е N=F-z. В периодической таблице до ее середины количество протонов и нейтронов в ядрах атомов примерно одинаково, т.е. (А-z)/z= 1, к концу таблицы (А-z)/z= 1,6.
Ядра атомов принято обозначать так: 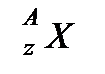
X - символ химического элемента;
Z – атомный номер;
A – массовое число.
При измерении масс ядер простых веществ было обнаружено, что большинство химических элементов состоят из групп атомов. Имея одинаковый заряд, ядра различных групп отличаются массами. Разновидности атомов данного химического элемента, отличающегося массами ядер, назвали изотопами. Ядра изотопов имеют одинаковое число протонов , но разное число нейтронов ( 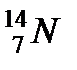 и
и 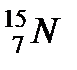 ;
; 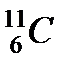 ,
, 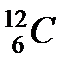 ,
, 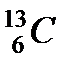 ,
, 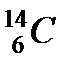 ;
; 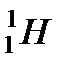 ,
, 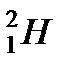 ,
, 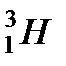 ).
).
Кроме ядер изотопов (z – одинаково, А – различно) существуют ядра изобары (z - различно, А – одинаково). ( 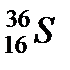 и
и 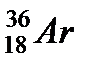 ).
).
Массы нуклонов, ядер атомов, атомов, электронов и других частиц в ядерной физике принято измерять не в «КГ», в атомных единицах массы (а.е.м. – иначе называют углеродной единицей массы и обозначают «е»). За атомную единицу массы (1е) принята 1/12 массы атома углерода 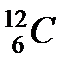 1е=1,6603 ∙ 10-27кг.
1е=1,6603 ∙ 10-27кг.
Массы нуклонов: mp -1.00728 e, mn =1,00867 е.
Видим, что масса ядра выраженная в «е» будет записываться числом близким к А.
Спин ядра. Механический момент импульса (спин) ядра равен векторной сумме спинов нуклонов, составляющих ядро. Протон и нейтрон обладают спином равным L = ± 1/2ћ. В соответствии с этим спин ядер с четным числом нуклонов (А четное) является целым числом или нулем. Спин ядра с нечетными числом нуклонов (А нечетное) является полуцелым.
Магнитный момент ядра. Магнитный момент ядра(Pmя) ядра по сравнению с магнитным моментом электронов, заполняющих электронные оболочки атома, очень мал. На магнитные свойства атома магнитный момент ядра не влияет. Единицей измерения магнитного момента ядер является ядерный магнетон μя = 5,05,38 ∙ 10-27 Дж/Тл. Он в 1836 раз меньше магнитного момента электрона – магнетона Бора μБ = 0,927 ∙ 10-23 Дж/Тл.
Магнитный момент протона равен 2,793 μя и параллелен спину протона. Магнитный момент нейтрона равен 1,914 μя и антипараллелен спину нейтрона. Магнитные моменты ядер имеют порядок ядерного магнетона.
Чтобы расщепить ядро на составляющие его нуклоны надо совершить определенную работу. Величина этой работы является мерой энергии связи ядра.
Энергия связи ядра численно равна работе, которую надо совершить для расщепления ядра на составляющие его нуклоны и без сообщения им кинетической энергии.
При обратном процессе образования ядра из составляющих нуклонов должна выделяться такая же энергия. Это следует из закона сохранения энергии. Поэтому энергия связи ядра равна разности энергии нуклонов, составляющих ядро, и энергии ядра:
ΔЕ = Енук – Ея. (1)
Учитывая взаимосвязь массы и энергии (Е = m ∙ c2) и состав ядра, уравнение (1) перепишем так:
ΔЕ = [zmp +(A-z)mn – Mя] ∙ с2 (2)
Величина
Δm = zmp +(A-z)mn – Mя , (3)
Равная разности масс нуклонов, входящих в состав ядра, и массы самого ядра, называется дефектом массы.
Выражение (2) можно переписать в виде:
ΔЕ = Δm ∙ с2 (4)
Т.е. дефект массы является мерой энергии связи ядра.
В ядерной физике массу нуклонов и ядер измеряют в а.е.м. (1 а.е.м.=1,6603 ∙ 1027кг), а энергию принято измерять в МэВ.
Учитывая, что 1 МэВ = 106 эВ = 1,6021 ∙ 10-13 Дж, найдем величину энергии, соответствующей атомной единице массы
1.а.е.м. ∙ с2 = 1,6603 ∙10-27 ∙9 ∙1016 = 14,9427 ∙ 10-11Дж = 931,48 МэВ
Таким образом, энергия связи ядра в МэВ равна
ΔЕсв= Δm ∙931,48 МэВ (5)
Учитывая, что в таблицах обычно дается не масса ядер, а масса атомов, для практического вычисления дефекта массы вместо формулы (3)
пользуются другой
Δm = zmН +(A-z)mn – Mа , (6)
Т.е массу протона заменили массой атома легкого водорода 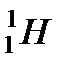 , добавив тем самым z электронных масс, а массу ядра заменили массой атома Mа, этим самым вычли эти z электронных масс.
, добавив тем самым z электронных масс, а массу ядра заменили массой атома Mа, этим самым вычли эти z электронных масс.
Энергию связи, приходящуюся на один нуклон в ядре, называют удельной энергией связи
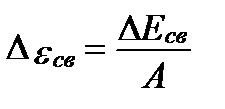 (7)
(7)
Зависимость удельной энергии связи от числа нуклонов в ядре (от массового числа А) дана на рис.1.

Рис.1.
Анализ графика показывает:
1. Нуклоны прочнее связаны в ядрах элементов средней части периодической таблицы (30<А< 100), для этих ядер 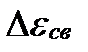 ≈8,7 МэВ.
≈8,7 МэВ.
2. У ядер с массовым числом А > 100 удельная энергия связи с ростом числа нуклонов (А) уменьшается; для ядер конца периодической таблицы 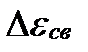 ≈7,5 МэВ.
≈7,5 МэВ.
3. У ядер с массовым числом А < 30 удельная энергия связи с уменьшением числа нуклонов (А) уменьшается; для ядер начала периодической таблицы 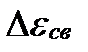 ≈ 1 - 3 МэВ.
≈ 1 - 3 МэВ.
4. У легких ядер удельная энергия связи обнаруживает характерные максимумы и минимумы: 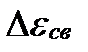 у нечетно-нечетных ядер (
у нечетно-нечетных ядер ( 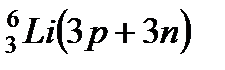 ,
, 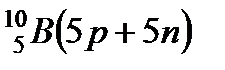 ); максимум у четно-четных ядер (
); максимум у четно-четных ядер ( 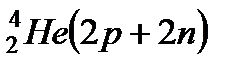 ,
, 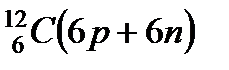 ).
).
Проведенный анализ графика показывает, что легчайшим ядрам энергетически выгодно сливаться друг с другом в более тяжелые (возрастает энергия). Наиболее тяжелым ядрам, наоборот, энергетически выгоден процесс деления на осколки (более легкие ядра)
Тема 17. Радиоактивное излучение
Дата добавления: 2015-08-11; просмотров: 2916;
