Термические превращения компонентов нефти при газофазном крекинге
В термических, а также каталитических процессах нефтепереработки одновременно и совместно протекают как эндотермические реакции крекинга (распад, дегидрирование, деалкилирование, деполимеризация, дегидроциклизация), так и экзотермические реакции синтеза (гидрирование, алкилирование, полимеризация, конденсация) и частично реакции изомеризации с малым тепловым эффектом. Об этом свидетельствует то обстоятельство, что в продуктах термолиза (и катализа) нефтяного сырья всегда содержатся углеводороды от низкомолекулярных до самых высокомолекулярных: от водорода и сухих газов до смолы пиролиза, крекинг-остатка и кокса или дисперсного углерода (сажи). В зависимости от температуры, давления процесса, химического состава и молекулярной массы сырья возможен термолиз с преобладанием или реакций крекинга, как, например, при газофазном пиролизе низкомолекулярных углеводородов, или реакций синтеза как в жидкофазном процессе коксования тяжелых нефтяных остатков.
Термическая деструкция углеводородов — это их pacщепление, распад на части под действием температур. Однако при термической деструкции в интервале температур 500—900°С протекают не только реакции распада вещества (1), но одновременно имеют место и реакции его синтеза (II). Условно эти реакции можно разделить на следующие основные группы:
| І | Реакции распада веществ | ІІ | Реакции синтеза веществ |
| Распад | Конденсация | ||
| Дегидрирование | Полимеризация | ||
| Деалкилирование | Алкилирование | ||
| Дециклизация | Циклизация непредельных углеводородов |
Все реакции разложения (I) и соединения (II) — равновесные и характеризуются изменением числа молекул в ходе реакции. Это обусловливает сильное влияние концентраций реагентов или давления в системе на скорость реакции и на положение равновесия.
Реакции группы І протекают с увеличением объёма системы, числа молекул в ходе реакции и поглощением тепла. Очевидно, что для того, чтобы разорвать химические связи в молекуле (реакции этой группы – это реакции деструкции молекулы). Необходимо затратить некоторое количество энергии (например, тепловой). Таким образом, реакции первой группы – это эндотермические реакции. Часто вместо одного объёма исходного вещества образуется два объёма веществ-продуктов. Иногда конечный объём системы увеличивается многократно. Например, реакции крекинг и дегидрирования циклогексана:
С20 Н42 → С10Н22 + С10Н20
С6Н12 → С6Н + 3Н2
Реакции группы ІІ идут с уменьшением объёма и числа молекул в ходе реакции. Эти реакции можно отнести к реакциям синтеза вещества. Реакции соединения сопровождаются выделением энергии. Причина в том, что в ходе реакции синтеза разрываются менее прочные связи и образуются более прочные. Реакции второй группы являются экзотермическими реакциями. Например, реакции полимеризации бутена:
3С4Н8 → С12Н24
Для процессов, связанных с выделением или поглощением тепла, влияние температуры на изменение свободной энергии системы характеризуется принципом Ле-Шателье. Согласно правилу Ле-Шателье при увеличении температуры для экзотермических реакций смещается влево и вправо для эндотермических. Следовательно, для эндотермических реакций необходимо повышать температуру, а для эндотермических реакций температуру следует понижать. Это означает, что термодинамическая вероятность протекания реакций возрастает в эндотермических реакциях крекинга с повышением температуры, а в экзотермических реакциях синтеза - наоборот, при понижении температуры. По этому признаку реакции крекинга являются термодинамически высокотемпературными, а синтеза - термодинамически низкотемпературными.
Поскольку реакции обеих групп протекают с изменением объёма, то изменение внешнего давления имеет большое значение. Увеличение давления для реакций, идущих с уменьшением объёма, приводят к смещению равновесия вправо. Напротив, для реакций распада или других реакций протекающих с увеличением объёма. Сдвиг равновесия вправо происходит при понижении давления. Однако, несмотря на то. Что при термическом крекинге объём системы увеличивается, процесс ведут при повышенном давлении (≥5, 0 Мпа). Это позволяет подавлять реакции глубокого распада, приводящие к повышенному газообразованию, т.е. получению побочного нецелевого продукта. При термическом крекинге выход жидких целевых продуктов составляет около 70% мас., а газа – около 15% мас. Если же целью является получение газообразных продуктов, давление процесса снижают, как, например, в случаи парофазного крекинга (0.2-03 Мпа, выход газа порядка 30%), или пиролиза (1.0 – 1.2 Мпа, выход газа около 60%).
Для реакций, протекающих без изменения объема, таких, как изомеризация или замещение, давление не оказывает влияния на их равновесие.
Энергия связей
Для прогнозирования вероятности образования того или иного продукта реакций в термодинамике пользуются данными по энергиям связи в химических веществах.
Энергией связи называется количество энергии, необходимое для разрыва или образования определенного типа связи между атомами в молекулах. При возникновении связи происходит переход химической системы в более устойчивое состояние, сопровождающееся выделением тепла. Следовательно, энергия образования связи положительна. При распаде молекул тепло поглощается, и энергия разрыва связи отрицательна.
Из сопоставительного анализа данных, приведенных в табл.1, можно сформулировать некоторые качественные выводы о влиянии структуры и массы молекул углеводородов на величину энергий разрыва связей между атомами углерода, углерода с водородом и углерода с серой.
Таблица №1
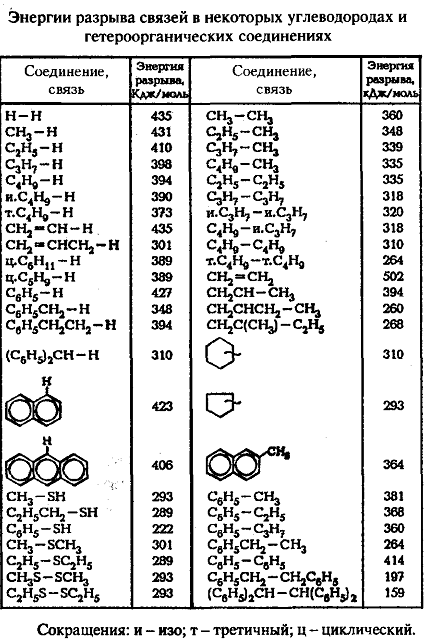
Из таблицы видно, что наименьшей энергией связи обладает связь углерод-гетероатом, следовательно, на её разрыв необходимо затратить наименьшее количество энергии. При термическом воздействии эта связь будет разрываться первой. Следом будут разрываться связи углерод- углерод в парафинах (распад), нафтенах (дециклизация), будут отрываться боковые цепи в ароматических молекулах (деалкилирование). Самыми прочными углерод- углеродными связями являются ароматические и ацетиленовые связи. Именно поэтому в термических процессах одним из продуктов реакции являются конденсированные ароматические системы. Получающиеся по реакции конденсации ароматических и циклизации непредельных углеводородов (кокс, смола пиролиза, тяжёлые смолы парофазного и жидкофазного крекинга).
Неравноценны связи одного типа в пределах одной молекулы. Например, для высокомолекулярных парафиновых углеводородов разорвать цепь в середине молекулы проще, чем разрывать углерод углеродную связь в конце молекулы. Это же относится к связям С-Н в молекулах углеводородов. Так для отрыва первого атома Н от молекулы метана требует больше энергии, чем для отрыва последующих водородных атомов.
Таким образом, на величину энергии связи влияет не только принадлежность к тому или иному гомогилогическому ряду, но и строение молекулы, и местонахождение данной связи в молекуле.
Из вышесказанного можно сделать следующие выводы.
В реакциях углеводородов отрыв водорода всегда легче происходит от
третичного атома углерода, труднее от вторичного, ещё труднее от первичного. Наименьшая вероятность отрыв характерна для метана.
Основные типы углеводородов нефти можно расположить по термической стабильности в следующий возрастающий ряд:
нормальные алканы < разветвленные алканы < нафтены < ароматические углеводороды < полициклические углеводороды.
Основные положения механизма термических реакций нефтяного сырья
При гомолитическом разрыве пара электронов, принадлежащая ранее двум связываемым атомам, поровну распределяется между ними:
Y – X →Y' + 'X
где Y-X — валентно-насыщенная молекула; Y', 'X — два свободных радикала.
СН3°- СН3°↔ СН3° + СН3°
СН3 -СН2°°Н ↔ СН3-СН2° + °Н
Гомолитический разрыв происходит чаще всего при термических превращениях углеводородов.
Гетеролитический разрыв приводит к образованию ионов. Связь разрывается так, что пара электронов связи целиком переходит к одному из атомов, образующих связь:
СН3°- СН3° ↔(СН3°°)- + СН3+
Гомолитический разрыв энергетически выгодней, чем гетеролитический. Гетеролитический разрыв атомов углеводородов происходит только при каталитических реакциях углеводородов.
Радикалы, являясь химически ненасыщенными частицами, обладают исключительно высокой реакционной способностью и мгновенно вступают в различные реакции.
Радикалы высокой молекулярной массы термически нестабильные и распадаются с образованием низкомолекулярного более устойчивого радикала, в том числе водородного:
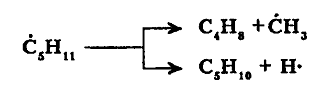
Концентрация радикалов в реакционной системе обычно невелика, и вероятность их столкновения между собой ничтожно мала. При термолизе более значительно преобладают взаимодействия между радикалом и молекулами исходного сырья. Поскольку радикал имеет свободный неспаренный электрон, то его реакция с молекулами, все электроны которых спарены, должна в силу принципа неуничтожимости свободной валентности привести к образованию нового вторичного радикала. Если последний не является малоактивным, то он, в свою очередь, вступит в реакцию с новой молекулой сырья и т.д. Так как число радикалов, могущих образоваться при термолизе, велико, на некоторой стадии образуется радикал, принимавший участие в одной из предыдущих стадий, и возникает регулярное чередование двух или более последовательно параллельных элементарных реакций с образованием конечных продуктов. Этот процесс продолжится до тех пор, пока радикал не «погибнет». Реакции такого типа называются цепными.
1.Зарождение цепи (образование свободных радикалов).
При термическом распаде всех алканов, начиная с этана, зарождение цепи происходит в результате разрыва связи С – С. При этом образуются свободные радикалы:
СН3-СН2- СН3 → СН3-СН2°+ СН3°
В случаи алканов с большими числом атомов углерода при не очень высоких температурах крекинга (350-450°С), разрыв углеродной цепи происходит посередине, т.е. по наиболее слабым связям С – С. При более высоких температурах могут рваться и другие С – С связи. Значительно менее вероятен при зарождении цепи разрыв С-Н связей углеводородов, и он возможен только для низших алканов (этан, пропан) при соударении молекул со стекой реактора при высоких температурах. Так как молекулы атома водорода являются внешними атомами в молекулах, то при соударении со стенкой реактора может произойти отрыв атома водорода:
СН3- СН2│Н → СН3-СН2° +Н°
2. Продолжение цепи (реакции свободных радикалов).
Свободные радикалы обладают высокой реакционной способностью, так как содержат неспаренный электрон. Поэтому они стремятся стабилизироваться и подвергаются различным превращениям. Реакции радикалов с молекулами углеводородов являются основными, приводящими к развитию цепи.
Низшие свободные радикалы (атомарный Н, СН3°, С2Н5°) при столкновении с молекулами алканов отбирают у них атомы водорода.
СН3° + СН3-СН2- СН3 → СН4 + СН3-СН°- СН3
СН3-СН2° + СН3-СН2- СН3 → СН3- СН3 + СН3-СН°- СН3
СН3-СН2° → СН2 = СН2 + Н°
СН3-СН°- СН3 → СН3 = СН - СН3 + Н°
СН3-СН2- СН3 + Н° → СН3-СН°- СН3 + Н2
3. Обрыв цепи. Квадратичный обрыв происходит при взаимодействии двух радикалов. Он характерен для жидкофазных реакций.
СН3°+ СН3° → СН3 - СН3
СН3° + СН3-СН2° → СН3-СН2- СН3
Линейный обрыв цепи чаще встречается при газофазных реакциях. Он происходит при адсорбции свободных радикалов на стенки или другой твёрдой поверхности либо на ингибиторах.
Ингибиторы – вещества, приводящие к гибели активных радикалов по различным механизмам.
СН3 – СН =СН2 + СН3° → СН4 + СН2° - СН = СН2
СН3 СН3
l l
СН3° + СН - СН3 → СН4 + СН2 - С°
l l
СН3 СН3
В случаи олефина стабилизация радикала происходит за счёт эффекта сопряжения двойной связи, а в случаи изопарафина – индукционного эффекта метильных групп.
Термолиз алканов приводит преимущественно к образованию более термостойких низкомолекулярных алкенов и алканов. Из алканов наибольшей термостабильностью обладает метан. Его термическая деструкция термодинамически возможна при температуре выше 560 °С. С заметной скоростью распад метана протекает при температуре выше 1000°С. Высокая термостабильность метана объясняется тем, что в его молекуле отсутствуют связи С-С, энергия разрыва которых меньше, чем для связей С-Н. При высокотемпературном пиролизе метана, кроме водорода (и пироуглерода), образуются этилен, этан, ацетилен и арены. Синтез этих продуктов можно выразить следующей схемой:

Ароматические углеводороды образуются в результате вторичных реакций синтеза из ацетилена и этилена.
Этан менее устойчив, чем метан: его деструкция начинается при температуре = 500°С. При пиролизе этана образуются преимущественно этилен и водород, а также метан и жидкие продукты, богатые аренами и алкенами.
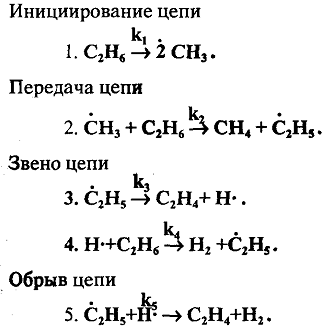
Чередование элементарных реакций (3) и (4) даёт реакцию распад этан по стереохимическому уравнению:
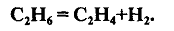
Пропан и бутан термически менее устойчивы, чем этан. Пропан начинает разлагаться при 460 °С, а н-бутан и изобутан - около 435°С. Основные направления пиролиза пропана:
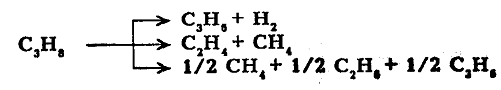
Начиная с бутана, при термолизе алканов преобладающим становится распад по связи С-С. Относительная скорость их термолиза возрастает с увеличением молекулярной массы, что обусловливается уменьшением энергии разрыва С-С-связей по мере приближения к середине цепи и увеличения степени разветвленности молекул.
В процессе пиролиза н-бутана преобладают следующие 2 реакции его распада:
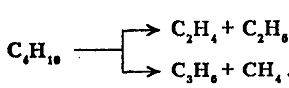
Характерно, что чем выше температура пиролиза бутана, тем больше отодвигается место его распада по С-С-связи к краю молекулы. На это указывает непрерывное возрастание содержания метана в газообразных продуктах реакции вплоть до 900°С. Аналогичные реакции распада характерны для термолиза более высокомолекулярных алканов. Для них при умеренных температурах (400 - 500 °С) наблюдается симметричный разрыв молекулы с образованием олефина и парафина приблизительно одинаковой молекулярной массы. При более высоких температурах в продуктах их термолиза обнаруживаются низшие алканы и высокомолекулярные алкены и арены, вероятно, как результат вторичных реакций.
Алкены характеризуются ввиду наличия двойной связи высокой реакционной способностью в реакциях присоединения, но повышенной, по сравнению с алканами, термостойкостью в отношении реакций распада. Этилен из алкенов наиболее устойчивый. Он всегда содержится в продуктах термолиза нефтяного сырья как первичный и вторичный продукт их превращений. По термической стабильности он занимает промежуточное положение между метаном и этаном. Термический распад этилена заметно начинается при температуре 660 °С. При 400 - 600°С в основном протекает его полимеризация:

В тех же условиях в продуктах пиролиза этилена содержатся высокомолекулярные олефины - продукт сополимеризации бутиленов с этиленом. При температурах 600°С и выше в продуктах термолиза этилена появляются бутадиен и водород в результате дегидрирования бутена-1.
Оптимальная температура образования диенов при пиролизе этилена - 750 °С. При температурах выше 900°С бутадиен в продуктах пиролиза исчезает, вероятно, превращаясь по диеновому синтезу в арены:
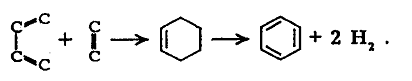
Пропилен по термической стабильности уступает этилену и при термолизе образует метан и этилен:
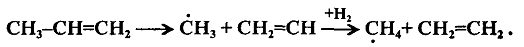
Термолиз бутиленов приводит к образованию метана, пропилена и бутадиена по реакциям:
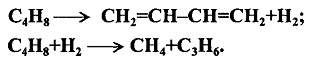
При этом одновременно начинается интенсивное образование ароматизированных жидких продуктов.
В процессе термолиза высших алкенов при умеренных температурах основной реакцией является полимеризация. При повышении температуры развивается реакция распада по С- С-связи (то есть обратная реакции полимеризации). С малой скоростью происходит также изомеризация алкенов с образованием более стабильных симметричных олефинов.
С увеличением молекулярной массы алкенов возрастает тенденция к разрыву С - С-связи. Для высокомолекулярных алкенов наличие двойной связи практически не влияет на термостойкость алкенов, и по устойчивости они становятся близкими алканам с тем же углеродным атомом.
Нафтены при термолизе более стабильны, чем соответствующие алканы. Наиболее устойчивыми среди нафтенов являются циклопентан и циклогексан. Реакции термолиза незамещенных циклоалканов протекают по нецепному механизму посредством разрыва одной из С-С-связей и образования бирадикала, который далее распадается на стабильные молекулы:
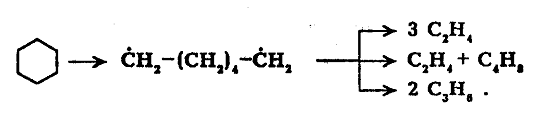
Дегидрирование незамещенных цикланов по цепному механизму не происходит, так как по сравнению с ним распад с образованием бирадикала протекает со значительно большей (на несколько порядков) скоростью. Алкилнафтены при термолизе ведут себя, как алканы: преимущественно распадаются боковые цепи
по радикально-цепному механизму.
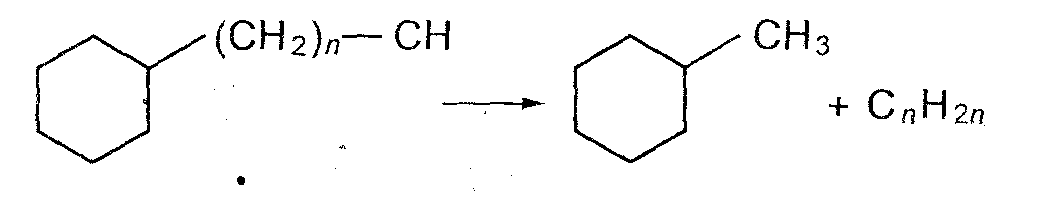
Бициклические нафтены при 600°С и выше подвергаются дециклизации, деалкилированию и дегидрированию:

Термолиз ароматических углеводородов.
Арены термически устойчивы и поэтому накапливаются в продуктах термических процессов. Ароматические углеводороды с длинными боковыми цепями способны деалкилироваться с образованием преимущественно монометилированных ароматических углеводородов.
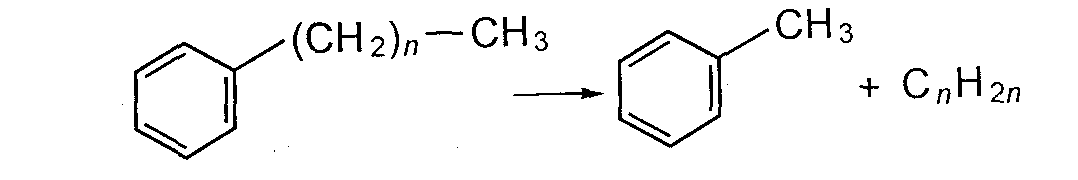
Ароматические углеводороды без заместителей (голоядерные) и ароматические углеводороды с низким числом углеродных атомов в цепи практически не подвергаются распаду. В условиях термических процессов они способны конденсироваться с выделением водорода:
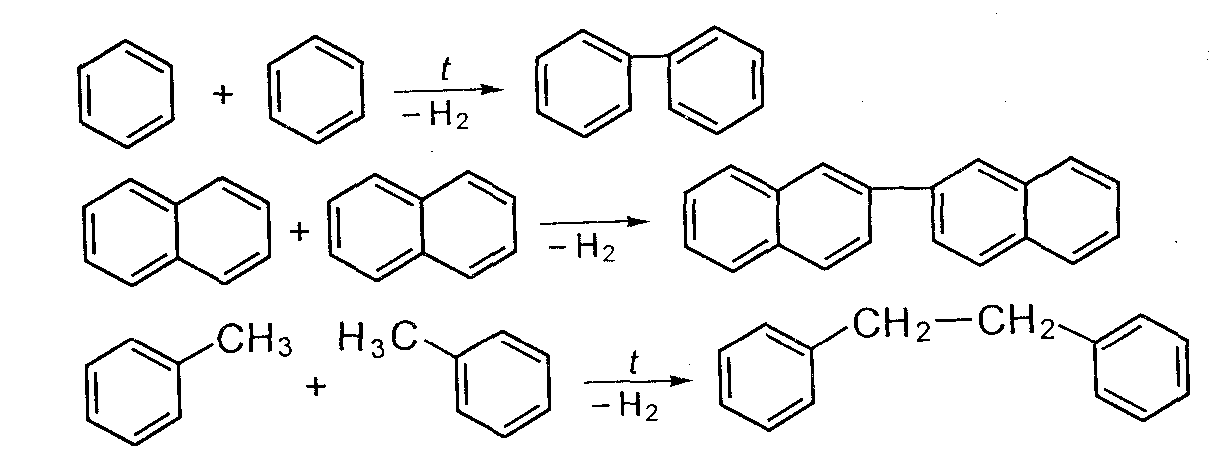
В результате образуются высококонденсированные нелетучие и нерастворимые в хинолине вещества, из которых затем получается твердый углеродистый остаток — кокс или сажа.
Термолиз смеси углеводородов. Цепные реакции, протекающие при термолизе углеводородов всегда взаимозаменяемы. Инициирование в радикально-цепных процессах термолиза является самой энергоемкой и, следовательно, лимитирующей стадией. Дальнейшие превращения радикалов происходят значительно меньшими энергиями активации. Термолиз смеси углеводородов, по сравнению с индивидуальными углеводородами, во многих случаях протекает с большей скоростью вследствие увеличения скорости инициирования активными радикалами, которые не всегда могут образоваться при распаде отдельных классов углеводородов. Отдельные углеводороды, например нафтены, распадающиеся в чистом виде по нецепному пути из-за малой скорости инициирования, в смесях могут превращаться по цепному механизму. В качестве инициаторов цепных реакций могут участвовать и отдельные продукты, образующиеся при термолизе углеводородных смесей.
Основные выводы по химизму газофазного термолиза различных классов углеводородов сводятся к следующему.
Алканы подвергаются реакциям распада на предельные и непредельные углеводороды. Молекулярная масса полученных углеводородов постоянно снижается за счет последовательного крекинга.
Алкены полимеризуются и вступают в реакцию деструктивной полимеризации. В меньшей степени выражена реакция деполимеризации. Возможна также реакция циклизации.
Цикланы и арены претерпевают реакции деалкилирования алкильных цепей, образуя алканы, алкены и цикланы с короткой боковой цепью. Шестичленные цикланы дегидрируются в арены, а последние подвергаются поликонденсации, образуя высокомолекулярные жидкие продукты.
Из вышеизложенного следует, что при термолизе нефтяного сырья протекает множество реакций и получаются продукты чрезвычайно сложного состава. Исследовать ход превращений и конечную судьбу каждого компонента смеси не представляется возможным. Несмотря на это, зная средний состав сырья, можно приблизительно прогнозировать групповой (не индивидуальный) состав конечных продуктов термолиза.
Дата добавления: 2015-08-11; просмотров: 5468;
