Физико-химические свойства белков
Наиболее характерными физико-химическими свойствами белков являются высокая вязкость растворов, незначительная диффузия, способность к набуханию в больших пределах, оптическая активность, подвижность в электрическом поле, низкое осмотическое давление и высокое онкотическое давление, способность к поглощению ультрафиолетовых лучей.
Белки, как и аминокислоты, амфотерны благодаря наличию свободных NH2- и СООН-групп. Для них характерны все свойства кислот и оснований. В зависимости от реакции среды и соотношения кислых и основных аминокислот белки в растворе несут или отрицательный, или положительный заряд, перемещаясь к аноду или катоду. Это свойство используется при очистке белков методом электрофореза.
Белки обладают явно выраженными гидрофильными свойствами. Растворы белков имеют очень низкое осмотическое давление, высокую вязкость и незначительную способность к диффузии. Белки способны к набуханию в очень больших пределах. С коллоидным состоянием белков связан ряд характерных свойств, в частности явление светорассеяния, лежащее в основе количественного определения белков методом нефелометрии. Этот эффект используется, кроме того, в современных методах микроскопии биологических объектов. Молекулы белка не способны проникать через полупроницаемые искусственные мембраны (целлофан, пергамент, коллодий), а также биомембраны растительных и животных тканей, хотя при органических поражениях, например, почек капсула почечного клубочка (Шумлянского-Боумена) становится проницаемой для альбуминов сыворотки крови и последние появляются в моче.
Молекулярная масса белков. Белки относятся к высокомолекулярным соединениям, в состав которых входят сотни и даже тысячи аминокислотных остатков, объединенных в макромолекулярную структуру. Молекулярная масса белков колеблется от 6000 (нижний предел) до 1000000 и выше в зависимости от количества отдельных полипептидных цепей в составе единой молекулярной структуры белка. Такие полипептидные цепи получили название субъединиц.
Аминокислотный состав и последовательность аминокислот выяснена для многих тысяч белков. В связи с этим стало возможным вычисление их молекулярной массы химическим путем с высокой точностью. Однако для огромного количества встречающихся в природе белков химическое строение не выяснено, поэтому основными методами определения молекулярной массы все еще остаются физико-химические методы (гравиметрические, осмометрические, вискозиметрические, электрофоретические, оптические и др.). На практике наиболее часто используются методы седиментационного анализа, где определение молекулярной массы белков проводят в ультрацентрифугах и вычисляют её по скорости седиментации молекул белка или седиментационному равновесию.
Форма белковых молекул. Данные различных видов анализа указывают на существование в природе глобулярных (шарообразных) и фибриллярных (нитевидных) белков. В настоящее время общие представления о форме белковых молекул в основном подтвердились, однако только современные методы исследования позволили установить детали пространственной конфигурации (трехмерной структуры) белковых молекул. Благодаря применению сканирующей микроскопии и рентгеноструктурного анализа удалось в деталях расшифровать не только полную пространственную структуру, форму, но и степень асимметрии белковых молекул во всех трех измерениях. Оказалось, что даже глобулярные белки крови (гемоглобин, альбумины и глобулины) являются асимметричными в указанных измерениях.
Денатурация белков.Природные белковые тела наделеныопределенной, строго заданной пространственной конфигурацией и обладают рядом характерных физико-химических и биологических свойств при физиологических значениях температуры и рН среды.Под влиянием различных физических и химических факторов белки подвергаются свертыванию и выпадают в осадок, теряя нативные свойства.
Таким образом, под денатурацией следует понимать нарушение общего плана уникальной структуры нативной молекулы белка, преимущественно ее третичной структуры, приводящее к потере характерных для нее свойств (растворимость, электрофоретическая подвижность, биологическая активность и т.д.). Большинство белков денатурирует при нагревании их растворов выше 50–60°С (рис.6).
Внешние проявления денатурации сводятся к потере растворимости, особенно в изоэлектрической точке, повышению вязкости белковых растворов, увеличению количества свободных функциональных SH-групп и изменению характера рассеивания рентгеновских лучей. Наиболее характерным признаком денатурации является резкое снижение или полная потеря белком его биологической активности (каталитической, антигенной или гормональной). При денатурации белка, разрушаются в основном нековалентные связи (в частности, гидрофобные взаимодействия и водородные связи).
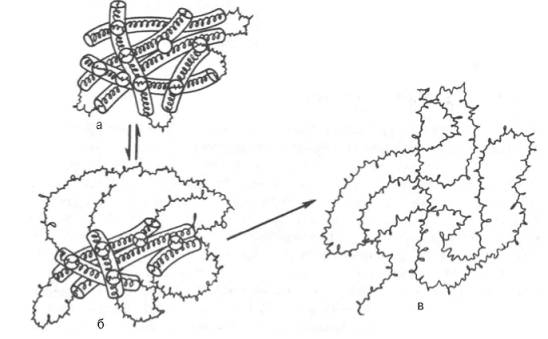
а - исходное состояние; б - начинающееся обратимое нарушение молекулярной структуры; в - необратимое развертывание полипептидной цепи.
Рисунок 6 -Денатурация белковой молекулы (схема)
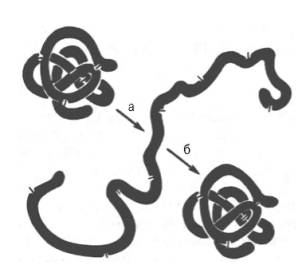
а - развертывание (мочевина + меркаптоэтанол); б - повторное свертывание
Рисунок 7-Денатурация и ренатурация рибонуклеазы (по Анфинсену)
При непродолжительном действии и быстром удалении денатурирующих агентов возможна ренатурация белка с полным восстановлением исходной трехмерной структуры и нативных свойств его молекулы (рис. 7), включая биологическую активность. Таким образом, при денатурации белковая молекула полностью теряет биологические свойства, демонстрируя тем самым тесную связь между структурой и функцией. Для практических целей иногда используют процесс денатурации в «мягких» условиях, например при получении ферментов или других биологически активных белковых препаратов в условиях низких температур в присутствии солей и при соответствующем значении рН. При лиофилизации белков (высушивание в вакууме путем возгонки влаги из замороженного состояния) для предотвращения денатурации часто пользуются химическими веществами (простые сахара, глицерин, органические анионы).
Изоэлектрическая и изоионная точки белков. В изоэлектрической точке суммарный заряд белков, обладающих амфотерными свойствами, равен нулю и белки не перемещаются в электрическом поле. Зная аминокислотный состав белка, можно приближенно определить изоэлектрическую точку (pI); pI является характерной константой белков. Изоэлектрическая точка большинства белков животных тканей лежит в пределах от 5,5 до 7,0, что свидетельствует о частичном преобладании кислых аминокислот. Однако в природе имеются белки, у которых значения изоэлектрических точек лежат в крайних значениях рН среды. В частности, величина рI пепсина (фермент желудочного сока) равна 1, а сальмина (основной белок из молоки семги) – почти 12.
В изоэлектрической точке белки наименее устойчивы в растворе и легко выпадают в осадок. Изоэлектрическая точка белка в сильной степени зависит от присутствия в растворе ионов солей; в то же время на ее величину не влияет концентрация белка.
Раствор белка называется изоионным, если он не содержит никаких других ионов, кроме ионизированных остатков аминокислот белковой молекулы и ионов, образующихся при диссоциации воды. Для освобождения белка от посторонних ионов обычно его раствор пропускают через колонку, наполненную смесью анионо- и катионообменников. Изоионной точкой данного белка принято называть значение рН изоионного раствора этого белка:
[Н]+ + [Р] Z = [ОН]-
где [Р] – молярная концентрация белка; Z – средний заряд молекулы. Согласно этому уравнению, изоионная точка белка зависит от его концентрации. Очевидно, поэтому белок, за исключением случая, когда рI равно 7, не может быть одновременно изоэлектрическим и изоионным.
Кислотно-основные свойства.Белки, как и аминокислоты, являются полиамфолитами, проявляя кислотные свойства за счет неионизированных группы – СООН, аммонийных групп – NН3+, тиольных групп – SН. Основные свойства белки проявляют за счет групп –СОО-, аминогрупп –NН2 и др. В водных растворах в зависимости от рН среды белки могут находиться при рН=рI белка в молекулярной, т.е. нейтральной форме, при рН < рI белок проявляет катионные свойства, а при рН > рI проявляется анионная форма.
NН3+ – Рrot – СОО- ↔ NН3+ – Рrot – СОО- ↔ NН3+ – Рrot – СОО-
|+ | |
RН2 RН R-
рН < рI рН = рI рН > рI
катион белка молекула белка анион белка
В зависимости от аминокислотного состава белки подразделяются на «нейтральные» ( рI = 5,0-7,0), «кислотные» ( рI < 4,0) с повышенным содержанием аспарагиновой и глутаминовой кислоты, и «основные» с повышенным содержанием аргинина, лизина или гистидина ( рI >7,5). На основе белков в организме действуют буферные свойства белков.
Буферные свойства белков обусловлены наличием в составляющих их аминокислотах (карбоксикислотах) аминогруппы (NH2-группы). Благодаря ней аминокислоты могут реагировать не только как слабые кислоты, но и как основания, то есть сами проявлять буферные свойства, присоединяя или отдавая ион водорода. Отщепляемый от карбоксильной группы протон может присоединиться к аминогруппе. В результате – молекула аминокислоты принимает дипольную форму (или форму цвиттер-иона), заряжаясь с одной стороны отрицательно, а с другой – положительно, но оставаясь в целом нейтральной. Именно в этой форме аминокислота и проявляет свои буферные свойства. При повышении концентрации протонов в среде (снижение рН) они фиксируются карбоксильной группой, а молекула оказывается положительно заряженной. Наоборот, при падении концентрации протонов третий протон с положительно заряженной стороны молекулы отдается, а вся молекула заряжается отрицательно. Аминокислота диссоциирует с образованием протона и диссоциированной карбоксильной группы.
NН2–R–СООН ↔ NН2–R–СОО- + Н+
Или аминогруппа принимает свободный протон и приобретает форму цвиттер-иона. В избытке протонов молекула заряжается положительно:
Н+ + NH2–R–СOО– ↔ NH3+ –R – СOО–
При дефиците протонов - молекула приобретает отрицательный заряд:
NН3+–R–СОО– ↔ Н+ + NН2–R–СОО–
Буферные свойства белков проявляются в связывании не только протонов, но и других заряженных частиц. Основная масса поступающих в кровоток веществ (красители, жирные кислоты, липиды, водорастворимые наркотики, релаксанты) связывается с белками, проявляя конкурентные отношения. Естественно, при этом уменьшается буферная емкость белков в отношении протонов, и высокая концентрация последних затрудняет освобождение и ослабляет действие веществ, образующих положительные заряды.
Белки активно вступают в химические реакции. Это свойство связано с тем, что аминокислоты, входящие в состав белков, содержат разные функциональные группы, способные реагировать с другими веществами. Важно, что такие взаимодействия происходят и внутри белковой молекулы, в результате чего образуется пептидная, водородная, дисульфидная и другие виды связей. Белки обладают большим сродством к воде, то есть они гидрофильны. Это значит, что молекулы белка, как заряженные частицы, притягивают к себе диполи воды, которые располагаются вокруг белковой молекулы и образуют водную или гидратную оболочку. Эта оболочка предохраняет молекулы белка от склеивания и выпадения в осадок. Величина гидратной оболочки зависит от структуры белка. Например, альбумины более легко связываются с молекулами воды и имеют относительно большую водную оболочку, тогда как глобулины, фибриноген присоединяют воду хуже, и гидратная оболочка и них меньше. Таким образом, устойчивость водного раствора белка определяется двумя факторами: наличием заряда белковой молекулы и находящейся вокруг нее водной оболочки. При удалении этих факторов белок выпадает в осадок. Данный процесс может быть обратимым и необратимым. Обратимое осаждение белков (высаливание) предполагает выпадение белка в осадок под действием определенных веществ, после удаления которых, он вновь возвращается в свое исходное (нативное) состояние. Для высаливания белков используют соли щелочных и щелочноземельных металлов (наиболее часто в практике используют сульфат натрия и аммония). Эти соли удаляют водную оболочку (вызывают обезвоживание) и снимают заряд. Между величиной водной оболочки белковых молекул и концентрацией солей существует прямая зависимость: чем меньше гидратная оболочка, тем меньше требуется солей. Так, глобулины, имеющие крупные и тяжелые молекулы и небольшую водную оболочку, выпадают в осадок при неполном насыщении раствора солями, а альбумины как более мелкие молекулы, окруженные большой водной оболочкой — при полном насыщении. Необратимое осаждение связано с глубокими внутримолекулярными изменениями структуры белка, что приводит в потере ими нативных свойств – денатурации, которая влечет потерю растворимости, биологической активности и т.д. Необратимое осаждение можно вызвать кипячением, действием концентрированными растворами некоторых из минеральных и органических кислот, солями тяжелых металлов.Гидролиз белка достигается при помощи кипячения белка с сильными минеральными кислотами (кислотный гидролиз) или основаниями (щелочной гидролиз). Но щелочной гидролиз редко используется из-за неустойчивости аминокислот в этих условиях. Проводят его при нагревании до 1100С в запаянной ампуле с 20% соляной кислотой в течение 24 ч. В организме он протекает при участии пептидаз в липосомах. Гидролиз может быть частичным (до пептидов) или полным (до аминокислот). В организме гидролиз белков осуществляется целым набором ферментов, каждый из которых расщепляет ту или иную связь. Карбоксипептидаза отщепляет от белка С-концевую кислоту, трипсин гидролизует связь образованную аминокислотами с неполярным (гидрофобным) заместителем, химотрипсин – связь, образованную между фенилаланином, тирозином, триптофаном с другими аминокислотами. В организме белки гидролизуются полностью. О H О Н О || | || | || NH2— СН—С—N—СH—С—N—СН—С— ·· + nH2O ↔ ОН- + | | | R1 R2 R3 O O О || || ||·· + NH2—СН—С— ОН+ NH2—СН—С—ОН + NH2—СН—С—ОН + ·· | | | R2 R3 R1Белки, содержащие аспарагиновую и глутаминовую кислоту, вступают в реакцию амидированиябелков, при которой обезвреживается аммиак:
NН3+ – Рrot – СОО- + NН3 ↔ NН3+ – Рrot – СОО-
|+ | + Н2О
СН2 – СООН СН2 – СОNН2
Окислительно-восстановительные свойства. Белки относительно устойчивы к мягкому окислению, за исключением содержащих аминокислоту цистеин, так как тиольная группа её легко окисляется в дисульфидную группу, причем этот процесс может носить и обратный характер:
окислитель
2 R–SН R–S – S – R +2е + 2 Н+
Восстановленная восстановитель окисленная
форма форма
В результате этих превращений происходит изменение конформации белка и его нативных свойств. Эти превращения лежат в основе химической завивки волос, так как цистеин и цистин входят в состав белка волос кератина. Сначала волосы обрабатывают восстановителем, чтобы разрушить связи –S – S – цистина и превратить в тиольные группы цистеина. Затем волосы укладывают в локоны и обрабатывают окислителем. При этом образуются дисульфидные связи цистина, которые помогают волосам сохранить их новую форму.
В организме белки, содержащие остатки лизина, пролина, фенилаланина и триптофана, подвергаются ферментативному гидроксилированию при участии кислорода и восстановленной формы кофермента:
NН3+ – Рrot – СОО- + О2 + восстановленная ↔ NН3+ – Рrot – СОО-+ Н2О + окисленная
| форма | форма
RН кофермента RОН кофермента
Также для белков характерны и все цветные (качественные) реакции на аминокислоты.
Дата добавления: 2015-08-11; просмотров: 3508;
