Вычисление давление продуктов горения пороха
Если бы горение пороха подчинялось законам идеальных газов и все взятое количество пороха обращалось в газы, то давление можно было рассчитать по уравнению Менделеева-Клайперона:
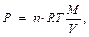 (2)
(2)
где 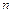 – число грамм молей газа, образовавшегося при взрыве 1 кг пороха.
– число грамм молей газа, образовавшегося при взрыве 1 кг пороха.
Величина 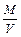 – отношение массы пороха к объему, в котором проходит взрыв.
– отношение массы пороха к объему, в котором проходит взрыв.
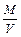 = ∆ – плотность заряжения.
= ∆ – плотность заряжения.
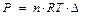 (3)
(3)
Произведение 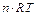 – называют силой пороха и обозначают f.
– называют силой пороха и обозначают f.
Формула имеет вид: P = f · ∆ – справедливо для идеальных газов.
Физический смысл:
Сила пороха 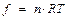 есть работа расширения 1 кг газа, охлаждающегося на Т0 при атмосферном давлении Р0. Повысить f можно таким изменением состава пороха, при котором Т и V0.
есть работа расширения 1 кг газа, охлаждающегося на Т0 при атмосферном давлении Р0. Повысить f можно таким изменением состава пороха, при котором Т и V0.
Для реальных газов их состояние может быть описано уравнением Ван-дер-Ваальса:
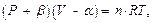
где 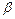 – внутреннее давление, обусловленное взаимным притяжением молекул.
– внутреннее давление, обусловленное взаимным притяжением молекул.
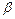 – пренебрегаем: уравнение заменяется:
– пренебрегаем: уравнение заменяется:
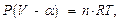 (4)
(4)
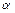 – называется коволюмом, учитывающий ту часть объема газа, которая представляет сумму сфер действия молекулярных сил и недоступна для движения молекул.
– называется коволюмом, учитывающий ту часть объема газа, которая представляет сумму сфер действия молекулярных сил и недоступна для движения молекул.
Величина коволюма согласно теоретическим расчетам приблизительно равна учетверенному объему самих молекул. Теоретический расчет объема молекул труден, а часто и невыполним. Поэтому при определении давления взрыва пользуются приближенной величиной коволюма газообразных продуктов, принимая ее равной 0,001 объема, который газы занимают при нормальных условиях.
Из уравнения (4) следует, что:
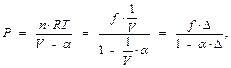
Это основная формула внутренней баллистики (выведена Л.Н. Шишковым в 1857 г).
Из этого уравнения следует, что:
а) давление тем больше, чем больше сила f и 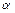 пороха;
пороха;
б) наибольшее давление дадут те пороха, которые способны образовывать наибольший объем газов с малой теплоемкостью и выделить при этом относительно большое количество тепла.
Дата добавления: 2015-08-08; просмотров: 2646;
