Закон Бугера—Ламберта—Бера
Вернемся к коэффициенту поглощения k для монодисперсного света. Уже сам Бугер предполагал, что величина k зависит от числа атомов, которые свет встречает на своем пути, то есть от концентрации С поглощающего вещества. В 1852 г. немецкий ученый Бер экспериментально показал, что коэффициент поглощения k пропорционален молярной концентрации поглощающего вещества
k= 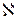 С
С
Молярный коэффициент поглощения 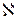 не зависит от концентрации, является табличной величиной и имеется в справочниках для каждого вещества при данной длине волны проходящего света. Формулу
не зависит от концентрации, является табличной величиной и имеется в справочниках для каждого вещества при данной длине волны проходящего света. Формулу
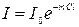
называют законом Бугера—Ламберта—Бера.
Напомним, что в химии молярную концентрацию измеряют не числом частиц, а числом молей в единице объема [С] = моль/м3. Зная концентрацию в молях на кубический метр, можно определить и концентрацию частиц (молекул), если умножить ее на число Авогадро NA=6·10231/моль. В любом случае С·l — характеризует количество молекул растворенного вещества, попадающихся на пути луча света единичной площади сечения. Размерность величины С·l, очевидно, равна [С·l] = (моль/м3) м = моль/м2 или просто м-2. Поскольку произведение 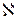 Сl должно быть безразмерно, то молярный коэффициент поглощения
Сl должно быть безразмерно, то молярный коэффициент поглощения 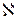 выражается в м2.
выражается в м2.
Закон Бугера—Ламберта—Бера очень часто используют в практике для определения концентрации растворов. Если на пути двух одинаковых пучков монохроматического света поставить кюветы с растворами одного и того же вещества, но в различных концентрациях С1 и Сх, то при одинаковой длине кювет можно написать
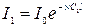
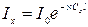
откуда следует
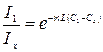
или
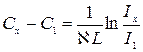
Таким образом, определение неизвестной концентрации раствора Сх сводится к сравнению интенсивности света Iх, прошедшего через кювету с исследуемым веществом Сх и интенсивности света I1 через контрольную кювету с известной концентрацией С1. Приборы, позволяющие определить концентрацию раствора таким методом, часто используют в лабораториях и на производстве.
Контрольные вопросы:
1. Свет проходит последовательно через две кюветы, расположенные одна за другой. Длина каждой кюветы L. Нарисовать изменение интенсивности света от координаты l в случаях а) если кюветы заполнены раствором одинаковой концентрации, б) если концентрация поглощающего вещества в первой кювете больше C1> C2, в) если С1<С2.
2. Нарисуйте аналогичные рисунки в случае, когда между кюветами имеется промежуток воздуха длиной L.
3. Зависимость молярного коэффициента поглощения 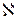
от длины волны света λ (спектр поглощения)
Для монохроматического света, то есть при определенном значении длины волны света λ, молярный коэффициент поглощения 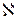 является постоянной величиной, которая определяется только типом поглощающего вещества. Если же длина волны света меняется, то перестает быть постоянной величиной и становится функцией λ. Например, молярный коэффициент поглощения раствора красной краски невелик при λ=600 нм, то есть для красного света, а при λ=400 нм (для синего света) становится гораздо больше (рис. 13в). Соответственно раствор красной краски будет сильно поглощать синие лучи и слабо поглощать красные лучи света. В результате в белом свете, прошедшем через раствор красной краски, останутся только красные лучи.
является постоянной величиной, которая определяется только типом поглощающего вещества. Если же длина волны света меняется, то перестает быть постоянной величиной и становится функцией λ. Например, молярный коэффициент поглощения раствора красной краски невелик при λ=600 нм, то есть для красного света, а при λ=400 нм (для синего света) становится гораздо больше (рис. 13в). Соответственно раствор красной краски будет сильно поглощать синие лучи и слабо поглощать красные лучи света. В результате в белом свете, прошедшем через раствор красной краски, останутся только красные лучи.
Зависимость молярного коэффициента поглощения от длины волны света 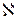 часто называют спектром поглощения данного вещества. Измерение спектров поглощения веществ позволяет проводить их идентификацию, поскольку спектры поглощения строго индивидуальны. На рис. 13 показаны спектры поглощения атомов водорода (а) и паров натрия (б). Подобными линейчатыми спектрами поглощения обладают газы и пары (особенно одноатомные). Спектры поглощения жидкостей и твердых тел, как правило, имеют вид сплошных линий, наподобие рис. 13(в).
часто называют спектром поглощения данного вещества. Измерение спектров поглощения веществ позволяет проводить их идентификацию, поскольку спектры поглощения строго индивидуальны. На рис. 13 показаны спектры поглощения атомов водорода (а) и паров натрия (б). Подобными линейчатыми спектрами поглощения обладают газы и пары (особенно одноатомные). Спектры поглощения жидкостей и твердых тел, как правило, имеют вид сплошных линий, наподобие рис. 13(в).
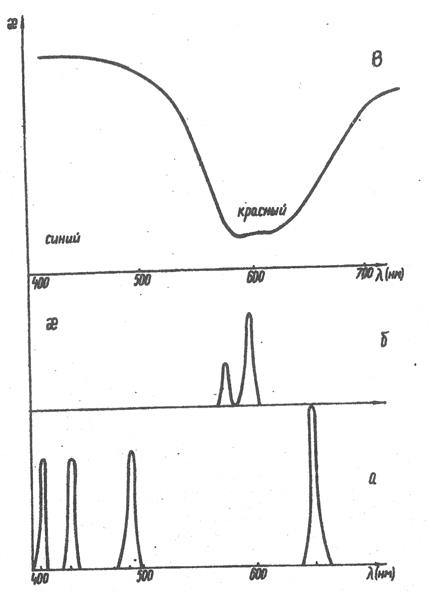
Рис. 13. Спектры поглощения паров водорода (а), паров натрия (б)
и раствора красной краски (или красного стекла) (в)
В физиологии по спектрам поглощения можно судить о характере и развитии болезней. Например, спектры поглощения клеток кожи человека в норме и при подкожных кровоизлияниях (при эритеме) отличаются (рис. 14). Поэтому, сняв спектры поглощения кожи, можно проводить диагностику и следить за развитием болезни.
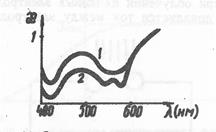
Рис. 14. Спектры поглощения кожи человека в норме (1) и при эритеме (2)
На рис. 15 приведены спектры поглощения гемоглобина в обычном и окисленном состояниях. Как видно, спектр поглощения позволяет легко различать эти состояния, а, следовательно, судить об эффективности работы крови как переносчика кислорода.
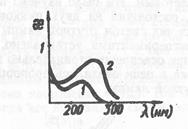
Рис 15. Спектры поглощения биологических важных
соединений — триптофана (1) и аденина (2)
По спектру поглощения легко идентифицировать даже очень малое количество вещества ~10-9 г; можно также определить наличие небольшого количества примеси ~10-6 %.
Занятие № 3
Тема: ФОТОЭФФЕКТ
Дата добавления: 2015-08-08; просмотров: 2158;
