Смещение равновесия гидролиза
1. 
По принципу Ле-Шателье уменьшение концентрации ионов водорода сместит равновесие вправо, т.е. усилит гидролиз. Чтобы усилить гидролиз, нужно добавить сильную щелочь, связывающую ионы водорода.
Добавление ионов водорода (кислоты) – подавляет гидролиз, смещая равновесие гидролиза влево.
2. 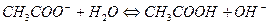
Добавление сильной кислоты (Н+) сместит равновесие гидролиза вправо, так как при этом будут связываться ионы гидроксила. Добавление щелочи подавляет гидролиз.
3. Гидролиз проходит до конца, если в результате получаются не растворимые в воде соединения и газы.
Например:
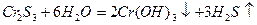
Соли, образованные многозарядными катионами (Cr3+, Fe3+, Al3+) и очень слабыми кислотами (угольной, сернистой, сероводородной, кремниевой) – в водном растворе не существуют, так как подвергаются необратимому гидролизу.
Дата добавления: 2015-08-08; просмотров: 933;
