Структура комплексных соединений по Вернеру.
Комплексные соединения состоят из внешней и внутренней сферы, внутреннюю сферу комплексного соединения составляют ион-комплексообразователь и лиганды. Комплексообразователем являются, чаще всего, d-элементы или амфотерные металлы. Лигандами являются нейтральные молекулы или отрицательно заряженные ионы. Количество лигандов определяется координационным числом комплексообразователя, которое, как правило, равно удвоенной валентности иона-комплексообразователя. Лиганды бывают монодентантными и полидентантными. Дентантность лиганда определяется числом координационных мест, которые лиганд занимает в координационной сфере комплексообразователя. Например, F- - монодентантный лиганд, S2O32- - бидентантный лиганд. Заряд внутренней сферы равен алгебраической сумме зарядов составляющих ее ионов. Если внутренняя сфера имеет отрицательный заряд – это анионный комплекс, если положительный – катионный. Катионные комплексы называют по имени иона-комплексообразователя по-русски, в анионных комплексах комплексообразователь называется по-латыни с добавлением суффикса –ат. Связь между внешней и внутренней сферами в комплексном соединении – ионная, во внутренней сфере связь между комплексообразователем и лигандами донорно-акцепторная, при этом комплексообразователь является акцептором, а лиганд – донором электронной пары.
Пример: Na2[Zn(OH)4] – тетрагидроксоцинкат натрия, анионный комплекс.
1. [Zn(OH)4]2- - внутренняя сфера
2. 2Na+ - внешняя сфера
3. Zn2+ - комплексообразователь
4. OH- - лиганды
5. координационное число – 4
6. связь между внешней и внутренней сферами ионная: 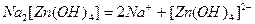
7. связь между ионом Zn2+ и гидроксильными группами – донорно-акцепторная, OH- - доноры, Zn2+ - акцептор.
Zn0: … 3d10 4s2
Zn2+: … 3d10 4s0 p0 d0
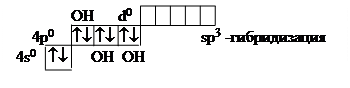 |
Типы комплексных соединений:
1. Аммино – комплексы (аммиакаты).
Лиганд: NH30 (аммино-)
Пример:
[ Cu2+(NH3)4]SO4 – сульфат тетраамминмеди (II).
Амминокомплексы получаются действием избытка аммиака на соединение, содержащее комплексообразователь.
2. Гидроксо – комплексы
Лиганд: OH- ( гидроксо – )
Na2[Zn(OH)4] - тетрагидроксоцинкат натрия
Получают гидроксо – комплексы действием избытка щелочи на соли амфотерных металлов.
3. Аква – комплексы.
Лиганд: H2O (аква -)
[Co(H2O)6]3+Cl3 – хлорид гексааквакобальта (III).
Получают аква-комплексы кристаллизацией или высаждением из водных растворов.
4. Ацидо – комплексы
Лиганд: анионы кислот – Cl-, F-, CN-, SO32-
K3[Fe3+(CN)6] - гексацианоферрат (III) калия.
Получают действием избытка соли, содержащей лиганд, на соль, содержащую комплексообразователь.
Дата добавления: 2015-08-08; просмотров: 3159;
