Нарушения сердечного ритма и проводимости (с указанием формы). 7 страница
Препарат может использоваться в течение длительного времени (курсовое лечение 1–3 месяца) в дозе 20 мг 3 раза в день. Лучшие результаты получают при комбинированном назначении тримезидина и одного из “гемодинамических” антиангинальных средств.
Ингибиторы АПФ
Ингибиторы АПФ в последнее время все шире используются в лечении больных ИБС с целью профилактики прогрессирования дисфункции ЛЖ. Они особенно показаны больным, перенесшим ИМ и имеющим признаки снижения насосной функции сердца. В этих случаях ингибиторы АПФ прежде всего оказывают влияние на гемодинамику. Они способствуют нормализации (или оптимизации) АД, уменьшают преднагрузку и постнагрузку, в известной степени устраняют констрикцию коронарных сосудов, повышают экскрецию натрия и воды, уменьшая продукцию альдостерона, устраняют прямое токсическое действие ангиотензина II и катехоламинов на миокард (А.Я. Ивлева). Помимо этого, ингибиторы АПФ ограничивают влияние ангиотензина II на процесс атерогенеза, миграцию и пролиферацию гладкомышечных клеток, гиперплазию сосудистой интимы и улучшают функцию эндотелия, повышая продукцию оксида азота и других вазодилатирующих субстанций. Ингибиторы АПФ способствуют стабилизации атеросклеротической бляшки и уменьшению частоты возникновения острого коронарного синдрома.
По данным нескольких широкомасштабных контролируемых клинических исследований (SAVE, АIRЕ, ТRAZU, ХЕАRТ, SОLVD), применение ингибиторов АПФ у больных, перенесших ИМ, приводит к достоверному уменьшению числа повторных ИМ и эпизодов нестабильной стенокардии, частоты развития сердечной недостаточности и общей летальности больных.
Показания. В настоящее время определены показания и тактика применения ингибиторов АПФ у больных, перенесших ИМ. Лечение ингибиторами АПФ показано в следующих случаях:
- при наличии клинических признаков сердечной недостаточности;
- при ФВ ЛЖ меньше 40% (независимо от наличия или отсутствия клинических признаков СН);
- при переднем ИМ;
- при повышенном риске возникновения повторного ИМ (у лиц старше 65 лет или у пациентов, перенесших обширные ИМ с величиной зоны акинезии, определяемой при ЭхоКГ, более 20%);
- при сохранении стабильной окклюзии КА в зоне инфаркта.
Методика лечения ингибиторами АПФ, побочные эффекты и противопоказания подробно описаны в главе 2 настоящего руководства.
Комбинированное лечение антиангинальными средствами
Положительный эффект лечения больных со стабильной стенокардией антиангинальными ЛС колеблется в широких пределах, в среднем составляя около 70–75%. При неэффективности или недостаточной эффективности монотерапии рекомендуется комбинированное лечение двумя или тремя антиангинальными препаратами. Нередко это позволяет снизить дозы каждого из назначаемых препаратов и уменьшить тем самым риск возникновения побочных эффектов. Оптимальными комбинациями антиангинальных ЛС считают следующие их сочетания.
1. β-адреноблокатор + нитраты. Это наиболее частая комбинация двух антиангинальных ЛС, в известной степени нивелирующая побочные эффекты каждого из препаратов. Сочетание нитратов и β-адреноблокаторов особенно показано больным ИБС со стенокардией напряжения III–IV ФК, в том числе пациентам, перенесшим ИМ.
2. β1-адреноблокатор + блокатор медленных кальциевых каналов пролонгированного действия из группы нифедипина. β1-адреноблокаторы (метопролол, атенолол и др.) нивелируют отрицательные эффекты рефлекторной активации САС, возникающей на фоне лечения препаратами дигидропиридинового ряда.
3. Верапамил + нитраты. Комбинация особенно показана в случае возникновения суправентрикулярных нарушений сердечного ритма.
При рефрактерности больных к монотерапии и комбинированному лечению двумя антиангинальными препаратами возможна попытка назначения трех ЛС, обладающих соответствующим действием. Например, можно использовать комбинацию: b-адреноблокатор + препараты изосорбида динитрата или изосорбида мононитрата + дилтиазем (Boden, 1985). Однако назначение препаратов, относящихся к трем различным группам антиангинальных ЛС, далеко не всегда приводит к усилению их суммарного эффекта. В этих случаях иногда полезно еще раз подумать о правильности выбора отдельных антиангинальных препаратов, адекватности их суточных доз и режима приема препарата в течение суток. При неэффективности лекарственной терапии ИБС следует рассмотреть вопрос о целесообразности хирургической реваскуляризации миокарда.
Гиполипидемическая терапия
Гиполипидемическая терапия (немедикаментозная и медикаментозная) должна являться обязательной составной частью комбинированного лечения больных со стабильной стенокардией напряжения. Известно, что уменьшение летальности от осложнений ИБС и частоты развития ИМ происходит пропорционально снижению уровня ХС и ХС ЛНП (А.Я. Ивлева). Успешная коррекция нарушений липидного обмена, вместе с воздействиями на другие ФР ИБС, существенно улучшает результаты назначаемой антиангинальной терапии и заметно улучшает качество жизни больных ИБС.
При лечении больных ИБС со стабильной стенокардией следует придерживаться принципов, подробно изложенных в главе 4.
 Запомните
Лечение больных ИБС со стабильной стенокардией напряжения основано на следующих основных принципах.
1. Коррекция основных ФР ИБС, в первую очередь, немедикаментозная и медикаментозная гиполипидемическая терапия, антигипертензивная терапия, прекращение курения, уменьшение избыточной массы тела, коррекция нарушений углеводного обмена, оптимальная физическая активность. 2. Антитромбоцитарная терапия (аспирин, клопидогрель, курантил и др.), которую должны получать все больные со стабильной стенокардией напряжения. 3. Выбор ЛС антиангинального (антиишемического) действия (нитратов, β-адреноблокаторов, блокаторов медленных кальциевых каналов или их комбинации) должен учитывать индивидуальные особенности течения ИБС, наличие сопутствующих заболеваний и ФР атеросклероза, а также состояние гемодинамики. 4. Прием антиангинальных ЛС гемодинамического действия целесообразно сочетать с применением метаболической терапии (триметазидин). 5. Признаки дисфункции ЛЖ или клинические проявления сердечной недостаточности являются показанием для применения ингибиторов АПФ, особенно у больных, перенесших ИМ. Запомните
Лечение больных ИБС со стабильной стенокардией напряжения основано на следующих основных принципах.
1. Коррекция основных ФР ИБС, в первую очередь, немедикаментозная и медикаментозная гиполипидемическая терапия, антигипертензивная терапия, прекращение курения, уменьшение избыточной массы тела, коррекция нарушений углеводного обмена, оптимальная физическая активность. 2. Антитромбоцитарная терапия (аспирин, клопидогрель, курантил и др.), которую должны получать все больные со стабильной стенокардией напряжения. 3. Выбор ЛС антиангинального (антиишемического) действия (нитратов, β-адреноблокаторов, блокаторов медленных кальциевых каналов или их комбинации) должен учитывать индивидуальные особенности течения ИБС, наличие сопутствующих заболеваний и ФР атеросклероза, а также состояние гемодинамики. 4. Прием антиангинальных ЛС гемодинамического действия целесообразно сочетать с применением метаболической терапии (триметазидин). 5. Признаки дисфункции ЛЖ или клинические проявления сердечной недостаточности являются показанием для применения ингибиторов АПФ, особенно у больных, перенесших ИМ.
|
Хирургические методы реваскуляризации миокарда
Методы хирургической реваскуляризации миокарда получили в последнее время достаточно широкое распространение в клинической практике. Реваскуляризация улучшает выживаемость больных с тяжелым течением и/или серьезным прогнозом заболевания. В клинике чаще используют два метода: чрескожную транслюминальную коронарную ангиопластику (ЧТКА) и аортокоронарное шунтирование (АКШ). Наиболее общими показаниями к проведению реваскуляризации являются ангиографические и клинические признаки, указывающие на высокий риск развития ИМ и внезапной сердечной смерти:
- трехсосудистое поражение КА;
- 2–3-х сосудистое поражение КА в сочетании с дисфункцией ЛЖ;
- поражение ствола ЛКА;
- ФВ ЛЖ меньше 30% (независимо от количества пораженных КА).
Частым показанием к проведению КАГ и хирургическому вмешательству у больных со стабильной стенокардией напряжения является неэффективность медикаментозной терапии и сохранение выраженных симптомов заболевания, резко ограничивающих физическую активность пациентов. Однако в этих случаях, как правило, имеется угрожающее поражение коронарного русла, т.е. присутствуют ангиографические показания к проведению реваскуляризации.
Выбор между двумя методами хирургической реваскуляризации (ЧТКА и АКШ) до сих пор является предметом дискуссий. Полагают, что при одно-двухсосудистом стенозе проксимальных участков КА (за исключением поражения ствола ЛКА) и удовлетворительной функции ЛЖ целесообразно проведение ЧТКА. Эта же процедура является предпочтительной у лиц пожилого возраста или при наличии противопоказаний к расширенному оперативному вмешательству на сердце. При многососудистом стенозировании КА или поражении ствола ЛКА, сочетающихся со снижением ФВ ЛЖ и/или наличием сахарного диабета, более показана операция АКШ.
Чрескожная транслюминальная коронарная ангиопластика (ЧТКА)
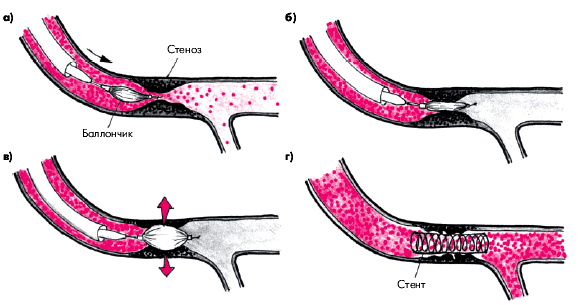
Операция заключается в механическом расширении стенозированного участка КА путем раздувания специального баллончика, введенного в артерию (рис. 5.50). С этой целью осуществляют катетеризацию бедренной или плечевой артерии. Катетер с баллончиком на конце проводят ретроградно через аорту в устье стенозированной КА. Когда баллончик оказывается на уровне стеноза, его несколько раз раздувают под давлением в несколько атмосфер и оставляют в надутом состоянии около 20–30 с. Обычно в результате механического растяжения просвет артерии увеличивается на 50–80%. Во время всей операции осуществляют ангиографический контроль.
В настоящее время смертность при проведении процедуры ангиопластики не превышает 0,2–0,6%, острый инфаркт миокарда развивается в 1–2% случаев. Только у 3% больных возникает необходимость в экстренной операции аортокоронарного шунтирования.
Первичный эффект (достижение желательной дилатации КА) отмечается в 85–90% случаев, однако в течение ближайших 6–12 месяцев после проведения ангиопластики у 30–40% больных развиваются рестенозы. Чаще они возникают у пациентов, которые были оперированы в период “обострения” ИБС, т.е. у больных с нестабильной стенокардией (см. главу 6). Для того чтобы уменьшить количество рестенозов в последние годы все чаще осуществляют так называемое стентирование — имплантацию в КА, подвергшуюся дилатации, специальных проволочных каркасов–стентов.
|
| Рис. 5.50. Схематическое изображение техники транслюминальной коронарной ангиопластики (а, б, в) и cтентирования (г) при стенозирующем коронарном атеросклерозе |
Аортокоронарное шунтирование
Операция аортокоронарного шунтирования (АКШ) заключается в наложении обходных анастомозов между аортой и пораженной КА дистальнее места ее сужения. Для создания анастомоза обычно используют трансплантат подкожной вены бедра или левой внутренней грудной артерии.
Положительный эффект операции АКШ наблюдается в 80–90% случаев, причем более чем у половины оперированных больных на время полностью исчезают клинические проявления болезни. Интраоперационная и послеоперационная летальность во многом зависит от квалификации хирургических бригад и обычно в среднем не превышает 1–3%. Более высокая летальность наблюдается у лиц старше 70 лет, при поражении ствола ЛКА, а также у больных, оперированных по экстренным показаниям в связи с развитием нестабильной стенокардии. Примерно у 4–5% больных в послеоперационном периоде развивается ИМ. При использовании венозных трансплантатов в течение 5 лет окклюзия анастомозов развивается в 20% случаев; через 10 лет их количество достигает 41%. Применение артериальных трансплантатов обеспечивает сохранение проходимости анастомозов в течение 10 лет у 90% оперированных больных.
| 5.4.5. Прогноз |

|
Прогноз у больных стабильной стенокардией напряжения в целом относительно благоприятный. При отсутствии стеноза ствола ЛКА смертность составляет в среднем около 3% в год. Характерно, что количество приступов стенокардии в неделю не коррелирует с прогнозом до тех пор, пока приступы являются кратковременными и возникают только при физической нагрузке (G.J. Taylor).
Основными факторами, ухудшающими прогноз стабильной стенокардии, являются:
- распространенность коронарного атеросклероза: при однососудистом поражении ежегодная смертность составляет 2–3%, при двухсосудистом — 4–5%, а при трехсосудистом поражении коронарного русла — 7–10%;
- выраженный (более 70% просвета) стеноз ствола ЛКА (смертность в течение года достигает 30–40%);
- низкая толерантность к физической нагрузке: ежегодная смертность составляет 6–10%, тогда как при высокой толерантности она не превышает 1%;
- снижение систолической функции ЛЖ;
- возраст больных;
- наличие сопутствующей АГ и/или сахарного диабета.
| 5.5. Спонтанная (вариантная) стенокардия |

|
Спонтанная (вариантная, вазоспастическая, типа Принцметала) стенокардия была впервые описана в 1959 г. М. Принцметалом. Это особая форма стенокардии покоя, которая возникает внезапно, без действия видимых провоцирующих факторов, и характеризующаяся спазмом КА, тяжелым болевым ангинозным приступом и в большинстве случаев значительным преходящим подъемом сегмента RS–Т на ЭКГ.
| 5.5.1. Особенности патогенеза |

|
В основе вариантной стенокардии лежит выраженный спазм КА, ведущий к ее кратковременной динамической окклюзии. Прекращение или резкое уменьшение коронарного кровообращения приводит к глубокой, часто трансмуральной, ишемии миокарда, снижению локальной сократимости ЛЖ, асинергии сокращений и значительной электрической нестабильности миокарда, проявляющейся нарушением ритма и проводимости.
Морфологические изменения венечных сосудов у больных со стабильной стенокардией весьма вариабельны. В одних случаях имеется более или менее выраженный фиксированный стеноз проксимальной КА, обусловленный атеросклеротической бляшкой, суживающей просвет артерии. В других случаях атеросклеротическое сужение крупных КА по данным КАГ может быть минимальным или даже отсутствовать совсем. Не исключено, что в этих случаях спазм КА происходит на уровне мелких интрамуральных (резистивных) венечных сосудов, морфологические изменения которых обычно не фиксируются при КАГ.
Механизмы возникновения спазма КА были описаны выше. При спонтанной вазоспастической стенокардии основное значение имеет нарушение функции эндотелия коронарных сосудов, повреждение которого способствует усиленной выработке мощного вазоконстриктора — эндотелина и, наоборот, уменьшению синтеза основного эндотелийзависимого вазодилатирующего фактора — оксида азота (NО), а также снижению выработки простациклина.
Значение имеют и другие вазоконстрикторные субстанции, выделяющиеся тромбоцитами, адгезированными и агрегированными в области повреждения сосудистого эндотелия (тромбоксан А2, серотонин и др.).
Активация САС и возбуждение α-адренорецепторов коронарных сосудов играет, по-видимому, существенно меньшую роль в возникновении спазма КА, тем более что прием ингибиторов a-адренорецепторов обычно не купирует приступ вазоспастической стенокардии.
| 5.5.2. Клиническая картина |

|
Клинические проявления спонтанной (вариантной) стенокардии Принцметала имеют некоторые особенности, отличающие ее от типичной стенокардии напряжения.
Интенсивные болевые приступы возникают в покое, чаще ночью во время сна, или в ранние утренние часы (от 4 до 6 ч утра). Болевым приступам обычно не предшествуют какие-либо явные провоцирующие факторы, в том числе те, которые сопровождаются повышением потребности миокарда в кислороде (увеличение ЧСС, подъем АД и др.).
Боли, как правило, локализуются за грудиной и иррадиируют в левую руку, плечо и лопатку. Продолжительность боли может быть различной — от 5–10 мин до 20–30 мин. Нередко на фоне болевого приступа возникает брадикардия. Тахикардия может появиться на высоте приступа или в конце его, но лишь как следствие рефлекторной активации САС в ответ на боль, пробуждение или прием нитроглицерина.
Боли могут сопровождаться одышкой, слабостью, потливостью, головокружением, что указывает на снижение сократимости ЛЖ и выраженные вегетативные расстройства. Прием нитроглицерина не всегда купирует боль и облегчает состояние больного. Хороший эффект получают от применения блокаторов медленных кальциевых каналов группы нифедипина.
Другими частыми проявлениями вариантной стенокардии являются нарушения ритма и проводимости, возникающие во время ангинозного приступа и обусловленные выраженной электрической нестабильностью ишемизированной сердечной мышцы и замедлением проводимости. У больного во время приступа вариантной стенокардии могут развиться преходящие внутрижелудочковые и атриовентрикулярные блокады, частая желудочковая экстрасистолия высоких градаций, пароксизмальная тахикардия или даже фибрилляция желудочков. Внезапное формирование АВ-блокады II или III степени, остановка синусового узла могут сопровождаться синкопальными состояниями.
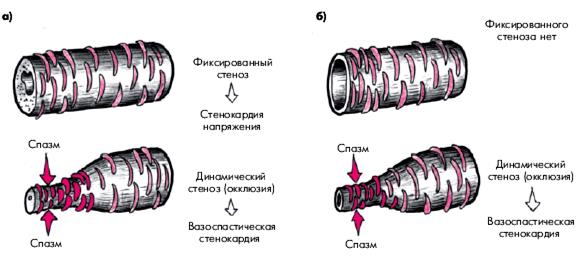
Можно выделить по меньшей мере два клинических варианта течения ИБС у больных со стенокардией Принцметала (рис. 5.51). У половины больных с наличием фиксированного стеноза КА ночные приступы спонтанной стенокардии (спазм) сочетаются с типичной стенокардией напряжения, обусловленной фиксированным стенозом КА и повышением потребности миокарда в кислороде. В этих случаях приступы стенокардии напряжения возникают в дневные часы и обычно провоцируются физической нагрузкой, психоэмоциональным напряжением, подъемом АД, тогда как приступы вариантной стенокардии, обусловленные спазмом КА, возникают спонтанно ночью или под утро (рис. 5.51, а). Толерантность к физической нагрузке у таких больных может быть существенно снижена из-за наличия стеноза КА.
Особенно пристального внимания заслуживают случаи, когда у больного, страдающего стенокардией напряжения, впервые появляются описанные приступы спонтанной стенокардии, что обычно указывает на обострение ИБС, вызванное формированием осложненной атеросклеротической бляшки (нестабильная стенокардия).
У другой части больных, преимущественно у лиц сравнительно молодого возраста, у которых отсутствует гемодинамически значимое сужение КА, спонтанная вазоспастическая стенокардия может быть единственным клиническим проявлением ИБС, а стенокардия напряжения отсутствует (рис. 5.51, б). Для таких больных, как правило, характерна сравнительно хорошая переносимость физических нагрузок.
Физикальные данные у больных вазоспастической стенокардией могут быть самыми разнообразными. Нередко они напоминают таковые при стабильной стенокардии напряжения.
| ||
| Рис. 5.51. Два клинических варианта течения ИБС у больных с вазоспастической стенокардией Принцметала: а — при сочетании фиксированного и динамического стеноза; б — при «чистом» динамическом стенозе | ||
| 5.5.3. Лабораторная и инструментальная диагностика | ||

| ||
Электрокардиография
Наиболее характерным электрокардиографическим признаком спонтанной (вариантной) стенокардии является подъем сегмента RS–Т выше изолинии, свидетельствующий о наличии выраженной трансмуральной ишемии миокарда, обусловленной преходящей динамической окклюзией КА (рис. 5.52). В более редких случаях наблюдается ишемическая депрессия сегмента RS–Т ниже изолинии, что указывает на возникновение субэндокардиальной ишемии, обусловленной неполным перекрытием крупной КА или спазмом более мелких интрамуральных венечных сосудов (мелких артерий и артериол) при хорошем развитии коллатералей. После купирования приступа вазоспатической стенокардии сегмент RS–Т возвращается к изоэлектрической линии (рис. 5.53).
| Рис. 5.52. Изменения ЭКГ при приступе вазоспастической стенокардии Принцметала. Красным цветом обозначена трансмуральная ишемия миокарда, возникающая в результате спазма коронарной артерии | 
|
| Рис. 5.53. Фрагменты холтеровской записи ЭКГ больного с вариантной стенокардией (стенокардией Принцметала): а — исходная ЭКГ (вне приступа); б — ЭКГ во время приступа вазоспастической стенокардии | 
|
Суточное мониторирование ЭКГ по Холтеру
Особенно большое значение для диагностики вазоспастической стенокардии Принцметала имеет метод холтеровского длительного ЭКГ-мониторирования. На ЭКГ во время приступов вариантной стенокардии чаще наблюдается внезапный подъем сегмента RS–T выше изолинии (трансмуральная ишемия), хотя в отдельных случаях может встречаться и его депрессия (субэндокардиальная ишемия). Важно, что эти изменения сегмента RS–T, так же как и приступы стенокардии, развиваются в покое, чаще ночью, и не сопровождаются (по крайней мере, в начале приступа) увеличением ЧСС более чем на 5 ударов в минуту. Это принципиально отличает вазоспастическую стенокардию от приступов стенокардии напряжения, обусловленных повышением потребности миокарда в кислороде. Мало того, приступ вазоспастической стенокардии и ЭКГ-признаки ишемии миокарда могут исчезнуть, несмотря на увеличение ЧСС, обусловленное рефлекторной реакцией на боль, пробуждение и/или прием нитроглицерина (феномен “прохождения через боль”).
Непрерывная запись ЭКГ позволяет выявить еще один важный отличительный признак стенокардии Принцметала: смещение сегмента RS–T в начале приступа происходит очень быстро, скачкообразно и так же быстро исчезает после окончания спастической реакции. Для стенокардии напряжения, наоборот, характерно плавное постепенное смещение сегмента RS–T при повышении потребности миокарда в кислороде (увеличении ЧСС) и столь же медленное возвращение его к исходному уровню после купирования приступа.
Функциональные нагрузочные тесты
У значительного числа больных с вазоспастической формой стенокардии пробы с дозированной физической нагрузкой оказываются отрицательными. Это связано с отсутствием у этих пациентов гемодинамически значимого органического сужения просвета венечных сосудов, а также с тем, что физическая нагрузка и увеличение ЧСС достаточно редко могут спровоцировать приступ вариантной стенокардии, сопровождающейся выраженным спазмом КА.
Только у  больных на высоте нагрузки удается спровоцировать приступ вазоспастической стенокардии и/или подъем сегмента RS–Т. Чрезвычайно характерным для таких случаев является постоянное, изо дня в день и даже в течение одного дня, колебание толерантности к физической нагрузке, т.е. быстрое изменение степени коронарного резерва. Такие колебания обусловлены постоянно меняющимся тонусом КА и, соответственно, степенью динамической обструкции просвета сосуда, которая как бы “добавляется” к величине фиксированного стеноза венечного сосуда, обусловленного органическим стенозом.
больных на высоте нагрузки удается спровоцировать приступ вазоспастической стенокардии и/или подъем сегмента RS–Т. Чрезвычайно характерным для таких случаев является постоянное, изо дня в день и даже в течение одного дня, колебание толерантности к физической нагрузке, т.е. быстрое изменение степени коронарного резерва. Такие колебания обусловлены постоянно меняющимся тонусом КА и, соответственно, степенью динамической обструкции просвета сосуда, которая как бы “добавляется” к величине фиксированного стеноза венечного сосуда, обусловленного органическим стенозом.
Следующие функциональные пробы используют для провокации спазма КА.
Холодовая проба. Руку пациента до середины предплечья помещают на 3–5 мин в воду, охлажденную до температуры +4°С. ЭКГ регистрируют в течение 10 мин после окончания холодового воздействия. Проба отличается низкой чувствительностью, поскольку ишемические изменения сегмента RS–Т выявляются примерно у 15–20% больных вазоспастической стенокардией.
Пробу с эргометрином(см. выше) считают наиболее адекватной для выявления вазоспастических реакций, в частности, у больных ИБС, у которых во время коронароангиографии не обнаруживается стенозирование КА. Проба с эргометрином опасна развитием тяжелых осложнений (ИМ, внезапная смерть, желудочковые аритмии), в связи с чем она используется для диагностики ИБС только в специализированных научно-исследовательских учреждениях (Д.М. Аронов с соавт., 1996).
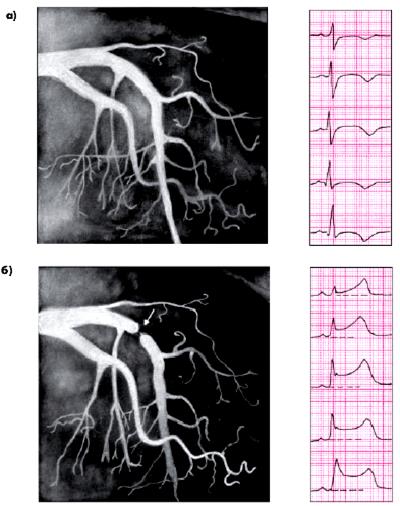
На рис. 5.54 приведены ЭКГ и КАГ больного с выраженным спазмом КА, возникшим во время эргометринового теста.
| ||
| Рис. 5.54. Коронароангиограмма, зарегистрированная у больного ИБС с вазоспастической стенокардией до (а) и во время (б) эргометринового теста. После введения эргометрина наблюдается выраженный спазм проксимальной части передней межжелудочковой ветви (ПМЖВ) левой коронарной артерии (динамическая окклюзия) | ||
| 5.5.4. Лечение | ||

| ||
Основой медикаментозной терапии больных вазоспастической стенокардией Принцметала являются блокаторы медленных кальциевых каналов. Эффективными могут оказаться любые препараты группы верапамила, нифедипина или дилтиазема, в том числе их сочетание. Предпочтительно использовать антагонисты кальция пролонгированного действия (ретардные формы).
Приступы ночной стенокардии покоя обычно купируются приемом нитроглицерина. В этих случаях нитроглицерин выступает как артериолярный вазодилататор, устраняющий спазм КА. Его влияние на венозный возврат крови и величину преднагрузки при вариантной стенокардии большого значения не имеет, за исключением тех случаев, когда динамический стеноз КА (спазм) возникает на фоне одновременно существующего фиксированного стеноза, обусловленного атеросклеротической бляшкой, суживающей просвет сосуда.
Для профилактики приступов вазоспастической стенокардии Принцметала используют нитраты пролонгированного действия. При этом следует помнить, что в большинстве случаев необходимо предусмотреть прием нитратов в вечернее время, а не утром и днем, как при стабильной стенокардии напряжения. Возможна комбинация ретардных форм нитратов с одним или даже двумя блокаторами медленных кальциевых каналов, например нитраты + нифедипин + верапамил или нитраты + нифедипин + дилтиазем.
В некоторых случаях целесообразно применение блокаторов a-адренорецепторов, например празозина или доксазозина (подробное описание этих ЛС приведено в главе 7).
Следует помнить, что в отличие от больных стабильной стенокардией напряжения, у пациентов с вазоспастической стенокардией применение b-адреноблокаторов может резко ухудшить состояние. Это объясняется тем, что блокада b-адренорецепторов может способствовать преобладанию a-адренергической стимуляции КА, которая приводит к возникновению спазма.
Для профилактики острого коронарного синдрома у больных вазоспастической стенокардией Принцметала целесообразно использовать курантил, обладающий не только мощным антитромбоцитарным эффектом, но и выраженными вазодилатационными свойствами. Препарат принимают в дозе 225 мг в сутки.
Хирургическое лечение больных со стенокардией Принцметала, как правило, неэффективно. Склонные к спазму КА очень чувствительны к различным механическим манипуляциям. Поэтому у таких пациентов любое оперативное вмешательство может привести к развитию ИМ и жизнеопасных желудочковых аритмий. Только в тех случаях, когда органическое сужение КА явно преобладает, и спазм развивается в области атеросклеротического стеноза, следует рассмотреть вопрос о возможности проведения ангиопластики со стентированием или аортокоронарного шунтирования.
| 5.5.5. Прогноз |

|
Прогноз при вариантной стенокардии определяется двумя основными факторами:
- степенью фиксированной (органической) коронарной обструкции;
- наличием или отсутствием осложненной атеросклеротической бляшки в КА, ведущей к дестабилизации ИБС и повышению риска развития ИМ и внезапной сердечной смерти.
Если у больного имеют место тяжелые, длительные или впервые возникшие и повторяющиеся приступы стенокардии Принцметала, которые могут быть отнесены к нестабильной стенокардии, прогноз достаточно серьезен: у 20–25% больных в течение 3-х месяцев развивается ИМ или наступает внезапная сердечная смерть.
При стабильном характере вариантной стенокардии редкие и легко купирующиеся болевые приступы под влиянием лечения прекращаются, иногда на многие годы, и прогноз определяется степенью коронарной обструкции и числом пораженных КА. 7-летняя выживаемость таких больных достигает 97%.
| 5.6. Безболевая ишемия миокарда |

|
Безболевая ишемия миокарда (БИМ) — это эпизоды транзиторной кратковременной ишемии сердечной мышцы, объективно выявляемые с помощью некоторых инструментальных методов исследования, но не сопровождающиеся приступами стенокардии или ее эквивалентами.
Феномен БИМ обнаруживается не менее чем у 2/3 больных ИБС со стабильной и нестабильной стенокардией и у 1/3 больных с постинфарктным кардиосклерозом. В большинстве случаев у одного и того же больного наблюдается сочетание как безболевой ишемии миокарда, так и болевых ангинозных приступов (стенокардии). Причем, лишь небольшая часть эпизодов преходящей ишемии сопровождаются приступами стенокардии (не более чем 20–25% от общего числа эпизодов ишемии), тогда как на долю БИМ приходится около 75–80%.
Дата добавления: 2015-08-04; просмотров: 667;
