Химические свойства. 1. Аминокислоты — это органические амфотерные соединения
1. Аминокислоты — это органические амфотерные соединения. Они содержат в составе молекулы две функциональные группы противоположного характера: аминогруппу с основными свойствами и карбоксильную группу с кислотными свойствами. Аминокислоты реагируют как с кислотами, так и с основаниями:
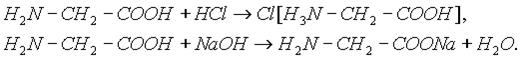
При растворении аминокислот в воде карбоксильная группа отщепляет ион водорода, который может присоединиться к аминогруппе. При этом образуется внутренняя соль, молекула которой представляет собой биполярный ион, который называется цвиттер-ионом:
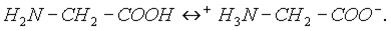
Кислотно-основные превращения аминокислот в различных средах можно изобразить следующей схемой:
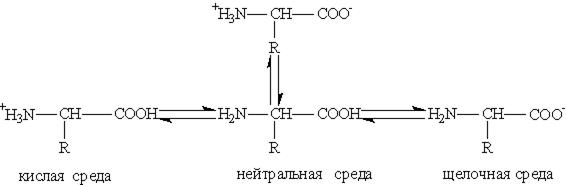
Водные растворы аминокислот имеют нейтральную, щелочную или кислую среду в зависимости от количества функциональных групп. Так, глутаминовая кислота образует кислый раствор (две группы —СООН, одна —NH2), лизин — щелочной (одна группа —СООН, две —NH2).
2. Трансаминирование - одна из реакций метаболизма аминокислот, которая заключается в переносе аминогруппы (NH2) из аминокислоты в кетокислоты; в результате образуется другая кетокислота и аминокислота.
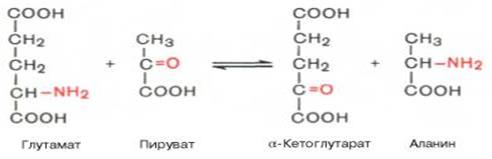
3. Дезаминирование - этоотщепление аминогруппы (—NH2) из молекулы органического соединения.
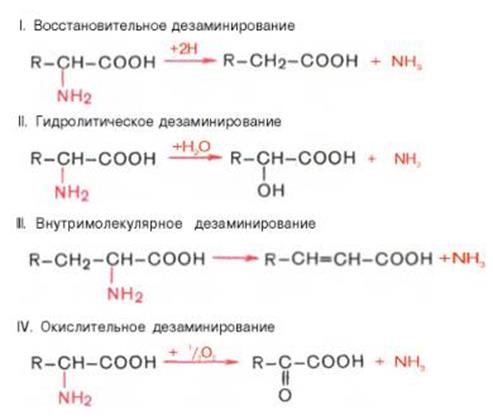
Дезаминирование играет важную роль в процессах обмена веществ, в частности в катаболизме аминокислот. Доказано существование 4 типов дезаминирования аминокислот (отщепление аминогруппы). Выделены соответствующие ферментные системы, катализирующие эти реакции, и идентифицированы продукты реакции. Во всех случаях NH2-группа аминокислоты освобождается в виде аммиака.
4. Декарбоксилирование– это процесс отщепления карбоксильной группы аминокислот в виде СО2 получил название декарбоксилирования. Несмотря на ограниченный круг аминокислот и их производных, подвергающихся декарбоксилированию в животных тканях, образующиеся продукты реакции – биогенные амины – оказывают сильное фармакологическое действие на множество физиологических функций человека и животных. Например, в животных тканях с высокой скоростью протекает декарбоксилирование гистидина под действием специфической декарбоксилазы.
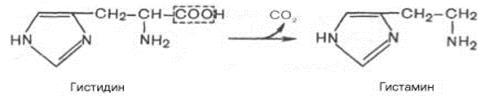
Гистамин оказывает широкий спектр биологического действия. По механизму действия на кровеносные сосуды он резко отличается от других биогенных аминов, так как обладает сосудорасширяющим свойством. Большое количество гистамина образуется в области воспаления, что имеет определенный биологический смысл. Вызывая расширение сосудов в очаге воспаления, гистамин тем самым ускоряет приток лейкоцитов, способствуя активации защитных сил организма. Кроме того, гистамин участвует в секреции соляной кислоты в желудке, что широко используется в клинике при изучении секреторной деятельности желудка (гистаминовая проба). Он имеет прямое отношение к явлениям сенсибилизации и десенсибилизации. При повышенной чувствительности к гистамину в клинике используют антигистаминные препараты (санорин, димедрол и др.), оказывающие влияние на рецепторы сосудов. Гистамину приписывают также роль медиатора боли.
5. Превращения аминокислот при нагревании. α-Аминокислоты, а еще легче их эфиры, при нагревании образуют циклические пептиды — дикетопиперазины:
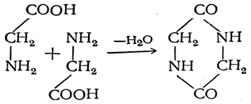
β-Аминокислоты при нагревании образуют α,β-ненасыщенные кислоты с отщеплением аминогруппы и водорода от соседних атомов углерода:
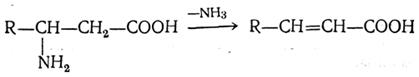
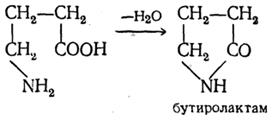
γ-, δ- и ε-Аминокислоты, как и соответствующие оксикислоты, легко отщепляют воду и циклизуются, образуя внутренние амиды — лактамы:
6. Качественные реакции на аминокислоты.Качественные (цветные) реакции аминокислот сохранили свое важное значение до настоящего времени. Общая качественная реакция α-аминокислот – это реакция с нингидрином. Все аминокислоты окисляются нингидрином с образованием продуктов, окрашенных в сине-фиолетовый цвет. Эта реакция может быть использована для количественного определения аминокислот спектрофотометрическим методом.
Для обнаружения пептидных связей в пептидах и белках служит биуретовая реакция. Для обнаружения ароматических и гетероциклических альфа-аминокислот используют ксантопротеиновую реакцию. (от греч. ксантос — желтый). При нагревании ароматических аминокислот с концентрированной азотной кислотой происходит нитрование бензольного кольца и образуются соединения, окрашенные в желтый цвет.
Дата добавления: 2015-08-04; просмотров: 1418;
