Наркомании и опиатные системы мозга
Представление о том, что в головном мозге человека и животных могут существовать нейроны («клетки-мишени»), обладающие способностью каким-то образом связываться с наркотическими веществами, в первую очередь с наркотиками опиатного происхождения, и под их воздействием изменять свои нормальные физиологические функции, существовало среди физиологов и фармакологов достаточно давно. Однако логика научного мышления неизбежно обусловливала следующий вопрос: если такие нейроны существуют, то какова их роль в нормальном организме? Невозможно предположить, что эволюция таким образом «позаботилась» о незначительной части рода человеческого, пристрастившейся к наркотикам. Что же касается животных, то естественной наркомании среди них до сих пор не замечено. Животные становятся наркоманами только по воле экспериментатора. Следовательно, и в нормальном, не отравленном наркотиками организме, должны существовать вещества, по своим физиологическим или химическим свойствам близкие к опиатам. После того, как экспериментальная медицина получила в свои руки тонкие биохимические и радиоиммунные методы анализа, такие вещества были найдены. Логика восторжествовала, а эволюция осталась неопороченной.
В 1975 г. два шотландских исследователя X. Костерлиц и Р. Хьюз обнаружили в экстрактах мозга вещества, обладающее опиатной активностью. Дальнейшие исследования позволили установить химическую структуру этих веществ. Они оказались пептидами, получившими названиеопиоидных нейропептидов(эндогенные морфиноподобные соединения) и подразделяющиеся на две основные группы: энкефалины (короткие пентапептиды) иэндорфины (пептиды с более длинной цепочкой, состоящей из 16-31 аминокислот).
В зависимости от порядка соединения аминокислот и длины аминокислотной цепочки эти соединения классифицируются следующим образом:α-эндорфин, (3-эндорфин, β-эндорфин - группа эндорфинов; метионии-энкефалин (метэнкефалин); лейцин-энкефалин (лейэнкефалин) - группа энкефалинов.
Кроме того, в экстрактах мозга были найдены и некоторые другие, до настоящего времени неидентифицированные по своей химической структуре нейропептиды, также обладающие опиатной активностью (например, пептиды полосатого тела, пептиды цереброспинальной жидкости и др.).
Рассматривая опиатную систему мозга, а то, что такая система, вернее, системы есть, сомневаться не приходится, следует честь и еще одно обстоятельство. В центральной нервной системе имеются нейроны, существенно изменяющие свои функции под влиянием опиоидных нейропептидов. Там же наличествуют нейроны, выделяющие эти нейропептиды. Оба вида нейронов тесно связаны между собой и чаще всего функционируют в пределах одних и тех же нервных центров. Как правило, один и тот же нейрон является и продуцентом нейропептида и его «мишенью». Но, как уже было указано выше, возможно существование и нейронов – «мишеней» опиоидных нейропептидов, не являющихся их продуцентами. Следует также иметь в виду, что «мишенью» определенного нейропептида является не весь нейрон, а весьма незначительная по протяженности часть его наружной мембраны – так называемый рецептор. По существу рецептор представляет собой сложную биомолекулу, способную специфически связываться только с определенным химическим веществом – лигандом данного рецептора. Для опиатных рецепторов такими лигандами, с одной стороны, являются эндорфины и энкефалины, а с другой – наркотические вещества опиатной природы или искусственно синтезированные лекарственные соединения. Роль рецептора заключается в том, чтобы трансформировать полученную информацию (ее несет лиганд) в биологический ответ (нервное возбуждение, нервное торможение – эффекторная посылка на исполняющий орган).
Наибольшее число клеток, продуцирующих эндорфины, расположено в гипоталамусе. Аксоны этих нейронов распределяются внутри гипоталамуса или направляются к перегородке и ядрам миндалины. Некоторые аксоны направляются в ствол мозга, к структурам голубого пятна и ядрам шва. Продуцентов энкефалинов в центральной нервной системе значительно больше. Кроме того, энкефалины найдены и в периферической нервной системе, в вегетативных системах внутриорганной регуляции функций.
Даже предварительное ознакомление со схемой распределения эндорфинов в структурах головного мозга наводит на мысль о ее схожести со схемой взаимодействия эмоциональных центров. В дальнейшем это предположение нашло свое подтверждение и в экспериментальной практике. Внутривенное и внутримозговое введение экспериментальным животным эндорфинов вызывало у них позитивные эмоциональные состояния и реакцию пристрастия (при самовведении по методике, изложенной ранее). Сходство эндогенных опиоидов и их экзогенных аналогов подтверждается и их влиянием на болевую чувствительность. И те, и другие снижают или модулируют ноцицепцию. Кстати, именно это свойство наркотических анальгетиков, несмотря на опасность развития реакции привыкания и пристрастия, заставляет врачей до сих пор широко применять наркотики в клинике. В последние годы появились сведения и о том, что эндогенные опиоиды принимают самое непосредственное участие в формировании мотиваций и в системе памяти. Энкефалины, так же как и эндорфины, обладают множеством физиологических функций. Среди них можно выделить регуляцию висцеральных рефлексов и эндокринных функций головного мозга; они вызывают кратковременный аналгезирующий эффект, активируют систему положительного подкрепления, обладают эйфоризирующим действием.
Заканчивая описание свойств эндогенных опиоидов, следует указать, что они продуцируются в ничтожных количествах и достаточно быстро дезактивируются соответствующими ферментными системами.
Клеточные и нейрогуморальные механизмы патогенеза наркомании
В нормальном организме опиоидные нейропептиды выполняют чрезвычайно важную функцию – соблюдение баланса между «старт- и стоп-зонами» головного мозга, между системами «наказания» (отрицательные эмоции) и «удовольствия» (положительные эмоции). Учитывая, что подавляющее большинство биологических процессов в организме подвержено хронобиологической регуляции, не удивительно, что каждый человек, даже без видимых и очевидных причин, испытывает периоды приподнятого или несколько угнетенного настроения. В первом случае – это может быть результатом повышенной продукции эндогенных опиоидов, во втором – следствием снижения интенсивности их синтеза или чрезмерной дезактивации. Конечно, эта схема несколько несколько примитивна для объяснения сложных процессов, лежащих в основе психической деятельности человека, но отрицать участие опиоидов в формировании психофизиологических свойств личности было бы наивно.
Однако важно учитывать следующее обстоятельство. Определенное число людей становятся наркоманами и алкоголиками именно потому, что в период длительной депрессии, вызванной и чисто внутренними (биологическими) и внешними (социальными) причинами, они попробовали купировать это состояние приемом дозы наркотика, алкоголя, психостимулятора или небрежно, без совета врача, воспользовались каким-либо психотропным медикаментозным средством антидепрессантного характера. В данном случае естественный относительный или абсолютный недостаток эндогенных опиоидов возмещается их экзогенным агонистом, и при этом в дозе, в сотни или тысячи раз превышающей объем естественной продукции этих нейропептидов. Мощное эйфоризирующее действие наркотика резко сдвигает баланс эмоционального состояния в сторону позитивной эмоции. Человек хорошо запоминает свои ощущения, но изменение психофизиологического гомеостаза «запоминает» и система эмоциональных центров. Далее возможно замыкание цепи патогенетических механизмов наркомании.
В изложенном ранее материале достаточно подробно обсуждалась роль позитивно-эмоциональных механизмов, их положительно подкрепляющее воздействие в развитии реакции привыкания и пристрастия к наркотическим веществам. Несомненным является участие и опиатных систем мозга в регуляции определенных эмоциональных состояний, как нормального организма, так и подвергнувшегося регулярному воздействию экзогенных опиатных агонистов. Однако далеко не все наркомании связаны с употреблением опиума и его производных (морфина, диацетилморфина, кодеина, дилаудида, тебаина и др.). Многие наркомании обусловлены развитием реакций привыкания и пристрастия и в дальнейшем - психической и физиологической зависимости к веществам, которые по своей химической природе не имеют ничего общего с опиатами. Таковыми, например, являются психомоторные стимуляторы (фенамин, фенатин, кокаин и его производные), депрессанты ЦНС, основное место среди которых занимает, конечно, этанол, а также барбитураты: некоторые медикаментозные средства антидепрессантного действия. У всех этих веществ, так разнящихся друг от друга по химическому составу, есть одно общее свойство: все они характеризуются возможностью влиять на эмоциональную сферу человека. Иначе говоря, все эти вещества обладаютгедоническим эффектом воздействия на психику, т. е. способностью вызывать эйфорию, приятные ощущения.
Для изучения и обоснования механизмов патогенеза наркомании в принципе неважно, благодаря чему возникает гедонический эффект: за счет возбуждения центров положительных эмоций или временной дезактивации эмоционально отрицательных структур головного мозга. Поэтому мы проанализируем интимные процессы, лежащие в основе развития реакции привыкания и пристрастия к опиатам экзогенного происхождения, на примере их воздействия на «стоп-зоны» ЦНС (рис. 1).
Для простоты объяснения условимся, что мы рассматриваем интегративную деятельность только одного нейрона, входящего в состав эмоционально-негативного центра. Каждый нейрон имеет огромное количество рецепторных образований, часть из которых является опиатными рецепторами. В норме некоторое количество опиатных рецепторов постоянно связано с эндогенными опиатами. Если учесть, что опиатный рецептор, как правило, входит в состав постсинаптической мембраны какого-либо синаптического образования и благодаря этому участвует в регуляции данной синаптической связи, можно понять, что таким образом он влияет на возможность нейрона получать информацию. Если большинство или значительная часть опиатных рецепторов связана эндогенными опиоидами (опиоидными нейропептидами), то может возникнуть ситуация, при которой деятельность нейрона изменяется и он, равно как и его соседи по конгломерации нейронов, становится неспособным выполнять свою основную функцию – генерировать возбуждение, которое в конечном итоге воспринимается организмом как отрицательная эмоция.
В балансе позитивных и отрицательных эмоциональных центров маятник эмоционального состояния смещается в сторону положительных эмоций, и организм испытывает чувство эйфории или других приятных ощущений (рис. 1 а). Однако в силу недостаточной продукции или усиленного разрушения эндогенных опиоидов соответствующими ферментными системами число «блокированных» опиатных рецепторов может резко уменьшиться. В результате возрастает возбуждение конгломерации нейронов, входящих в состав «стоп-зоны» головного мозга. Нарушается эмоциональный баланс, и отрицательные эмоции начинают превалировать (рис. 1 б). Возникновение в этот момент внешнего фактора, несущего негативную информацию для организма, может многократно усилить отрицательную эмоцию.
У человека с сильным типом высшей нервной деятельности это состояние побудит стремление к борьбе, преодолению возникших трудностей. Слабый тип ВНД будет диктовать свои способы трансформации негативных эмоциональных состояний, в том числе и за счет потребления веществ, являющихся агонистами опиоидных нейропептидов. В силу их высокой концентрации во внутренней среде организма они чрезвычайно быстро блокируют опиатные рецепторы и возвращают человеку положительное эмоциональное состояние (рис.1 в). Подобное качание «эмоционального маятника» не приводило бы к печальным последствиям, не вызывало бы психической и физической зависимости от наркотика, если бы каждый нейрон, каждый эмоциональный центр не был саморегулирующейся системой, активно реагирующей на изменение гомеостаза.
В действительности каждое новое введение в организм экзогенных заменителей опиоидных нейропептидов приводит к тому, что нейрон (точнее, нейроны, их конгломерация), находясь под контролем экзогенных опиатов, начинает адаптироваться к их воздействию и стремиться возобновить свою нормальную функцию, но на новом уровне регуляции. Предположительно эта адаптация осуществляется за счет пролиферации, увеличения количества опиатных рецепторов (рис. 88-г)
И тогда вновь возникает ситуация, при которой значительная часть опиатных рецепторов остается свободной, не связанной как эндогенными, так и экзогенными опиатами. Следует добавить, что по закону обратной связи длительное присутствие в организме суррогатных заменителей эндогенных опиоидов отрицательно сказывается на их синтезе, а дезактивирующие ферментные системы, наоборот, – повышенно активируются. В результате возникают два новых патофизиологических процесса:усиление синдрома абстиненции и толерантность к наркотическому веществу. Наркоман должен увеличивать дозу наркотического вещества, а промежутки между его приемами сокращаются. Так медленно, а затем все быстрее закручивается спираль патологического процесса, пока, наконец, функциональные изменения в ЦНС не перейдут в органические. Таким путем формируется вначале психическая, а затем и физическая зависимость от наркотика.
Для полной ясности следует указать, что аналогичным образом развиваются процессы адаптации к наркотикам нейронов эмоционально-позитивных центров. Разница заключается только в том, что контакт опиоидных нейропептидов или экзогенных опиатов с опиатными рецепторами вызывает повышенную возбудимость нейронов и тем самым обеспечивает генерацию положительных эмоциональных состояний. Адаптация же конгломерации нейронов к экзогенным опиатам осуществляется за счет уменьшения числа опиатных рецепторов.
Выше указывалось на разнообразие видов наркомании. Однако этапность патологических процессов, определяющая их формирование, имеет много общих черт.
Каждая наркомания начинается со стимуляции позитивно-эмоциональных реакций, за счет чего вначале возникает привыкание и пристрастие. Следом идет психическая зависимость, сопровождаемая такими явлениями, как абстиненция и толерантность к наркотику. Завершают цикл патологических изменений в организме физическая зависимость от наркотика и органические изменения органов и тканей. Таким образом, несмотря на различие в химическом строении, все вещества, вызывающие формирование зависимости организма, должны иметь близкие точки приложения в соответствующих нейрональных системах регуляции функций.
Исследования подтверждают это предположение. Исполнительные системы, обеспечивающие формирование мотивации «получения награды», состоят из множества конгломераций нейронов, связанных между собой очень сложными нейрональными цепями. Тем не менее, эксперименты, проведенные на животных с применением методики самостимуляции и самовведения различных веществ, вызывающих зависимость, показали, что ведущую роль в развитии этой патологии играют две медиаторно-трансмиттерных системы: опиатная и адренергическая.
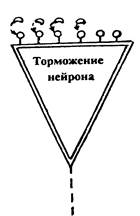

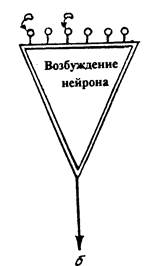
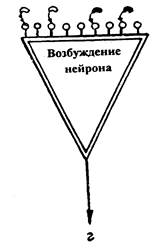

Рис.1. Схема, иллюстрирующая развитие процесса адаптации
нейрона к воздействию экзогенных опиатов.
Чаще всего предупредить развитие реакции зависимости у экспериментальных животных можно двумя способами: введением антагонистов эндогенных и экзогенных опиоидов (налоксон, налтрексон) или препаратов, обладающих антиадренергическими свойствами (бутироксан, нирроксан, карбидин и т. п.). Знание этих обстоятельств позволяет разработать примерную схему воздействия различных веществ (обладающих способностью вызывать синдром зависимости) на нейрональные элементы, обеспечивающие функционирование системы «награды» (системы положительного подкрепления).
Из анализа представленной схемы следует, что запуск нейрональной реакции положительного подкрепления может осуществляться несколькими путями. В первую очередь, это воздействие опийных препаратов и их синтетических аналогов на опиатные рецепторы. К веществам этого ряда в полной мере можно отнести и некоторые продукты метаболизма этанола. Кроме того, этанол и другие психодепрессанты (например, этами-нал натрия) обладают и своим, специфическим воздействием на мембраны нейронов, изменяя их ионную проводимость и в широких пределах варьируя возбудимость клетки. В свою очередь, психостимуляторы - кокаин, фенамин, фенатин и другие аналогичные по своему действию вещества влияют непосредственно на адренергические элементы нейрональных сетей, усиливая эффект катехоламинов. Точкой приложения электростимуляции (самостимуляции) в системе «награды» также являются адренергические элементы. Действие антидепрессантов и других подобных им психотропных веществ сосредоточено на нейрональных элементах центров отрицательных эмоций. Торможение этих центров сдвигает эмоциональное равновесие в сторону позитивных эмоций, т. е. опять же стимулирует систему положительного подкрепления и вызывает гедонический эффект.
Адаптация нейронов к длительному воздействию любого из перечисленных веществ переводит регуляцию их жизнедеятельности на новый, более высокий уровень. Механизмы этой адаптации могут быть различными, но в итоге человек, злоупотребляющий наркотиками или психотропными веществами, неизбежно приходит к постоянно усиливающемуся абстинентному синдрому, толерантности нервной системы к принимаемому веществу, физической зависимости от его приема. К этому можно добавить, что в результате длительного воздействия наркотиков, психостимуляторов и психотропных веществ на структуры ЦНС реорганизуется синаптоархитектоника нервных сетей, во многих отделах ЦНС на фоне повреждения и исчезновения синаптических образований организуются новые межнейрональные связи, не характерные для здорового, неповрежденного интоксикацией головного мозга.
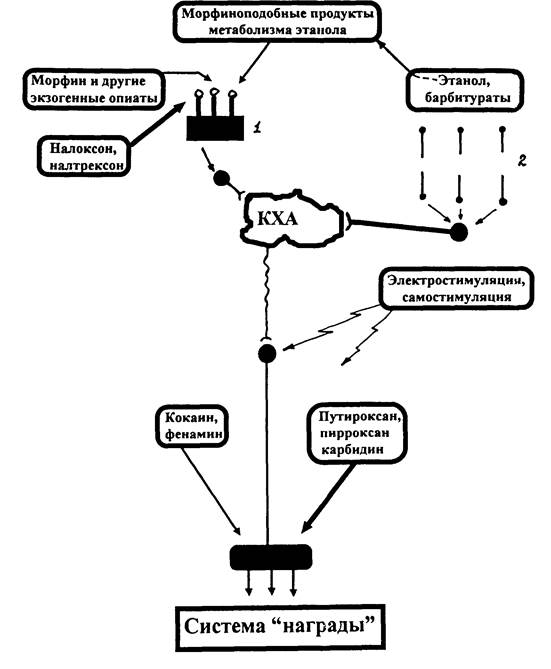
Рис. 2. Схема взаимодействия психоактивных веществ, способных вызвать наркогенную зависимость, и их антагонистов в нейрональных цепях, обеспечивающих функционирование системы «награды» (системы положительного подкрепления). 1 – опиатные рецепторы нейрона; 2 – мембрана нейрона; КХА-нейроны катехоламинергической системы. (По А.В. Вальдману, Э.А. Бабаян, Э.Э. Звартау, 1988)
Возникновение новых синаптических образований, а, следовательно, и создание новых нейрональных цепей и связей, извращение медиаторного механизма приводят к формированию патологических функциональных систем. Особое значение это явление имеет для структур ЦНС - высших вегетативных центров, регулирующих и координирующих деятельность внутренних органов и систем организма. Судя по всему, именно здесь лежат истоки множественных вегето-сомати-ческих изменений, характерных для клиники самых разнообразных наркомании.
Особое значение в формировании ряда патологических состояний, возникающих под влиянием наркотиков и психотропных веществ, имеет эндокринная система организма, изменяющая в этом случае свои нормальные функции. Клинические наблюдения и экспериментальная практика показывают, что даже относительно кратковременное потребление наркотиков (морфина, героина, метадона и некоторых других) вызывает значительное снижение половой функции. В крови экспериментальных животных уже при повторном введении опиатов наблюдается снижение концентрации тестостерона, лютеотропина. Данные экспериментов свидетельствуют о том, что точкой приложения опиатов в системе гипоталамус–гипофиз–половые железы являются биохимические системы, ответственные за синтез или высвобождение рилизинг-факторов, регулирующих деятельность половых желез, и действующие на гипоталамо-гипофизарном уровне. Наиболее сильное воздействие морфин и ему подобные вещества оказывают на половую сферу самцов экспериментальных животных. Так, значительное падение концентрации гормона лютеотропина в крови самцов крыс наступало при введении им морфина в ничтожной дозировке, даже не способной вызвать какой-либо заметный аналгезирующий эффект.
Под влиянием морфина и других опиатов происходит повышенное выделение соматотропина; по-видимому, это явление связано со стимулирующим воздействием опиатов на рилизинг-фактор соматотропина и с ингибицией ими соматостатина. Морфин и его производные способны вызывать антидиуретический эффект за счет значительного выброса в кровь вазопрессина. Судя по всему, в этом случае мы имеем дело с прямым воздействием опиатов на опиатные рецепторы супраоптического ядра гипоталамуса и нейросекреторных клеток промежуточной доли гипофиза, так как в экспериментах на животных введение налоксона (антагониста эндо- и экзогенных опиатов) снимало антидиуретическое действие морфина, а введение этого опиата непосредственно в супраоптическое ядро гипоталамуса активно его стимулировало.
Отмечено влияние наркотиков опиатной природы и на синтез гипофизом тиротропина. Даже однократное введение опиатов приводило к значительному понижению концентрации в крови этого гормона. Как и в предыдущих случаях, этот эффект объясняется прямым воздействием опиатов на гипоталамическую область, так как билатеральное разрушение медиальных ядер гипоталамуса полностью устраняло данный феномен.
Завершить анализ влияния опиатов на гормональную функцию гипоталамо-гипофизарной системы можно сведениями об их воздействии на продукцию кортикотропина, концентрация которого в крови и непосредственно в гипофизе экспериментальных животных под их влиянием достоверно снижается.
Имеются данные о возможном воздействии опиатов на другие гормональные системы, например на инкреторную функцию поджелудочной железы, которая под влиянием наркотиков значительно снижает выделение инсулина.
В нормальном организме существуют множественные обратные связи, управляющие как гормонопродукцией, так и образованием эндогенных опиоидов в структурах головного мозга. Известно, что стрессовая ситуация приводит не только к выбросу в кровь антистрессорных гормонов, но и способствует синтезу эндорфинов и энкефалинов, участие которых в антиноцицептивных реакциях и адаптации организма к действию стрессорных факторов в настоящее время бесспорно установлено. С другой стороны, гормоны и эндогенные опиоиды как бы уравновешивают друг друга, так как повышение концентрации гормонов в крови (во всяком случае, «тропных» гормонов гипофиза) снижает продукцию опиоидов и, наоборот, повышение синтеза опиоидов уменьшает образование гормонов. Однако в организме, находящемся в состоянии наркотической интоксикации, эти нормальные взаимоотношения резко нарушены. Постоянно поддерживаемая наркоманом высокая концентрация наркотика в крови извращает продукцию гормонов, а это, в свою очередь, весьма отрицательно сказывается на процессах метаболизма. К этому следует добавить и дисрегуляцию вегетативных функций за счет непосредственного действия наркотика на высшие центры регуляции нервной системой вегетативных функций. В результате в патологический процесс вовлекаются практически все органы и системы, что в конечном итоге полностью разрушает организм и приводит его к гибели. Именно поэтому очень важно не допустить развития крайних степеней наркомании, вмешаться в ее развитие еще тогда, когда функциональные нарушения регуляции жизнедеятельности не перешли роковой грани, за которой патологические процессы приобретают необратимый характер.
Дата добавления: 2015-08-04; просмотров: 3860;
