Ход определения. Подготовка пробы. Анализировать можно предварительно профильтрованную пробу или всю пробу вместе с присутствующим в ней осадком (в зависимости от поставленной
Подготовка пробы. Анализировать можно предварительно профильтрованную пробу или всю пробу вместе с присутствующим в ней осадком (в зависимости от поставленной цели). Фильтр надо предварительно промыть горячей водой и, проводя фильтрование, отбросить первую порцию (200 – 250 см3) фильтрата. Нельзя фильтровать сточную воду, содержащую вещества, которые могут улетучиваться во время фильтрования или окисляться кислородом воздуха. В таких случаях фильтрование заменяют продолжительным отстаиванием сточной воды и для анализа отбирают пипеткой верхний прозрачный слой.
Стандартизация титранта. Титр раствора соли Мора устанавливают по стандартному раствору бихромата калия. Берут 10 см3 стандартного раствора, разбавляют его дистиллированной водой до 250 см3, приливают 20 см3 концентрированной серной кислоты и дают остыть. Затем прибавляют 3 – 4 капли раствора ферроина или 5 – 10 капель раствора N – фенилантраниловой кислоты и титруют раствором соли Мора.
Определение дихроматной окисляемости.Отбирают такой объем анализируемой сточной воды, чтобы на окисление расходовалось не более 20 см3 стандартного раствора дихромата калия и чтобы в ней содержалось не более 40 мг хлорид-ионов, разбавляют до 50 см3 дистиллированной водой и переносят в круглодонную колбу вместимостью 300 см3. Прибавляют 1 г сульфата ртути (II), 5 см3 серной кислоты, перемешивают до растворения сульфата ртути, затем вливают 25,0 см3стандартного раствора дихромата калия. Очень осторожно, малыми порциями вливают 70 см3 серной кислоты, всыпают 0,4 – 0, 5 г сульфата серебра, вводят в колбу несколько стеклянных бусин или кусочков пемзы, закрывают пробкой, соединенной с обратным холодильником, и нагревают при слабом кипении 2 часа. Затем охлаждают, обмывают стенки холодильника 25 см3 дистиллированной воды и переносят содержимое этой колбы в коническую колбу вместимостью 500 см3, обмывая стенки первой колбы несколько раз дистиллированной водой. Добавив дистиллированную воду до объема 350 см3, вводят 3 – 4 капли раствора ферроина или 10 – 15 капель раствора N – фенилантраниловой кислоты и оттитровывают избыток дихромата титрованным ратвором соли Мора. При титровании раствор вначале приобретает фиолетовую окраску, а затем изумрудно-зеленую, что является сигналом окончания титрования.
Проводят холостой опыт; для этого берут 50 см3 дистиллированной воды и проводят ее через все ступени анализа.
Расчет.Химическое поглощение кислорода (ХПК), выраженное числом миллиграммов кислорода на 1 дм3 сточной воды, вычисляют по формуле:
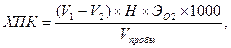
где V1–объем раствора соли Мора, израсходованного на титрование в холостом опыте, см3;
V2 – объем раствора соли Мора, израсходованного на титрование пробы, см3;
H – концентрация титрованного раствора соли Мора, моль-экв/дм3;
ЭО2–– эквивалент кислорода, 8 г/моль-экв.;
Vпробы – объем анализируемой сточной воды, см3;
1000– коэффициент для перехода от граммов к миллиграммам.
Дата добавления: 2015-08-04; просмотров: 1325;
