Химические свойства. Свойства спиртов определяются характером гидроксильной группы:
Свойства спиртов определяются характером гидроксильной группы:
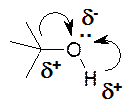
· электроноакцепторный атом кислорода сдвигает к себе электронную плотность связи О-Н, что приводит к появлению кислых свойств;
· аналогичный сдвиг к кислороду электронной плотности связи С-О приводит к появлению на спиртовом углероде частичного положительного заряда, что создает возможность атаки этого центра нуклеофильными реагентами;
· атом кислорода, богатый электронами, может выступать как в качестве основания, так и в качестве
· нуклеофила.
Спирты проявляют слабые кислотные свойства (они значительно слабее воды), поэтому классическая реакция со щелочами полностью сдвинута влево и образование алкоголятов в этих условиях не происходит.

Алкоголяты щелочных металлов получают растворением последних в спирте при комнатной температуре. Для получения алкголятов алюминия необходимо кипячение реакционной смеси.

Кислотность спиртов уменьшается в ряду:
метанол > первичные > вторичные > третичные.
Основность спиртов проявляется в образовании оксониевого катиона при взомодействии с сильными кислотами.
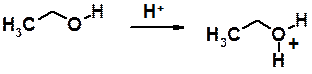
Способность спиртов образовывать оксониевые катионы, лежит в основе многих реакций, в которых плохую уходящую группу –ОН, в условиях реакции кислым катализом превращают в хорошую уходящую группу - Н2О.
Дегидратация спиртов (получение алкенов)
Реакция проходит под действием серной кислоты при нагревании. В спиртах, в отличие от галогеноалканов, элиминирование протекает по мономолекулрному механизму (Е1).
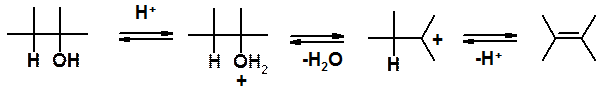
Нулеофильное замещение ОН-группы (получение галогеноалканов)
Особенности реакций нуклеофильного замещения подробно рассмотрены в разделе «Галогенопроизводные». Замещение гидрокси-группы на галоген – реакция обратная рассмотренной выше, проходящая по тем же основным закономерностям SN реакций. Замещение ОН-группы на галоген может быть выполнено несколькими путями. Самый простой, но не самый лучший (т.к. возможны перегруппировки и другие побочные реакции) – действием галогеноводородной кислоты на соответствующий спирт. Особенность превращения в том, что сначала происходит активация субстрата, посредством протонирования. В дальнейшем происходит замещение воды, а не ОН-группы.
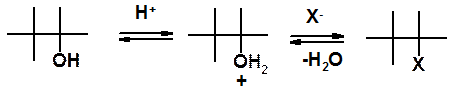
Первая стадия (атака протона) еще не нуклеофильное замещение. Это активация спирта. Вторая стадия – собственно нуклеофильное замещение.
Побочные реакции при замещении ОН-группы на галоген не наблюдаются при проведении замещения галогенидами фосфора.
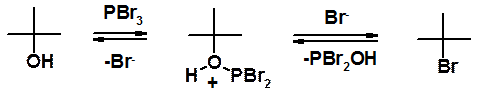
И в этой реакции нуклеофильное замещение только вторая стадия
Механизм конкретной реакции зависит от строения углеводородного радикала. Первичные спирты всегда вступают в реакцию SN2, третичные - SN1. Вторичные, в общем случае, могут реагировать по обоим механизмам. Бимолекулярные реакции идут с обращением конфигурации, мономолекулярные – с рацемизацией.
Очень хорошие результаты получены при использовании в качестве хлорирующего агента хористого тионила (SOCl2).

Важная особенность: реакция протекает с сохранением конфигурации. Т.е. если взять в реакцию энантиомерно чистый спирт, то в результате мы получим хлорпроизводное с той же самой абсолютной конфигурацией. Такие реакции носят название SNi (от internal – вниутримолекулярный).
Дата добавления: 2015-07-30; просмотров: 928;
