Поддержание эффективной гемодинамики
Характеристика кровообращения и его изменений в послеоперационном периоде должна основываться на разносторонней оценке сердечного выброса, регионального и тканевого кровотока, объемного транспорта крови и кислорода, ОЦК. Нарушения гемодинамики по шоковому типу характерны для больных, перенесших сложные реконструктивные вмешательства в черепно-лицевой области
ПОСЛЕОПЕРАЦИОННАЯ ИНТЕНСИВНАЯ ТЕРАПИЯ217
(гипертелоризм). Показатели кровообращения у них в ближайшем послеоперационном периоде достигают критического уровня, в связи с чем требуется проведение реанимационных мероприятий.
Система кровообращения обладает большими резервами для компенсации. Она достигается тахикардией, перераспределением крови, централизацией кровообращения, повышением экстракции кислорода. Реакцию кровообращения считают нормальной, если возрастают насосные параметры сердечной мышцы, ударный и минутный объем (здоровое сердце способно увеличить МОК до 12— 15 л/мин). Поддержание сердечного выброса в послеоперационном периоде обеспечивается активностью симпато-адреналовой системы. В то же время избыток адреналина способствует уменьшению производительности сердца при недостаточности транспорта кислорода в условиях тахикардии. При увеличении частоты сердечных сокращений уменьшается время диастолического наполнения желудочков (Дарбинян Т.М., 1979).
В установлении взаимосвязи параметров кровообращения у больных с высоким анестезиологическим риском большое значение имеют оценка и контроль центральной гемодинамики. Так, в покое у здорового человека с массой тела 70 кг (больные, поступающие на лечение по поводу деформаций челюстей, как правило, практически здоровы) сердечный выброс равен примерно 6 л/мин. При частоте сердечных сокращений (ЧСС) 72 в минуту ударный объем крови (УО) за одно сокращение составляет 83 мл. В ближайшем послеоперационном периоде, когда сердечнососудистая система функционирует в режиме гипер- и ги-подинамии, показатели кровообращения увеличиваются за счет увеличения ЧСС, увеличения диастолического и уменьшения конечного систолического объема.
Особое значение в системе контроля за центральной гемодинамикой в послеоперационном периоде имеет информация о производительности сердца в послеоперационном периоде, когда система кровообращения функционирует в разных режимах при наличии болей и кровопотери, чаще наблюдается уменьшение ударного объема кровообращения, а частоты сердечных сокращений не хватает для нормализации сердечного индекса (СИ). Тахикардия
| Глава 4 |
наиболее часто развивается в послеоперационном периоде в тех случаях, когда усиливается инотропизм сердечной мышцы, уменьшается длительность диастолы. Усиление инотропизма сердечной мышцы сопровождается изменением минутного объема кровообращения (МОК), который определяют по формуле:
МОК = ДО/Д! (Са02 — CvOs),
где AQ/ut — поглощение кислорода в минуту;
(СаОз — CvOz) — артерио-венозная разница по кислороду.
Функциональные возможности миокарда снижаются при сопутствующей соматической патологии, метаболических нарушениях и др. В большинстве случаев послеоперационные расстройства гемодинамики имеют субклинический характер (скрытая недостаточность кровообращения). В ближайшие сутки основными причинами циркуляторной гиподинамии являются гиповолемия и метаболические повреждения миокарда. Объем циркулирующей крови при гиповолемии представляет собой интегральную величину, которую особенно важно определить в послеоперационном периоде у больных, оперированных по поводу «сосудистых» новообразований.
Практически у каждого больного фиксируются проявления адаптации к нарушениям сердечного выброса, кислородного режима и гиповолемии. При проведении наркоза основная задача анестезиолога — сохранить механизмы компенсации за счет использования наиболее рациональной стратегии при лечении больного.
Гиповолемия — следствие массивной кровопотери и циркуляторной гиподинамии.
Существует мнение, что гиповолемия, развивающаяся после удаления сосудистых новообразований, является следствием недостаточного восполнения кровопотери. Исследования, проведенные с помощью серийной регистрации ОЦК после операции, показали, что замещение операционной кровопотери консервированной донорской кровью по принципу капля за каплей не предупреждает развитие гиповолемии. Вместе с тем известно, что наиболее выраженная гиповолемия наблюдается в послеоперационном периоде (Климанский В.А., Рудаев Я.А., 1984). Снижение параметров кровообращения у больных раком отражало недостаточность коронарного кровотока, свя-
ПОСЛЕОПЕРАЦИОННАЯ ИНТЕНСИВНАЯ ТЕРАПИЯ219
занную с нарушением метаболизма в сердечной мышце в результате кровопотери (Greenwalt T.J., 1981; Petz L.D., 1981). В послеоперационном периоде у больных с сосудистыми опухолями неизбежно возникал геморрагический и тромботический диатез в форме комплексного поражения тромбоцитарного и сосудистого компонентов гомеостаза. По существу это выражалось в развитии ДВС-синдрома, механизм развития которого заключается в нарушении регуляции агрегатного состояния крови в результате операции и кровопотери. Рассеянное внутрисосудистое свертывание крови в мелких сосудах и капиллярах вызывало гипоксию и явления ацидоза, которые могут принимать генерализованный характер, приводя организм к гибели. Диагностика ДВС-синдрома основывалась на выявлении геморрагического диатеза, низких концентраций фибриногена в крови, тромбоцитопении, что обусловлено «потреблением» тромбоцитов и фибриногена во внутрисосу-дистых сгустках крови. Снижение протромбинового индекса (менее чем на 50 %) и активности антитромбина-3 завершали клиническую картину ДВС-синдрома. Основные фазы этого синдрома в послеоперационном периоде у онкологических больных выглядели следующим образом:
— гиперкоагуляция характеризовалась повышением тестовых показателей свертывания крови, избытком плазменных субстратов фибриногена и протромбина;
— фаза гипокоагуляции и коагулопатии «потребления» проявлялась геморрагиями из мест повреждения тканей, которые приобретали характер генерализованно-го процесса. Эти нарушения явились следствием дефицита фибриногена, активизации процессов фибринолиза и про-теолиза, угнетения синтеза антитромбина-3.
Лечение геморрагического синдрома было направлено на предупреждение вторичного фибринолиза, особенно в стадии гипокоагуляции. Терапия заключалась во введении гепарина в количестве 10 000—15 000 ЕД в сутки, переливании свежезамороженной или сухой плазмы как до-натора антитромбина-3. При возникновении осложнений применяли дезагреганты (реополиглюкин), препараты, стабилизирующие мембраны клеток (гордокс, контри-кал), переливание свежезаготовленной донорской крови.
В схеме терапии больных со злокачественными новообразованиями важное значение придают устранению ги-
| Глава 4 |
поволемии, стабилизации реологических свойств крови, профилактике дыхательной недостаточности. Нарушения обмена и истощение обусловлены не только влиянием опухолевого процесса, но и нарушением поступления пищи и жидкости в организм, катаболическими перестройками в организме. Операционные и послеоперационные потери белка приводят к нарастанию гипопротеинемии, снижению концентрации альбумина. Уменьшение ОЦК вызывает уменьшение объема плазмы и электролитных композиций.
Злокачественная опухоль является «ловушкой» для отдельных субстратов обмена, истощая компенсаторные механизмы организма. В очаге повреждения после удаления опухоли развиваются катаболические процессы, которые с одной стороны, ускоряют поступление в кровоток токсичных продуктов распада, а с другой — способствуют увеличению «потребления» аминокислот, используемых опухолью для синтеза белка. Развитие белковой недостаточности сопровождается снижением энергетических показателей, усилением процессов липолиза и гликогеноли-за, истощением жировых и углеводных резервов организма, нарушением процессов утилизации углеводов в обеих фазах биологического окисления — аэробного расщепления глюкозы и аэробного окисления трикарбоновых кислот в цикле Кребса.
При изучении водно-электролитного баланса установлена взаимосвязь между белками, жирами, электролитами и водой. Близкие к нормальным средние показатели концентрации электролитов в крови и моче, отмечавшиеся до операции, изменялись на следующие сутки после операции: активно выводился из организма калий (с мочой), происходила задержка натрия. Уменьшение диуреза (14,2 + 0,8 мл/кг) и увеличение плотности мочи в ближайшие сутки свидетельствовали о перераспределении жидкости в организме и ее частичной задержке (Lohlein D., 1980).
Таким образом, основные задачи интенсивной терапии у онкологических больных с локализацией опухоли в че-люстно-лицевой области и шеи заключаются в следующем:
— поддержание необходимого ОЦК и его составляющих, устрь нение гиповолемии;
— нормализация КОС крови и водно-электролитного баланса дль усиления транскапиллярного обмена в тканях;
ПОСЛЕОПЕРАЦИОННАЯ ИНТЕНСИВНАЯ ТЕРАПИЯ
— восстановление кислородно-транспортной функции крови путем нормализации ее кислородной емкости (эритроцитная масса, свежезаготовленная кровь);
— усиление капиллярного кровотока (дезагреганты, декстраны) для улучшения реологических показателей крови, повышения выделительной функции почек;
— энтеральное и парентеральное питание;
— устранение органных расстройств.
Непреложными правилами коррекции гомеостаза у онкологических больных в послеоперационном периоде являются тщательный лабораторный контроль и динамическая клинико-лабораторная оценка состояния больного, гибкая коррекция плана лечения.
Метаболическая коррекция (трансфузионная терапия, парентеральное и энтеральное питание)
У наблюдавшихся нами больных увеличение отека в области операционной раны достигало максимума к 5— 6-м суткам после вмешательства и часто былосвязано нетолько с наличием раны, но и с перераспределением воды, белка и электролитов в организме. В плазме крови и моче наблюдалось увеличение выделения калия и задержка натрия, что свидетельствовало об изменении их соотношения по сравнению с пооперационным периодом. Диурез в 1-е сутки был равен +0,41 мл/кг, что расценивали как приспособительную реакцию, возникавшую вответ наоперационную травму.
Одними из основных причин дефицита калия в послеоперационном периоде являются катаболическая реакция и дефицит клеточных белков, обусловленный уменьшением их поступления с пищей. Послеоперационное усиление основного обмена в ответ на стрессовую реакцию — оперативное вмешательство — активизирует распад не только белков, но и углеводов.
При любых травма-точных вмешательствах, как правило, отмечаются значительные потери азота в послеоперационном периоде. По нашим данным, в первые сутки после остеотомии верхней и нижней челюсти потери азота
| Глава 4 |
составили 18 г, что в пересчете на белок составляет свыше 120 г или 475 г мышечной ткани. В белке содержится 16— 17 % азота, т.е. 1 г азота соответствует 6,25 г белка (в мышечной ткани содержится 25 % белка).
С 1-го дня голодания организм человека утилизирует структурный белок мышцы внутренних органов. Это приводит к нарушению регуляции обмена веществ, главным образом в печени. В 1-е сутки снижается синтез альбумина в печени, происходит снижение коллоидно-осмотического давления и водоудерживающей функции плазмы крови. При полном или частичном белковом голодании печень может потерять до 40 % белков. В то же время в ней происходит накопление жира, в результате чего ухудшается ее функциональное состояние, тормозится деятельность ферментных систем печени, осуществляющих синтез аминокислот. Таким образом, состояние процессов метаболизма в крови, оттекающей от печени, раскрывает сущность и динамику процессов, происходящих в органе после операции. Состояние кровотока в органах спланхни-ческого бассейна при проведении реконструктивных операций на костях черепа является важным показателем адекватности обмена в зависимости от функционального состояния печени, системного и регионального кровотока.
Исследования, проведенные нами у 48 больных, перенесших реконструктивные операции в черепно-лицевой области, позволили выявить нарушения обмена в послеоперационном периоде. У больных изучены биохимические показатели артериальной крови и крови в печеночной вене. Больные в возрасте от 18 до 38 лет были распределены на две группы: первая группа — практически здоровые лица с косметическим дефектом челюстей, которым были проведены реконструктивные операции на челюстях;
вторая группа — больные, перенесшие сложные реконструктивные операции в средней зоне лица и остеотомии с внутричерепным доступом. В послеоперационном периоде биохимические показатели крови, оттекающей от печени, претерпевали значительные изменения. В условиях целостного организма такой подход позволяет сделать вывод о со стоянии обменных процессов в послеоперационном периоде.
У соматически здоровых пациентов (первая группа) снижение кровотока в печени после оперативного вмеша
ПОСЛЕОПЕРАЦИОННАЯ ИНТЕНСИВНАЯ ТЕРАПИЯ
тельства не приводило к изменению ее функциональной активности. У больных второй группы в послеоперационном периоде отмечались ухудшения показателей кровообращения, уменьшение систолического объема и минутного объема кровообращения, тахикардия. Травматичная операция и уменьшение ОЦК провоцировали возникновение патологических реакций со стороны рефлексогенных зон основания черепа, сопровождавшихся критическим повышением или снижением артериального давления, нарушением ритма сердца.
Возмещение кровопотери, составляющей в среднем 80 % ОЦК, проводили плазмозаменителями, свежецит-ратной кровью, эритроцитной массой в количествах до 80 % от объема утраченного ОЦК.
В послеоперационном периоде оксигенация крови в печеночной вене была достоверно ниже, чем в артериальной крови (см. табл. 3). Концентрация фибриногена в крови, оттекающей от печени, была значительно выше исходного уровня. Установлено, что артерио-венозная разница по кислороду крови, оттекающей от печени, резко возраставшая во время операции, постепенно стабилизировалась, но не достигла исходного уровня. По нашему мнению, этот факт объясняется снижением насыщения крови кислородом у больных второй группы, что свидетельствует о несоответствии между энергетическими затратами и кровотоком в печени. Нарушение газообмена в печени и изменения скорости кровотока в ней находят свое выражение в изменении обмена белка и нарушении синтеза аминокислот. Начиная с 1-х суток послеоперационного периода у больных наблюдаются отрицательный азотистый баланс, снижение концентрации белка, увеличение экскреции азота мочевины, уменьшение коэффициента А/Г. Закономерным отражением белковой недостаточности явилось изменение аминокислотного спектра в организме. В плазме увеличивалась концентрация аммиака, в моче содержание аммиака уменьшалось до 90 % по сравнению с дооперационньш уровнем. Дефицит пластических и энергетических резервов вызывал ухудшение общего состояния больных и замедление репаративных процессов в ране. Из изложенного выше следует, что при лечении больного большое значение имеют рациональное питание
| Глава 4 |
и введение в организм дефицитных субстратов, обеспечить которыми больных в послеоперационном периоде естественным способом не представляется возможным (Silberman H. et al., 1982).
Таким образом, результаты хирургической операции в области лицевого и мозгового черепа в значительной степени зависят от эффективности послеоперационной интенсивной терапии, которая нередко принимает характер реанимационных мероприятий. Приводим наблюдение, иллюстрирующее характер терапии после операции.
Больной Т., 35 лет, поступил в клинику с диагнозом:
сочетанная деформация челюстей (верхняя микрогнатия и нижняя макрогнатия), синдром удлиненного лица.
Операция: плоскостная двусторонняя остеотомия нижней челюсти, остеотомия верхней челюсти по Безру-кову,гениопластика.
Комбинированный эндотрахеальный наркоз: фента-нил, дроперидол, закись азота с кислородом, интубация трахеи через нос под контролем прямой ларингоскопии. В условиях нейролептаналгезии и ИВЛ проведена остеотомия верхней челюсти, двухсторонняя остеотомия нижней челюсти, гениопластика. Все оперативные вмешательства выполнены последовательно. Анестезия протекала гладко, продолжительность наркоза 4 ч. 35 мин. По ходу операции проводили управляемую гемодилюцию с использованием коллоидных и кристаллоидных растворов, аутоге-мотрансфузию (800 мл). Операционная кровопотеря составила 1 л 200 мл. По ходу операции перелито 800 мл поли-глюкина, 800 мл реополиглюкина, 400 мл лактасола, 800 мл аутокрови. К концу операции дефицит ОЦК составил более 20 % от расчетной нормы.
После пробуждения и восстановления спонтанного дыхания больной доставлен в послеоперационную палату, где за ним проводили мониторное динамическое наблюдение. Несмотря на тампонаду носовых ходов, выполненную с целью гемостаза, отмечено подтекание крови из носоглотки. Проведена задняя и передняя тампонада.
Спустя 2 ч. 50 мин. в момент осмотра больного отмечаются бледность кожных покровов, цианоз губ, дыхание поверхностное, не адекватно. В полости рта большое количество крови, пульсация на периферических сосудах от-
ПОСЛЕОПЕРАЦИОННАЯ ИНТЕНСИВНАЯ ТЕРАПИЯ225
сутствует, тоны сердца не выслушиваются. Незамедлительно начаты реанимационные мероприятия: удаление крови и сгустков из полости рта для обеспечения свободной проходимости верхних дыхательных путей; аппаратная вентиляция легких, закрытый массаж сердца (аппарат РО-6, минутный объем вентиляции 13 л/мин, дыхательный объем 750 мл, кислород 100 %; трансфузионная терапия с целью поддержания необходимого ОЦК и центральной гемодинамики. В подключичную вену введено 1 мл адреналина и 1 мл атропина. Спустя 2 мин. после начала реанимационных мероприятий кровообращение было восстановлено, АД 140/90 мм рт. ст., пульс 115 в минуту. Приняты меры для остановки кровотечения.
Гемотрансфузиии интенсивная трансфузионная терапия: 1500 мл консервированной донорскойкрови, 400 мл реополиглюкина,400 мл лактасола,600 мл плазмы,20 мл10 % раствора альбумина, 200 мл 20 % раствора глюкозы с инсулином, витамины группы В и С. Под влияниемтерапии увеличился сердечныйвыброс, улучшился транскапиллярный обмен.
Больному наложена трахеостома. В конце дня объем перелитой жидкости составил б л, кровопотеря3500 мл, диурез 3 л.
Второй этап лечения начали после ликвидации геморрагии и устранения непосредственной угрозы жизни больного. С целью доставки в организм пластических и энергетических веществ на следующий день, помимо корригирующих трансфузий, начали проводить парентеральное питание в режиме гипералиментации (продолжительность 7 дней с последующим переходом на смешанное питание. Расчет компонентов парентерального питания:
1) раствор альвезина (аминокислоты Д-формы) применяли из расчета 0,57 г на 1 кг массы тела (всего1—1,2 гусловного белка);
2) энергетические расходы покрывались растворами глюкозы (гипералиментация) из расчета 25— 30 к кал/кг (126 кдж) — 1500 мл 20 % раствора глюкозы, всего 2100 ккал.;
3) минеральные вещества: калий в виде КИ вводили в дозе до 6 г/сут или в виде 7,4 % раствора аспирагината калия и магния. Применялся раствор Ринге ра, лактасол;
| Глава 4 |
4) анаболические стимуляторы: инсулин в расчетных дозировках, неробол 5 % раствор 1 мл через 3—4 дня. Витамины группы В, С.
Парентеральное питание проводили через подключичную вену в режиме до 40 капель в минуту в течение 8— 10 ч. С 3-го дня послеоперационного периода начато вспомогательное комбинированное питание, включавшее энте-ральные средства, всасывающиеся в верхних отделах же-лудочно-кишечного тракта (сметана, яйца, спирт, молоко, сливки). На 8-й день больной переведен в общую палату. Дефицит массы тела к этому времени составил 1,2 кг по сравнению с исходным уровнем. На 35-й день больной выписан из стационара в удовлетворительном состоянии.
Парентеральное и энтеральное питание. Результаты операции часто больше зависят от эффективности интенсивной терапии, которую проводят в послеоперационный период, чем от мастерства хирурга, особенно при заболеваниях челюстно-лицевой области, пищеварительного тракта и смежных областей. Поиск оптимальных методов лечения по-прежнему остается актуальной проблемой (Roth E., 1986; Karner J. et al., 1987).
Интенсивная трансфузионная терапия, парентеральное и энтеральное питание, проводимые в послеоперационном периоде, обеспечивают поддержание адекватных приспособительных реакций организма в ответ на операционную травму и способствуют восстановлению постоянства внутренней среды. Обеспечение жизнедеятельности основных систем организма должно идти по пути нормализации их работы, а компоненты вводимых смесей, воздействуя на обменные процессы, обеспечивают доставку к ним необходимых пластических и энергетических веществ.
Многообразные физико-химические и физиологические реакции объединяют термином «обмен». Обмен состоит из анаболитической фазы — доставка и усвоение питательных веществ — и катаболитической — расщепление, распад и выведение продуктов обмена из организма. Функция питания строится по принципу энергетического, пластического, ферментативного и резервного построения всей системы обменных реакций, происходящих в организме от момента зарождения и смерти.
ПОСЛЕОПЕРАЦИОННАЯ ИНТЕНСИВНАЯ ТЕРАПИЯ227
Основные превращения белков, жиров и углеводов совершаются в процессе ассимиляции и диссимиляции. Биологическое значение этих процессов состоит в том, что при расщеплении веществ освобождается энергия, которая обеспечивает все функции организма. В то же время при синтезе образуются видоспецифические субстраты:
углеводы, жиры и белки, т.е. те структурные элементы, которые определяют целостность организма. Питательные вещества представляют собой крупные молекулы, и их распад на более простые соединения является необходимым условием дальнейшего использования в клетке источников энергии и пластического материала.
Ближайший послеоперационный период характеризуется увеличением потребностей организма в заменимых и незаменимых факторах питания, энергии возрастанием функциональной нагрузки на жизнеобеспечивающие системы организма (рис. 27).
Рис. 27. Парентеральное питание в клинической стоматологии
8*
| Глава 4 |
Парентеральное питание. Парентеральное питание реализуется на клеточном и субклеточном уровне, минуя фазу пищеварения, именно ту фазу, которая у стоматологических больных наиболее часто бывает затруднена. При этом внутривенно вводимые субстраты поступают с кровью портальной вены в печень, где подвергаются химическим превращениям, после чего используются на построение клеток организма. Этот схематически представленный процесс в определенной мере объясняет основной принцип метода парентерального питания, необходимость его применения у стоматологических больных в отличие от больных с другими заболеваниями.
Важным фактором катаболической фазы обмена является усиление гликогенолиза с быстрым истощением запасов гликогена — одного из главных источников энергии в организме. В катаболической фазе существенно увеличиваются потери организмом азота, которые могут достигать 35—49 г в сутки. Содержание азота в белке составляет в среднем 16 %, т.е. 1 г азота соответствует 6,25 г белка. Следовательно, выделение 35—40 г азота эквивалентно потере 220—250 г белка в сутки (средние потери белка за сутки в состоянии относительного покоя составляют 60—70 г).
Важным энергетическим компонентом парентерального питания является глюкоза, которая подвергается качественной и количественной перестройке в случае развития патологического процесса. При парентеральном питании углеводы, попадая в печень, превращаются в сложный полисахарид — гликоген. Находящаяся в крови глюкоза выполняет роль основного биологического топлива и является составной частью полисахаридов и гликопротеидов.
Гликопротеиды входят в состав клеточной оболочки и циркулируют в кровяном русле в качестве транспортных молекул. К гликопротеидам относятся некоторые гормоны, ферменты, иммуноглобулины. В организме глюкоза является исходным продуктом для биосинтеза ряда Сахаров, например фруктозы, галактозы, ксилозы и др.
Не менее важное значение в обмене играют жиры, являющиеся энергетической формой питательных веществ. Вместе с тем они используются в организме и как источники энергии.
ПОСЛЕОПЕРАЦИОННАЯ ИНТЕНСИВНАЯ ТЕРАПИЯ229
Содержание общих липидов в плазме крови человека зависит от многих факторов, таких, как количество потребляемой пищи, физическая активность конституции. Из многочисленных функций жирных кислот наиболее важной является участие липидов в построении биологических мембран.
Обязательной составной частью парентерального питания являются витамины, различные соли, микроэлементы и другие химические вещества. Именно они поддерживают обмен белков, жиров и углеводов, обеспечивая необходимые для организма структурные перестройки.
Важная задача парентерального питания — не только восполнить дефицит питательных веществ, необходимых для жизнедеятельности организма, но и обеспечить течение процессов саморегуляции и функциональной системы питания и поддержание концентрации необходимых веществ в крови на оптимальном уровне.
Относительно обеспечения эффективного питания больных с опухолями до сих пор высказываются противоречивые мнения. По существу в послеоперационном периоде в зоне травмы необходимо создать максимальный покой, что не может быть выполнено у стоматологических больных. В то же время в этот период организм нуждается в достаточном количестве пластического и энергетического материала, способного обеспечить повышение регенеративных процессов в ране. Зондовое и парентеральное питание имеет своих противников и сторонников, которые достаточно аргументированно обосновали свои взгляды на тот или иной способ питания стоматологических больных в послеоперационном периоде.
Ряд исследователей убедительно доказали наличие прямой связи между нормализацией метаболизма, рациональным азотистым питанием и клиническим течением послеоперационного периода. Парентеральное питание в послеоперационном периоде может быть эффективным только после ликвидации грубых расстройств (восстановление КОР, водно-солевого равновесия, адекватного кислородного режима), возникших во время оперативного вмешательства.
Парентеральное питание назначают при ликвидации функциональных расстройств жизненно важных органов
| Глава 4 |
и систем: нарушений деятельности сердечно-сосудистой и дыхательной систем, отека мозга и шокового состояния. Обязательными условиями являются ликвидация кровотечения и возмещение кровопотери. Эти положения особенно важны для онкологических больных, так как при их лечении анестезиологу нередко приходится решать вопросы борьбы с кровотечением, функциональными нарушениями и расстройствами метаболизма в ближайшем послеоперационном периоде (Jehn U., 1986).
В это время организм больного страдает от того, что не обеспечен полноценными питательными веществами (нутриентами), и от метаболических расстройств, явившихся следствием реакции на травму.
Выбор средств определялся катаболизмом белка, нарушениями обмена жиров, энергетической недостаточностью и невозможностью обеспечить физиологический режим доставки питательных ингредиентов в организм больного. Для восполнения пластического и энергетического дефицита использовали гидролизаты белка (казеин, аминозол), аминокислоты (вамин, левамин, жировая эмульсия (интралипид), растворы углеводов, раствор Рин-гера, витамины, стимуляторы анаболизма (неробол, рета-болил).
В зависимости от общего состояния больного и средней энергетической потребности (24 ккал/кг в сутки) у больных в послеоперационном периоде рекомендуется увеличить энергетический уровень на 10—20 % от должных показателей. Ряд авторов рекомендуют увеличивать объем парентерального питания на 5—8 % на каждый градус температуры тела сверх 37°С (Рябов Г.А., 1983).
Тесная взаимосвязь энергетических и пластических процессов в организме обусловливает введение энергетических компонентов в виде глюкозы или жировой эмульсии (чаще применяют оба компонента одновременно).
В 1-е сутки послеоперационного периода больному требуется от 30 до 40 ккал на 1 кг массы тела или 200-250 небелковых килокалорий на каждый грамм вводимого азота (2100—2300 ккал в сутки). Для этого необходимо 2100 : 4 = 525 г глюкозы (1 г глюкозы утилизируется с выделением 4,1 ккал). При повышении температуры на каж-
ПОСЛЕОПЕРАЦИОННАЯ ИНТЕНСИВНАЯ ТЕРАПИЯ231
дые 0,5°С (свыше 37°С) необходимо добавить еще 100 ккал. Таким образом, суточная потребность в глюкозе (вводимой через магистральную вену) составит:
^Зр100 = 1750 мл 30 % глюкозы
В последние годы за рубежом выпускают 50 % оффи-цинальные растворы глюкозы с микроэлементами, предназначенные для введения через крупные сосуды. При этом общее количество вводимой жидкости уменьшается в несколько раз. Следует помнить, что концентрацию глюкозы необходимо повышать постепенно в связи с адаптацией инкреторного аппарата поджелудочной железы к большим дозам и высокой концентрации.
После оперативных вмешательств возможно снижение толерантности к глюкозе вследствие подавления инкреторной функции поджелудочной железы. Обязательным компонентом энергетической смеси является инсулин (Ollenschlager G., 1985; Green N.M., 1987). Если глю-козурия превышает 1—3 %, то следует увеличить дозу инсулина. Жировая эмульсия интралипид является энергетическим материалом (1 г жира считается эквивалентным 9,1 ккал), доза эмульсии составляет 1,5—2 г/кг в сутки.
Практический учет всех показателей дефицита должен быть индивидуальным в зависимости от биохимических показателей. Важную роль в обмене играют витамины группы В и С, являющиеся биологическими катализаторами метаболических процессов.
Зондовое (энтеральное) питание. Обеспечить нормальные процессы синтеза после операции можно лишь с помощью адекватного сбалансированного питания, т.е. путем введения в организм необходимых количеств, пластических материалов, энергии, воды, электролитов, витаминов, микроэлементов. Использовать оральное питание далеко не всегда возможно, особенно в хирургии челюстно-лицевой области, глотки, полости рта. В связи с этим в до-и послеоперационном периодах особое значение приобретает энтеральное питание как единственное средство, способное нивелировать потери, вызванные катаболической направленностью обмена веществ в организме больного,
| Глава 4 |
обусловленной влиянием заболевания и операционной травмы. Еще сравнительно недавно среди клиницистов было распространено мнение, что в первые 2—3 дня после оперативного вмешательства больной не нуждается в питании. Об этом в 1959 г. писал известный специалист по метаболизму и лечению больных после операции Д.Мур. Спустя несколько лет он признал необходимость питания хирургических больных с 1-го дня после операции (BablerK.H.etal., 1987).
При обычном питании белок поступает в желудочно-кишечный тракт с неизменной первичной структурой. В желудке он подвергается дальнейшей денатурации с помощью соляной кислоты желудочного сока и далее — ферментативному расщеплению до аминокислот. Аминокислоты всасываются в средних и нижних отделах кишечника, поступают в венозные сосуды кишечника, затем через систему воротной вены в печень, где и начинается их метаболический цикл в организме (Kommerell В., 1985).
При парентеральном питании препараты белка вводятся в сосудистое русло, как правило, в отделы, не связанные с портальной системой. Если для парентерального питания используют гидролизаты белка (наиболее употребительная лекарственная форма), то имеющиеся в ней аминокислоты, пройдя через малый круг кровообращения и попав в ткани, сразу вступают в обменные процессы. Почти то же самое происходит с остальными компонентами парентерального питания: углеводами, жирами, витаминами (Adibi S.A. et al., 1984).
У большинства хирургических больных имеется дефицит белка и энергии, причем его выраженность зависит от ряда причин.При дефиците потребления и затрудненной утилизации пищевых продуктов (деформации челюстей, опухоли, анкилозы височно-нижнечелюстного сустава и др.) у больных отмечается уменьшение массы тела до 50 % за счет скелетной мускулатуры и подкожной жировой клетчатки. Содержание альбумина в плазме у них может быть нормальным, а признаков повышения обмена не отмечается, при этом потери азота с мочой невелики. Сумма суточных энергетических потребностей хирургического больного резко возрастает при наличии сопутствующего патологического процесса или присоединении инфекции и достигает 43 ккал/кг, или 180 кДж/кг, в сутки.
ПОСЛЕОПЕРАЦИОННАЯ ИНТЕНСИВНАЯ ТЕРАПИЯ
Оперативное вмешательство в челюстно-лицевой области нарушает обычный путь поступления пищи в начальные отделы пищеварительной трубки при сохранной функции желуд очно-кишечного тракта. Эффективным методом, позволяющим предупредить возникновение классической катаболической реакции после операции, является специальное питание — зондовое (энтеральное). В зондовом питании нуждаются стоматологические больные с пониженным статусом питания, пациенты с нарушениями белкового и водно-солевого обмена, у которых в послеоперационном периоде возникают осложнения, препятствующие адекватному питанию. Применение зондово-го питания оправдано в тех случаях, когда после операции поступление пищи через рот затруднено или невозможно. Питательную смесь вводят через тонкий пластмассовый зонд (через нос) с помощью помпы (насоса) либо обычной капельной системы без фильтра.
Перед началом операции определяют тактику питания больного, которому предполагают ввести зонд и проводить искусственное кормление:
1) расчет диетической формулы питания;
2) прогнозирование степени риска возникновения обменных нарушений;
3) выявление питательного дефицита с помощью физических и лабораторных методов исследования;
4) выбор метода введения энтеральной смеси;
5) организация питания и наблюдение за больным. Для зондового питания применяют энпиты, представляющие собой полимерные питательные модули или элементные диеты, т.е. питательные смеси, обеспечивающие потребность больных в повышенных количествах того или иного нутриента. С этой целью используют инцитан (СССР), терапии (ПНР), козелат (ВНР), биосорб (ФРГ). При раздельном применении этих препаратов выявлено недостоверное различие в их составляющих, а отсутствие изменений в биохимических показателях вследствие их относительной однотипности позволило нам оценить данные смеси как единый препарат для зондового питания (например, терапин содержит 1—1,5 ккал/мл, инпитан — 1,06 ккал/мл, козелат — 1 ккал/мл).
Белки в этих смесях представлены казеином, жиры — в форме масел (кукурузное, соевое). Энпиты имеют вид по-
| Глава 4 |
рошка, который разводят в воде, а затем вводят через эластичный полимерный зонд. Биосорб представлен в виде жидкости во флаконах заводской упаковки.
Суточную дозу препаратов мы рассчитывали на основании реальных энергетических потребностей, исходя из основного обмена:
00= 66,4 + 13,7хМТ+50Р—6,7хВ,
где00 — основной обмен, ккал/сут;
МТ — масса тела, кг, Р — рост, см; В — возраст, годы
Энергетическая ценность суточного рациона составила 2100 ккал, из которых на долю белка приходилось 15 %, жира — 35 %, углеводов — 50 % . Зондовое питание проводили в течение 7 дней. Контрольная группа состояла из практически здоровых людей.
Для оценки эффективности проводимой терапии изучали антропометрические данные: Р, МТ, толщину кожной складки (ТКС) в области проекции трехглавой мышцы, окружность конечности (ОК). ТКС и ОК измеряли с помощью калипера Align Arrows и измерительной линейки.
За стандартные показатели принимали данные, полученные в контрольной группе, и значения, рекомендованные ВОЗ. Кроме того, определяли концентрацию общего белка и альбумина в сыворотке крови, уровень гемоглобина, содержание мочевины в суточной моче, коэффициент альбумин/глобулин (А/Г), количество лимфоцитов. Суточную экскрецию азота (N) рассчитывали по Тодорозу (доклад ФАО, ВОЗ, 1987):
| N= |
| 0,8 МТ |
где V — количество выведенной мочевины (в моче), г/сут, МТ — масса тела, кг
Азотный баланс (АБ) определяли как разность между введенным и выведенным за сутки количеством азота + 4;
дополнительные потери N (пот, мокрота и др.) принимали равными 4 г/сут.
Из отечественных смесей для лечения больных применяют белковый, низколактозный энпит и инпитан, разработанные в Институте питанияАМН СССР. Инпитан не только сбалансирован по всем нутриентам, но частично гидролизован по белку, содержит 440 ккал на 100 г сухого вещества, или 1000 ккал в 1000 мл смеси.
ПОСЛЕОПЕРАЦИОННАЯ ИНТЕНСИВНАЯ ТЕРАПИЯ
Хорошо зарекомендовала себя смесь, состоящая из общедоступных продуктов: 500 мл молока, 250 г сухого молока, по 50 г сливочного масла, меда, сахара, 3 яйца, разведенные в 1000 мл воды; 2500 мл этой смеси содержат 2500 ккал.
Результаты анализа биохимических показателей при применении энпитов свидетельствовали об их положительной динамике. Концентрация белка в плазме крови у больных в предоперационном периоде была достоверно ниже, чем в контрольной группе. Высокая концентрация мочевины и низкое содержание альбумина указывали на снижение белоксинтезирующей функции печеночной клетки в дооперационном периоде.
Отрицательный АБ у больных до операции свидетельствовал о существенном дефиците белка и его неполноценности по аминокислотному составу. Применение энпитов стабилизировало АБ или делало его положительным к окончанию послеоперационного периода. Ко 2-й неделе наблюдалась положительная динамика антропометрических показателей (МТ, ТКС, ОК). В результате корреляци-
Таблица 8.
Результаты зондового питания 8 клинике челю с тно -лицевой хирургии (М±т)
| Показатель | Больные (п=15) | Здоровые | |
| при поступлении | после лечения | (контроль, п=15) | |
| Альбумин, г/л | 36,5±0.5 | 40,7±0.9* | 42,8±0,8 |
| Коэффициент А/Г | 0,б±0,03 | 0,8±О.ОГ | 0.9±0,01 |
| Общий белок, г/л | 72.7±1,3 | 75.1±2,3 | 78,0±1,2 |
| Гемоглобин, г/л | 131±1 | 141±8* | 146±5 |
| Выведение мочевины*, ммоль/сут | 556.8±1В,1 | 360.4±24,Г | 480,5±13,1 |
| МТ, кг | 70,1±3.1 | 74,0±2.6* | 74,8±2,5 |
| ТКС,мм | 15,3±0,8 | 17,1±0,6" | 19,2±0,5 |
| ОК, мм | 24,6±2,0 | 25,8±2,8 | 27,6±1,3 |
| АБ, г/кг/сут | -0,3 | +0,8 | — |
| Примечание * статистически достоверное (р<0,05) различие с исходными |
| Глава 4 |
энного анализа биохимических и антропометрических показателей установлено, что у больных в пооперационном периоде и после лечения энпитами МТ коррелировала с концентрацией альбумина (Ч = +0,56; р<0,05). Содержание гемоглобина и мочевины, коэффициент А/Г находились в прямой зависимости от эффективности терапии с помощью зондового питания.
У больных, перенесших реконструктивные операции, были выявлены энергетический дефицит, нарушения синтеза липидов, отрицательный АБ. Данные, полученные при исследовании (высокая концентрация мочевины, гипопротеинемия, нарушения кровотока в печени), указывали на выраженную катаболическую направленность обмена и нарушения утилизации субстратов потребления. Преобладание положительного АБ при зондовом питании свидетельствовало о тенденции к анаболизму;
усилении протеиносинтеза и улучшении клинических показателей по сравнению с контрольной группой (Klimberger G., Deutch E., 1983).
Из осложнений, которые могут встретиться при применении зондового питания, следует указать на диарею и тошноту, т.е. осложнения, чаще связанные с техническими погрешностями и изменением темпа введения (быстрое) смеси в организм.
Количество энергетического материала, введенного при зондовом питании, должно покрывать основные потребности организма и компенсировать повышенные потери (рис. 28). Потребность в энергии при остеотомиях верхней и нижней челюсти возрастала в зависимости от индивидуальных особенностей больных (пол, возраст, масса тела, изменения основного обмена, операционная кровопотеря, степень травматичности вмешательства) и составила в среднем 2600 ккал.
Введение азота стимулирует анаболические реакции, ускоряет репаративные процессы в тканях и костях, обеспечивает эффективную консолидацию костных фрагментов. Однако уровень белка в послеоперационном периоде не должен быть выше 1,5 г/кг. Целесообразно обеспечить адекватное количество аскорбиновой кислоты, которой придают большое значение в восстановлении и образовании волокон
ПОСЛЕОПЕРАЦИОННАЯ ИНТЕНСИВНАЯ ТЕРАПИЯ
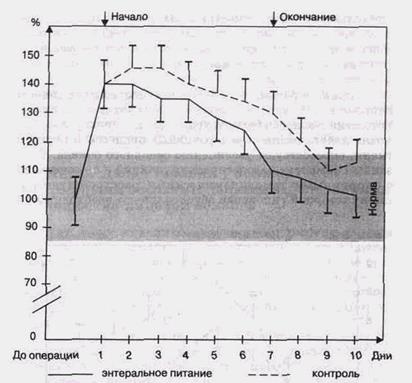
Рис. 28. Изменения величины основного обмена при энтеральном питании (%)
коллогена (содержание в пище не менее 10 мг/сут). Количество минеральных веществ в составе энпита должно быть:
Са — 1000 мг., Р — 1000 мг., Mq — до 500 мг.
Перечисленные особенности катаболической реакции дали нам основание считать целесообразным применение зондового питания, обеспечивающего организм веществами, необходимыми для коррекции послеоперационного катаболизма у больных после реконструктивных операций в челюстно-лицевой области. При зондовом питании (биосорб) ингредиенты в адекватных пропорциях поступают через стенку кишечника в кровь, в портальную зону, как при естественном питании. Ряд данных, полученных
| Глава 4 |
в результате исследования (рис. 29), указывали, что в контрольной группе имел место катаболический характер обмена и нарушение утилизации субстратов потребления (высокая концентрация мочевины, глюкозы, нарушения кровотока в печени).
Таким образом, в ближайшем послеоперационном периоде катаболические процессы приводят к быстрому истощению запасов белков, углеводов и жиров, резко тормозят пластические и репаративные процессы в костной ткани, способствуют увеличению основного обмена. Указанный комплекс патологических реакций и их сочетание с вторичными гемодинамическими расстройствами и циркуляторной гипоксией обусловливают необходимость
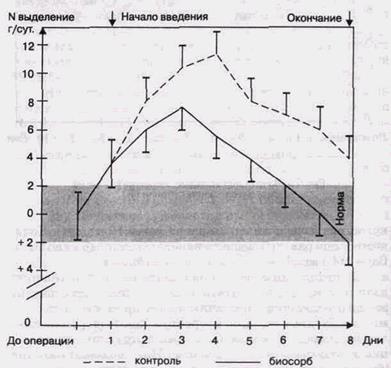
Рис 29 Эк креция азота у больных в послеоперационном периоде при энтеральном питании (г/сутки)
ПОСЛЕОПЕРАЦИОННАЯ ИНТЕНСИВНАЯ ТЕРАПИЯ
проведения патогенетически обусловленной терапии, основными звеньями которой являются коррекция общих метаболических потребностей и осуществление важнейших компонентов интенсивной терапии: обеспечение адекватного газообмена, сердечного выброса, ОПК, функции печени, почек. Это послужило основанием для примене ния зондового питания, способного обеспечить организм больного всеми необходимыми веществами и предупредить развитие осложнений (Wilhamson D.U., 1984).
Дата добавления: 2015-07-24; просмотров: 1256;
