НЕКОТОРЫЕ ПАРАМЕТАБОЛИЧЕСКИЕ ПРОЦЕССЫ
Вещества, образующиеся в ходе параметаболических процессов, могут оказывать как негативное, так и положительное действие на организм.
ПРИМЕРЫ НЕГАТИВНОГО ВЛИЯНИЯ
Негативное влияние оказывают две группы биомолекул:
1. Вещества, в составе которых имеется карбонильная, альдегидная или кетогруппа
2. Вещества – сильные окислители
ГРУППА 1.
Карбонильная группа имеется в молекуле глюкозы, но эта группа маскируется, потому что в физиологических условиях почти все молекулы глюкозы находятся не в линейной форме, где карбонильная группа проявляет свои свойства, а в циклической - пиранозной или фуранозной (99,997% от общего количества молекул глюкозы). Для других моносахаридов характерен больший процент линейной формы, из которых самыми опасными являются триозы (они не имеют циклической формы), но их содержание в организме, по сравнению с глюкозой, невелико.
Ферментативное взаимодействие белков с углеводами наблюдается в норме, в результате чего образуются сложные белки – гликопротеины. Источником углеводного компонента служит УДФ-глюкоза, а сам процесс называется гликозилированием. Образуются O-гликозидные связи с участием радикалов серина, треонина (через ОН-группу) и N-гликозидные связичерз амидную группу аспарагина. (при этом источником углеводнФерментативное взаимодействиеЕсли процесс идет с участием ферментов, ативногЭто приводит к гликозилированию белков и нуклеиновых кислот, что приводит к возникновению мутаций.
Без участия ферментов карбонильная группа моносахаридов может взаимодействовать с аминогруппами полипептидных цепей белковых молекул, а также азотистых оснований нуклеиновых кислот.
В случае взаимодействия с белками процесс называется гликированием. Мишенями для присоединения углеводного компонента являются аминогруппа в радикалах лизина и аргинина, а также свободная a-аминогруппа на N-конце белковой молекулы.
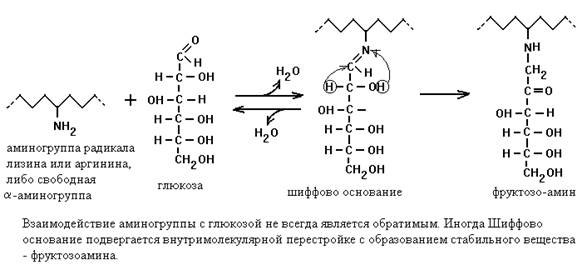
В отличие от ферментативных реакций, скорость гликирования зависит от концентрации глюкозы прямо пропорционально (для ферментативных реакций характерна гиперболическая зависимость скорости от концентрации субстрата). Поэтому у здорового человека гликирование если и протекает, то очень медленно, а у больных сахарным диабетом – быстро, и у них в организме много гликированных белков. Интенсивно гликируются, как правило, альбумины и глобулины – эти белки плазмы крови содержат много фруктозоамина, а также белки, находящиеся в инсулин-независимых тканях.
Фруктозо-амин тоже обладает карбонильной группой, поэтому возможно образование Шиффовых оснований между фрагментами двух разных полипептидных цепей. Так образуются вторичные продукты гликирования:
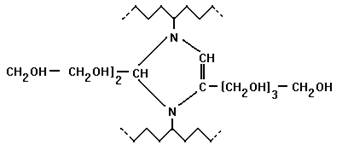
Большинство этих веществ являются хромофорами - пигментами коричневого цвета. Вторичные продукты гликирования характерны для долгоживущих белков, обновляющихся в течение месяцев, лет. Это коллаген, кристаллины (белки хрусталика глаза), некоторые другие белки.
Образование первичных и вторичных продуктов гликирования не всегда сопровождается нарушением функции белка. Например, гликирование гемоглобина с образованием молекулярной формы А1с не влияет на способность этого белка переносить кислород. Но иногда гликирование вызывает серьезные нарушения функционирования белка. Так, гликирование апобелка АпоB100 в составе липопротеинов низкой плотности (ЛНП) ведет к потере его способности взаимодействовать с тканевыми рецепторами, он начинает восприниматься организмом как чужеродный. В результате вырабатываются антитела к этому белку, ЛНП взаимодействуют с рецепторами макрофагов и фагоцитируются. Макрофаги, получившие много холестерина, погибают, а кристаллы холестерина откладываются в интиме сосудов. Поэтому для больных сахарным диабетом характерен ранний атеросклероз.
Гликирование белков мембраны эритроцита приводит к изменению ее эластических свойств, в результате чего ухудшается кровоснабжение и оксигенация тканей.
При гликировании коллагена атаке подвергаются радикалы лизина и оксилизина, необходимые для образования поперечных сшивок в молекуле этого белка. Сшивки все-таки образуются, но при этом нарушается архитектура молекулы коллагена, что приводит к нарушению его эластических свойств. В результате снижается эластичность стенки артерий. Опасным для организма является гликирование коллагена базальной мембраны почечных клубочков – увеличивается проницаемость фильтрационного барьера, поэтому одним из частых осложнений сахарного диабета является нефропатия.
Гликирование кристалинов ведет к помутнению хрусталика – катаракте.
Для оценки состояния больного сахарным диабетом используется определение уровня гемоглобина А1с и фруктозоамина.
Лекарственный препарат амидогуанидин предотвращает образование вторичных продуктов гликирования, образуя Шиффово основание с карбонильной группой фруктозо-амина.
Значительное количество продуктов параметаболизма обнаруживается в крови больных, страдающих почечной недостаточностью. У таких больных концентрация мочевины в крови может возрастать до 80 ммоль/л (в норме: 3,3 – 6,6 ммоль/л). Сама мочевина является инертным веществом, но способна вступать в неферментативную реакцию. Теряя аминогруппу, мочевина превращается в изоциановую кислоту:
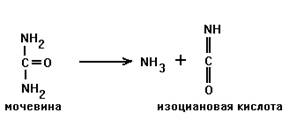
Изоциановая кислота может взаимодействовать с аминогруппами белковых молекул, вызывая их карбомоилирование:

Карбомоилирование гемоглобина приводит к увеличению сродства к кислороду, поэтому ухудшается его способность отдавать кислород тканям – наблюдается гипоксия. При карбомоилировании ферментов карбоангидразы и глюкозо-6-фосфатдегидрогеназы снижается их активность.
Долгоживущие белки также подвергаются карбомоилированию с последствиями, характерными для сахарного диабета (например, катаракта).
Цианаты иногда могут использоваться в лечебных целях. Например, карбомоилируя концевой валин гемоглобина S при серповидно-клеточной анемии, они усиливают его гидрофильность.
Витамин В6 имеет альдегидную группу, и при его поступлении в организм способен пиридоксилировать белки. При избытке В6 в организме наблюдаются нарушения со стороны нервной системы, а иногда – рак печени.
При поступлении этанола в организм продукт его метаболизма – уксусный альдегид вызывает ацетилирование белков, например, гемоглобина. Опасным является ацетилирование белков нервной ткани, и нейромедиаторов.
ГРУППА II.
Эта группа веществ представлена сильными окислителями.

NO, HOCl – продукты ферментативных реакций. HOCl образуется в полиморфно-ядерных гранулоцитах под действием миелопероксидазы:
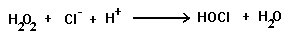
NO образуется с участием фермента NO-синтетазы в лейкоцитах, нейронах, в эндотелии сосудов:
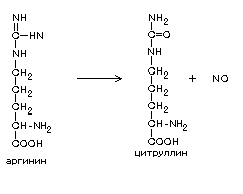
Некоторые сильные окислители являются сигнальными молекулами: NO может выступать в качестве нейромедиатора, супероксид анион и пероксида водорода иногда выполняют сигнальную функцию.
Сильные окислители используются как «молекулярное оружие» для разрушения чужеродных веществ.
Сильные окислители также воздействуют на белки, нуклеиновые кислоты и липиды.
При окислении липидов происходит обогащение их кислородом и фрагментация. Из полиненасыщенных жирных кислот при этом образуются токсические вещества:
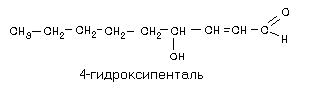
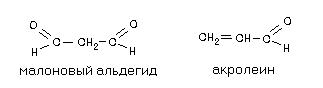
При взаимодействии с белками эти вещества образуют сшивки, вызывая инактивацию некоторых из них.
Продукция сильных окислителей ускоряется при инфекционных заболеваниях, стрессах (оксидативный стресс, карбонильный стресс). Борьба с таким стрессом возможна с помощью антиоксидантов – веществ, содержащих SH-группу: глутатиона, липоевой кислоты, тиосульфата, а также витамина «С».
РЕАКЦИИ ПАРАМЕТАБОЛИЗМА В НОРМЕ.
Играют положительную роль. Сюда относятся:
1) Декарбоксилирование ацетоацетата с образованием ацетона. Ацетон летуч и быстро удаляется из организма.
2) Неферментативная реакция образования Шиффова основания: протекает в процессе зрительного восприятия между опсином и ретиналем.
3) При синтезе коллагена образуются поперечные сшивки в его молекуле неферментативным путем.
| <== предыдущая лекция | | | следующая лекция ==> |
| | | Дифференцирование под знаком интеграла |
Дата добавления: 2015-07-22; просмотров: 833;
