Понятие о кислотности и щелочности почвы
Характерным свойством почвы является ее реакция. Она определяется соотношением свободных ионов Н+ и ОН- в почвенном растворе. Концентрация свободных ионов Н+ выражается величиной РН, представляющей отрицательный логарифм концентрации ионов водорода. РН=7 характеризует нейтральную реакцию, РН<7 – кислую и РН>7 – щелочную.
Реакция почвенного раствора в различных почвах колеблется от РН 3,5 до 8-9 и выше. Наиболее кислую реакцию имеют болотные почвы верховых торфяников. Кислой реакцией почвенного раствора характеризуются подзолистые и дерново-подзолистые почвы, а также красноземы (РН 4-6). Черноземы имеют реакцию близкую к нейтральной. Наиболее щелочная реакция у солончаков, особенно содовых (РН-8-9 и выше).
Сельскохозяйственные растения предъявляют разные требования к реакции почвы. Наиболее благоприятная слабокислая и слабощелочная реакция. С реакцией почвенного раствора тесно связана жизнедеятельность почвенной микрофлоры. В кислой среде преобладает грибная микрофлора, в нейтральной или слабощелочной – бактериальная.
С реакцией почвенного раствора связаны процессы превращения компонентов минеральной и органической частей почв, растворение веществ, образование осадков, миграция и аккумуляция веществ в почвенном профиле. Кислая среда является следствием развития в почве кислотности, щелочная реакция – следствие щелочности почвы.
Кислотность почвы - способность почвы подкислять воду и растворы нейтральных солей. Различают актуальную (активная) и потенциальную (скрытая) кислотность.
Актуальная кислотность обусловлена концентрацией свободных ионов Н+ и характеризует кислотность почвенного раствора. Потенциальная кислотность характерна для твердой фазы почвы. Между актуальной и потенциальной кислотностью в почве сохраняется подвижное равновесие
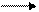
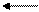 Н+тф Н+п.р, но доминирующее значение во всех почвах имеет кислотность твердой фазы почвы.
Н+тф Н+п.р, но доминирующее значение во всех почвах имеет кислотность твердой фазы почвы.
В большинстве почв актуальная кислотность обусловлена угольной кислотой и ее кислыми солями. Причиной потенциальной кислотности почвы являются обменные ионы Н+ и Al+++, т.к. при взаимодействии почвы с растворами солей эти катионы вытесняются в раствор и подкисляют его:
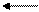
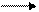 (ППК-)Н+ + КCl (ППК-) К+ + HCl;
(ППК-)Н+ + КCl (ППК-) К+ + HCl;
 (ППК-)Al+++ + 3KCl (ППК-)К+ +AlCl3
(ППК-)Al+++ + 3KCl (ППК-)К+ +AlCl3
 AlCl3+3H2O Al (OH)3 + 3HCl
AlCl3+3H2O Al (OH)3 + 3HCl
В зависимости от характера вытеснения Н+ и Al+++ различают 2 формы потенциальной кислотности: обменную и гидролитическую.
Обменная кислотность проявляется при взаимодействии почвы с растворами нейтральных солей, которые образуются при соединении сильных оснований с сильными кислотами (KCl, BaCl2, NaCl и т.п.)



 Са++
Са++
 Н+ Са++
Н+ Са++
ППК Аl+++ +4КСl ППК- Mg++ + HCl + AlCl3
 Mg++ 4K+ подкисляют раствор
Mg++ 4K+ подкисляют раствор

 Гидролитическая кислотность проявляется при обработке почвы растворами гидролитически щелочных солей, т.е. солей, образовавшихся в результате реакции между сильным основанием и слабой кислотой (CH3COONa, (CH3COO)2Ca и т. д.).
Гидролитическая кислотность проявляется при обработке почвы растворами гидролитически щелочных солей, т.е. солей, образовавшихся в результате реакции между сильным основанием и слабой кислотой (CH3COONa, (CH3COO)2Ca и т. д.).
 ППК-] H+ + 4 CH3COONa + 3H2O ППК-]4Nа + 4CH3COOH + Al (ОН)3
ППК-] H+ + 4 CH3COONa + 3H2O ППК-]4Nа + 4CH3COOH + Al (ОН)3
Al3+
Гидролитическая кислотность обычно больше обменной. Она может рассматриваться как суммарная кислотность почвы, состоящая из актуальной и потенциальной кислотности. Кислотность выражается в миллиграмм – эквивалентах (м-экв) на 100г почвы.
Для устранения кислотности почв проводят известкование.При определении степени нуждаемости почвы в известковании следует учитывать насыщенность почвы основаниями (таблица 2), а также ее гранулометрический состав и набор культур в севообороте.
Таблица 2 -Деление почв по степени нуждаемости в известковании.
| Степень нуждаемости в известко-вании | РН – солевой вытяжки | Степень насыщен-ности почвы основа-ниями (%) |
| Сильная | До 4,5 | До 50 |
| Средняя | 4,6-5,0 | 50-70 |
| Слабая | 5,1-5,5 | >70 |
| Отсутствует | >5.5 | >80 |
Дозу извести чаще всего рассчитывают по величине гидролитической кислотности. Для этого гидролитическую кислотность умножают на коэффициент 1,5; полученная величина означает дозу (в т/га), которая должна быть внесена в почву для доведения ее реакции до слабокислой
Если для известкования используют не чистый СаСО3, то проводят перерасчет на содержание СаСО3 в применяемом известковом материале, а для MgСО3, СаО и Са(ОН)2 пользуются соответственно коэффициентами 0,84;0,56 и 0,74. Можно также пользоваться дозами извести, предлагаемыми справочниками по удобрениям для отдельных почвенных разновидностей с учетом рН солевой вытяжки. На легких почвах с низкой буферностью полную дозу извести, рассчитанную по гидролитической кислотности, обычно уменьшают на 25-30%. Для отдельных культур (лен, картофель) дозу извести можно снизить на 50%. При расчете доз известкования освоенных торфяников необходимо иметь в виду значительно меньший объемный вес их по сравнению с минеральными почвами
Щелочность почвы обуславливается повышенной концентрацией в почве ионов гидроксила ОН-. Различают актуальную и потенциальную щелочность. Актуальная щелочность обуславливается наличием в почве гидролитически щелочных солей (Na2CO3, NaHCO3, Ca(HCO3)2 и др.).
 Na2CO3 +2HOH H2CO3 +2Na+ +2OH-
Na2CO3 +2HOH H2CO3 +2Na+ +2OH-
Потенциальная щелочность обнаруживается у почв, содержащих поглощенный Na.



 Na+ H+
Na+ H+

 ППК Na+ + H2CO3 ППК H+ + Na2CO3
ППК Na+ + H2CO3 ППК H+ + Na2CO3

 Na+ H+
Na+ H+
Щелочность почвы устраняют гипсованием- традиционный способ ее нейтрализации. Дозу гипса для замены натрия на кальций в ППК вычисляют по формуле:
Х= 0,086· Na· H·d,
где, Х – доза гипса в т/га;
0,086 – миллиэквиваленты гипса, в г;
Na – содержание обменного натрия, в м-экв. на 100г почвы;
Н- мощность пахотного слоя, в см;
d – плотность массы мелиорируемого горизонта, г/см3.
С изменением реакции среды тесно связано важное свойство почв – их буферность, т.е. буферная способность.
Буферностью называют способность почвы противостоять изменению реакции почвенного раствора. Буферная способность различных почв неодинакова. Почвы, богатые карбонатами (черноземы, каштановые), хорошо противостоят смещению реакции в кислую сторону, тогда как почвы, обедненные основаниями (подзолы, красноземы), имеют высокую буферность при изменении реакции в щелочную сторону. Особенно низка буферность песчаных и супесчаных почв, а также содержащих мало органического вещества.
Благодаря этому замечательному свойству почвы (буферности) возможно применение хорошо растворимых солей в качестве минеральных удобрений, в противном случае в зонах вокруг гранул удобрений создавались бы губительные для растений концентрации солей.
Контрольные вопросы:
1 Происхождение, состав и основные свойства почвенных коллоидов?
2. Что такое ацидоиды, базоиды и амфолитоиды? Дайте им характеристику.
3. Охарактеризуйте процессы коагуляции и пептизации коллоидов?
4. Как Вы понимаете поглотительную способность почвы, от чего она зависит?
5.Назовите закономерности обменного поглощения катионов и анионов в почве.
6. Назовите состав обменных катионов в основных типах почв.
7. Какова роль поглотительной способности в плодородии почв?
8. Что называется емкостью поглощения почв, от чего она зависит, в каких пределах колеблется?
9. Каковы происхождение и виды почвенной кислотности и щелочности?
Дата добавления: 2015-07-18; просмотров: 2672;
