Состав нефти. Нефть – это жидкое полезное ископаемое, состоящее в основном из углеводородных соединений
Нефть – это жидкое полезное ископаемое, состоящее в основном из углеводородных соединений. По внешнему виду это маслянистая, обычно коричневатая или чёрная жидкость со специфическим запахом. Однозначно говорить о составе нефти сложно, потому что в ней присутствуют сотни различных твёрдых, жидких и газообразных соединений. Важнейшими характеристиками нефти являются её элементный, фракционный и групповой состав.
2.2.1. Элементный и фракционный состав нефти
Элементный состав нефтей характеризуется обязательным наличием пяти химических элементов – C, H, O, N и S. Углерода в нефти 82,5–87 %, водорода 11,5–14,5 %, кислород встречается в виде различных соединений (кислоты, фенолы, эфиры) в количестве 0,05–3,6 %. Азота в нефти не более 1,7 %, содержание серы составляет от десятых долей процента до 5–8, редко 14 %. Сера – крайне нежелательный компонент нефти, потому что она способствует коррозии оборудования.
При сжигании нефтей образуется небольшое количество золы – обычно сотые доли процента. В золе обнаружены кальций, магний, железо, алюминий, кремний, фосфор, ванадий, никель, германий, хром и др. Считается, что эти элементы входили в состав органических соединений, из которых образовалась нефть.
Нефть состоит из многокомпонентной смеси углеводородов. Обычными методами перегонки не удаётся разделить их на индивидуальные соединения со строго определёнными физическими константами. Поэтому пользуются понятием фракционного состава нефти. Фракция (дистиллят) – это доля нефти, выкипающая в заданном интервале температур. При температуре начала кипения выпадает первая капля сконденсировавшихся паров. Испарение фракции прекращается при температуре конца кипения. Процентное содержание фракций в нефтях характеризует возможность получения дистиллятов моторных топлив и смазочных масел. Бензины выкипают в пределах 30–205 оС, керосины при 150–315, дизельные топлива при 180–350, масла до 350 оС и выше. Большинство нефтей содержит 15–25 % бензиновых фракций, выкипающих до 180 оС, и 45–55 % фракций с температурой конца кипения 300–350 оС.
2.2.2. Групповой состав нефти
Групповой состав нефти характеризует количественное содержание трёх основных групп углеводородов: парафиновых, нафтеновых и ароматических (рис. 2.2). Выбор метода переработки, ассортимент и эксплуатационные свойства получаемых нефтепродуктов зависят от группового состава.
Парафиновые (метановые, или алканы) углеводороды имеют химическую формулу СnH2n+2, где n – число атомов углерода. Оно может меняться от 1 до 60. В нормальных условиях при атмосферном давлении и температуре плюс 20 оС соединения с числом атомов углерода от 1 до 4 – это газы метан, этан, пропан, бутан. Если n равно 5–15, то это жидкости; при n ³16 парафины представляют собой твёрдые вещества. Температура плавления парафинов находится в пределах 52–62 оС. На глубине в условиях высоких температур и давлений они находятся в жидком состоянии, но при добыче начинают выпадать из нефти на забое скважин, в подъёмных трубах или промысловых нефтепроводах, тем самым засоряя их.
а б в
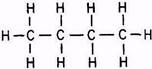
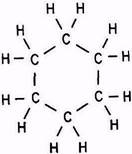
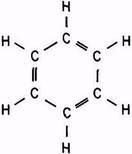
Рис. 2.2. Структурные формулы углеводородов:
а – парафиновые, или метановые (алканы); б – нафтеновые (цикланы);
в – ароматические (арены)
В парафиновых углеводородах валентность всех атомов углерода насыщена до предела. Каждый атом углерода связан с соседями простыми одинарными связями, поэтому метановые углеводороды называют насыщенными, или предельными. Химическая активность таких соединений небольшая.
Нафтеновые углеводороды (цикланы) открыл в 1880-х гг. русский учёный В. В. Марковников. Цикланы имеют общую формулу СnH2n, их молекулы циклического строения. Нафтеновые углеводороды, как и метановые, тоже насыщенные. Они являются основными компонентами моторных топлив и смазочных масел.
Ароматические углеводороды (арены) – важная и обширная группа. Их формула СnH2n-6, где n начинается с 6. В структуре аренов имеются особые связи: атомы углерода через один соединены не одинарными, а двойными связями. Арены – непредельные углеводороды (ненасыщенные), для них характерны реакции замещения атомов водорода атомами других элементов – хлора, брома, йода; они вступают в реакцию с кислотами. Ещё ароматические углеводороды легко реагируют с водородом и в присутствии катализатора могут восстанавливаться до нафтенов. Это свойство используется при переработке нефтей на нефтеперерабатывающих заводах. Арены – хорошие растворители органических веществ, но они ядовиты. Индивидуальные ароматические углеводороды: бензол, толуол, ксилолы, нафталин – ценное сырьё для нефтехимического и органического синтеза.
Дата добавления: 2015-06-27; просмотров: 1765;
