Взаимодействие клеток с полимерной поверхностью скаффолда.
(Влияние химических, энергетических и морфологических параметров) и принципы модификации полимерной поверхности для улучшения ее взаимодействия с клетками).
Самой серьезной проблемой в тканевой инженерии является взаимодействие живых клеток с поверхностью скаффолда. Эта проблема важна во многих областях биологии и медицины – хранение донорской крови, протезирование органов и тканей и многое другое. Однако наиболее существенную роль взаимодействие клеток, предназначенных для выращивания тканей, с поверхностью полимерного материала имеет именно в тканевой инженерии. Эти клетки на протяжении всего процесса выращивания ткани – от посева их в скаффолде и до имплантации в организм – должны вести себя определенным образом. На первой стадии они должны адсорбироваться на поверхности полимерного изделия. При этом силы, определяющие адсорбцию должны быть достаточными для связывания клетки, но не быть настолько большими, чтобы клетку деформировать. На последующих стадиях развития клетки, генерируя белки внеклеточного матрикса (коллаген, фибронектин и другие), сами создают благоприятную для себя поверхность, вслед за чем идет интенсивная пролиферация (размножение) клеток с их интеграцией в единую ткань. Параллельно с этим идет процесс дезинтеграции полимерного материала скаффолда.
Силы, определяющие адсорбцию клеток на поверхности скаффолда, можно разделить на несколько групп по их природе:
· неспецифические слабые нековалентные взаимодействия, определяемые, главным образом свободной энергей поверхности полимерного материала (точнее, свободной межфазной энергией на границе полимер-физиологическая среда);
· электростатические взаимодействия отрицательно заряженной клетки с поверхностью полимерного материала;
· высокоспецифические взаимодействия рецепторов клетки со связывающими химическими агентами, как правило, пептидной природы, иммобилизованными на поверхности полимерного материала;
Кроме физико-химических и биоспецифических факторов на связывание клеток с поверхностью оказывает существенное влияние и морфология поверхности. Исследования влияния характера поверхности на адсорбцию клеток проводятся в основном на пленках, так как и создавать определенную морфологию поверхности, и исследовать ее в трехмерных образцах значительно сложнее, чем на пленках. Создание полимерных материалов с определенной морфологией поверхности можно достигать различными способами – использованием различных комбинаций полимер – растворитель (или смесь растворителей), изготовлением пленок из смесей полимеров или же термической или химической обработкой пленки после ее изготовления.
Что касается свободной энергии поверхности, она определяется, главным образом, химической природой полимерного материала. Самые низкие значения свободной энергии поверхности имеют (пер)фторированные полимеры (для тефлона – 18 мДж/м2). Взаимодействие таких поверхностей с клетками ничтожно, что позволяет использовать их для хранения донорской крови и других целей. Для того чтобы клетки уверенно адсорбировались на поверхности скафолда, необходимы более высокие значения свободной энергии поверхности. Как взаимосвязанный фактор важное значение имеет гидрофильность поверхности. Большая часть клеток (кроме клеток жировой ткани) функционируют в водной среде, поэтому имеют высокое сродство к гидрофильным поверхностям. Полигидроксиалканоаты наиболее широко используемые для изготовления скаффолдов, имеют гидрофобную поверхность, что понижает адсорбцию на них клеток.
Для увеличения гидрофильности поверхности скаффолдов, изготовленных из полигидроксиалканоатов, используют различные приемы. Одним из наиболее распространенных является обработка поверхности растворами белков внеклеточного матрикса. Этим достигается сразу два эффекта – повышается гидрофильность и биосовместимость поверхности. Показано, что использование для адсорбции клеток пленок, обработанных раствором коллагена, позволяет существенно повысить количество сорбируемых клеток на единицу поверхности. Более того, эти клетки практически сразу, без дополнительной адаптации, оказываются способными к пролиферации. Недостатком реализации такого подхода является то, что коллаген и другие белки матрикса в физиологической среде очень быстро десорбируются с полимерной поверхности. Для предотвращения этого используют их ковалентное связывание, например, глутаровым диальдегидом.
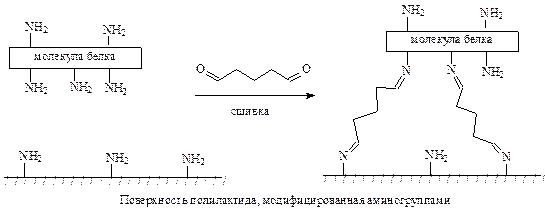
Однако для реализации такого подхода нужно иметь полимерные материалы, несущие на поверхности аминогруппы. Очень удобным для этих целей оказывается хитозан, количество аминогрупп в котором можно легко регулировать степенью гидролиза ацетамидных групп. В структуру полигидроксиалканоатов, наиболее подходящих для конструирования скаффолдов, вводят звенья лизина путем сополимеризации лактида с соответствующим морфолиндионом. В результате после удаления защитной карбобензокси группы в боковых цепях образуются аминогруппы.
Наличие на поверхности скаффолда положительно заряженных аминогрупп играет роль не только для ковалентного связывания белков матрикса. Такие аминогруппы увеличивают адсорбцию клеток за счет электростатического взаимодействия с отрицательно заряженной поверхностью клетки. Для увеличения этого взаимодействия Лангер реализовал прививочную полимеризацию N-карбоксиангидрида ε-карбобензокси лизина на аминогруппах лизина в цепях сополимера.
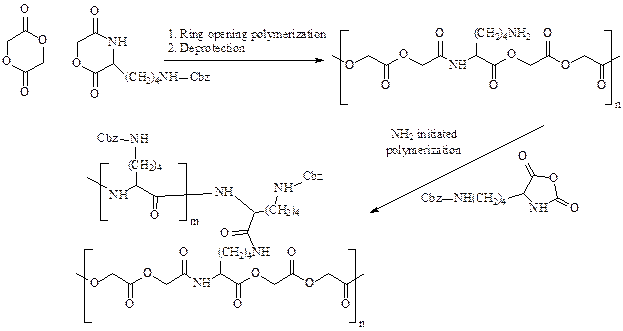
Одним из интересных подходов к увеличению сродства полимерной поверхности скаффолда к адсорбируемым клеткам является ковалентное связывание с поверхностью полимера т.н. «связывающих» пептидов. Наиболее изученным является трипептид аргинил-глицил-аспартил (RGD-пептид), взаимодействующий со связывающими рецепторами клеток. Введение его даже в незначительных количествах позволяет значительно увеличить адсорбцию клеток на поверхности. Работы по биоспецифическому связыванию клеток с поверхностью полимерного материала с использованием связывающих пептидов развиваются сравнительно недавно. Пока нет данных о влиянии способа прививки пептида к поверхности, позволяющего получить лучшие результаты. Однако эти работы обещают большие успехи в исследовании физико-химии и биохимии взаимодействия живых клеток с поверхностями различной природы.
Очевидно, что методы тканевой инженерии скоро займут достойное место не только в заместительной хирургии, но и в лечении заболеваний, против которых современная медицина пока бессильна. Важный вклад в достижение этих результатов должно внести создание новых биодеструктируемых полимерных материалов.
Дата добавления: 2015-06-22; просмотров: 2457;
