Сложные реакции
В биологических процессах химические и биохимические реакции часто образуют сложные каскады, включающие целый ряд элементарных актов реакций, протекающих последовательно или одновременно. Кинетика таких многокомпонентных (многостадийных) процессов основывается на уже знакомых закономерностях.
Несколько последовательно протекающих элементарных реакций образуют линейные цепи реакций: 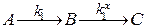 , каждая стадия характеризуется своей константой скорости (k1 и k1x, соответственно).
, каждая стадия характеризуется своей константой скорости (k1 и k1x, соответственно).
Рассмотрение данного примера так же начнем с установления граничных условий: в момент времени t = 0 a = a0, b = c = 0; в любой момент времени a + b + c = a0.
Кинетическое описание данной цепи реакций можно представить в виде системы уравнений:
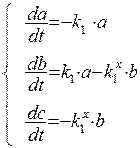
Первая формула представляет собой уравнение скорости реакции первого порядка, решение которого имеет вид
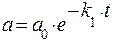
Тогда, с учетом b=a0–a–c
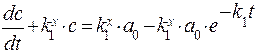
Общее решение этого уравнения складывается из решения однородного уравнения с правой частью, равной нулю, и частного решения неоднородного уравнения:
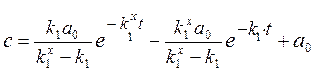
Используя заданные граничные условия, можно получить формулу и для кинетики вещества В:
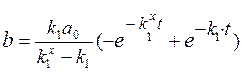 .
.
В первую фазу процесса происходит накопление вещества В, а во вторую – вещества С.
Если скорость первой реакции существенно выше, чем второй, в системе образуется избыток вещества В и вторая реакция начинает подчинятся кинетическому уравнению нулевого порядка. Тогда накопление вещества С в системе перестанет зависеть от скорости первой реакции и будет подчиняться уравнению:
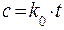
В результате скорость линейной цепи реакций полностью определяется ее второй стадией, которую в этом случае называют лимитирующей стадией процесса.
Если цепь последовательных реакций замыкается, то есть конечный продукт цепи является субстратом для ее первой стадии, такую реакцию называют циклической.
Циклические реакции нередко встречаются в биохимических системах, играя важную роль в процессах метаболизма, широко известен цикл Кребса. Скорость цикла всегда определяется скоростью лимитирующей (то есть самой медленной) стадии.
Разветвленные (параллельные) цепи реакций
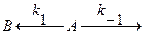 протекают на условиях
протекают на условиях 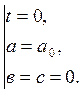
В результате, необходимо решить систему уравнений:
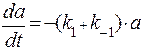
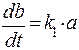
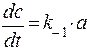
Решая эти уравнения, получим:
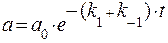
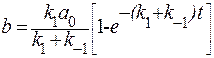 и
и 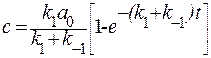
Нетрудно увидеть, что b/с=k1/k-1., т.е. соотношение образующегося вещества при параллельных реакциях пропорционально отношениям констант скоростей реакций.
Дата добавления: 2015-06-22; просмотров: 1152;
