Энтропия. Принцип минимума производства энергии
Энтропи́я (от греч. ἐντροπία — поворот, превращение) – эта функция используется во многих науках. В термодинамике понятие энтропии впервые было введено Клаузиусом в 1865 году для определения меры необратимого рассеивания энергии, меры отклонения реального процесса от идеального. Ее изменение находится как отношение подведенной (отведенной) к системе теплоты к абсолютной температуре

Клаузиусом получены следующие положения, которые мы принимаем без доказательства:
а) энтропия системы, состоящей из нескольких тел, равна сумме энтропий этих тел.
б) если в изолированной системе происходят необратимые процессы, то ее энтропия возрастает.
в) энтропия изолированной системы не может уменьшаться ни при каких процессах.
Математически эти выражения записываются в виде неравенства Клаузиуса:
 .
.
Пока речь шла только об изменении энтропии. Нерстом же была показана возможность определить абсолютное значение энтропии, хотя бы для одной температуры. Теорема Нерста (третье начало термодинамики) гласит, что при стремлении абсолютной температуры к нулю, энтропия любого тела также стремится к нулю:
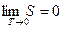 .
.
Изложенные выше вопросы относятся в основном к равновесным процессам или к процессам, приводящим к равновесным состояниям. Однако реальные процессы и состояния в природе и технике являются неравновесными, а многие системы – открытыми. Эти процессы и системы рассматриваются в неравновесной термодинамике.
Аналогично тому, как в равновесной термодинамике особым состоянием является состояние равновесие, так в неравновесной – особую роль играют стационарные состояния.
Несмотря на то, что в стационарном состоянии необратимые процессы, протекающие в системе, увеличивают энтропию, энтропия системы не изменяется. Как понять это противоречие?
Пригожин указал экстремальное значение некоторой функции, сформулировав принцип минимума производства энтропии: в стационарном состоянии системы скорость возникновения энтропии вследствие необратимых процессов имеет минимальное значение при данных внешних условиях, препятствующих достижению системой равновесного состояния (dS/dt>0 и минимальна)
Согласно этому принципу в системе при стационарном состоянии внутренние неравновесные процессы протекают так, что ежесекундный прирост энтропии минимален. Это означает, что система за счет внутренних необратимых процессов не способна выйти из стационарного состояния. Так, если за счет небольших отклонений (флуктуаций) система несколько и отклонилась бы от стационарного состояния, то стремление внутренних процессов уменьшить dS/dt вернет систему вновь к этому состоянию.
Необходимо отметить, что это справедливо при заданных и неизменных внешних условиях. При изменении внешнего воздействия (потоков входящих и выходящих из системы) система уходит из одного стационарного состояния и переходит в другое, если новые внешние условия будут сохраняться во времени.
Дата добавления: 2015-06-22; просмотров: 909;
