II. Прямое окисление этилена.
Этот процесс, разработанный Шмидтом, является одним из новейших в промышленном органическом синтезе.
Окисление алкенов по ненасыщенному атому углерода, в частности этилена, происходит под воздействием хлорида палладия.
PdCl2 + C2H4 + H2O = CH3–CHO + Pd + 2HСl
Заслуга Шмидта состоит в создании окислительно-восстановительной системы, в которой Pd быстро окисляется, т.е. непрерывно регенерируется в активной форме. Это происходит при добавлении в раствор хлорида меди (II). Она окисляет Pd, переходя в Cu+, легко окисляемую кислородом воздуха. Соли меди при этом являются переносчиками кислорода
Pd + 2Cu2+ = Pd2+ + 2Cu
2Cu+ + 0,5O2 + 2H+ = 2Cu2+ + H2O
Суммарная реакция:
С2Н4 + 0,5О2 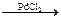 CН3–СНО
CН3–СНО
Реакция протекает в кислой среде, в которой соли палладия находятся в форме Н2[PdCl4]. Механизм процесса заключается в замещении хлорид-ионов во внутренней сфере палладиевого комплекса молекулами этилена и воды и перегруппировками внутри образующегося комплекса.
В случае одностадийного процесса (с восстановлением и окислением катализатора в одном аппарате) условия процесса и соотношение компонентов подбирается таким образом, чтобы скорости самого синтеза, окисление или восстановление солей Pd протекали с одинаковыми скоростями. Это зависит от концентрации PdCl2, CuCl2 и рН среды. Лучшие результаты достигаются с водными каталитическими растворами, содержащими 0,3-0,5% PdCl2, 12-33% CuCl•2H2O, 2-3% Cu(CH3COO)2.
Достаточно интенсивно идёт реакция при 100-1300С при давлении до 10 атм. При этом необходима интенсивная турбулизация жидкости реакционными газами, и во избежание побочных реакций конденсации и смолообразования быстрая отдувка получающегося альдегида.
Высокая коррозионная активность каталитических растворов и паро-газовых смесей обусловили применение титана для изготовления основной аппаратуры.
Дата добавления: 2015-06-17; просмотров: 2978;
