Коензим Q
Синоніми:кофермент Q, Ко Q, убіхінон. Коензим Qзначно поширений кофермент, звідси його інша назва «убіхінон» – «всюдисущий хінон».
Хімічна структура та властивості
· За хімічною структурою убіхінонє 2,3-диметокси-5-метил-1,4-бензохінон із ізопреновим ланцюгом у 6-му положенні.
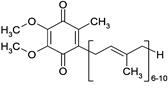
Убіхінон
· Число залишків ізопрену у бічному ланцюгу убіхінону варіює від 6 до 10, що позначають як КоQ6 – Ко Q10. У мітохондріях клітин людини та тварин зустрічається убіхінонлише з 10 ізопреновими ланцюгами.
· Ко Q являє собою жовто-оранжеві кристали без смаку і запаху. Температура плавлення 49–51° С.
· Він розчинний у діетиловому ефірі, дуже слабо розчинений в етанолі, практично не розчиняється у воді.
· На світлі поступово розкладається і забарвлюється. З водою утворює емульсію з концентраціями 10 %, 20 % і 40 %.
Біосинтез
В організмі людини Коензим Qможе синтезуватися з мевалонової кислоти та продуктів обміну тирозину. Цей процес відбувається в печінці, охоплює 17 етапів, потребує 7 вітамінів та декілька мікроелементів. У зв′язку з тим що убіхінонутворюється в організмі, він не є істинним вітаміном, але при окремих патологічних станах, пов'язаних із порушеннями харчування, Коензим Q стає незамінним фактором.
Нормальна концентрація убіхінону в крові: 1,0 мг/мл.
Поширення у тканинах. Коензим Qнеобхідний для нормального функціонування тканин з високим рівнем енергетичного обміну. Найбільша концентрація убіхінону у серцевому м'язі, печінці, нирках, підшлунковій залозі.
Поширення у природі та добова потреба
Убіхінон відкритий у всіх живих клітинах: рослин, тварин, грибів, мікроорганізмів. Усередені клітин убіхінонлокалізова-ний виключно у мітохондріях.
Джерела:
· продукти рослинного походження: соєва олія, арахіс, фісташки, броколі, кольорова капуста, апельсини, суниці;
· продукти тваринного походження: яловиче серце, курятина, риба, печінка, яєчний жовток.
У процесі кулінарної обробки кількість Ко-Q у продуктах знижується.
Добова потреба в убіхіноні невідома. У середньому людина вживає 5 мг Ко-Q10 за добу, що недостатньо для забезпечення організму. Решта синтезується у самому організмі з тирозину. З віком здатність організму синтезувати Коензим Qпомітно знижується, тому людям старшого віку потрібно додатково вживати його з їжею. Знижують кількость убіхінону в організмі стресові стани, переохолодження, рівень гормонів, фізична активність, вживання деяких лікарських засобів та ін.
Потреба у вітаміні збільшується у хворих на ішемічну хворобу серця, при гіпертензії, ревматичних пороках серця, інфекційних захворюваннях, цукровому діабеті.
Біологічна роль
КоферментQ є компонентом ланцюга перенесення електронів у мітохондріях, бере участь у реакціях окисного фосфорилюванняі синтезу АТФ.
· За рахунок донорно-акцепторних властивостей він виконує колекторну функцію – переносить відновлювальні еквівален-ти від І комплексу (НАДН-КоQ–редуктази) та ІІ комплексу (Сукцинат-КоQ–редуктази) дихального ланцюга.
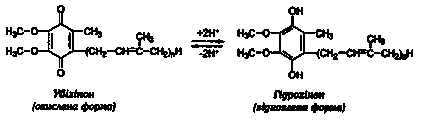
· Коензим Q10 проявляє антиоксидантнівластивості, здатен регенерувати в організмі, а також відновлювати антиоксидантнівластивості вітаміну Е.
· Антиоксидантна дія убіхінону зумовлена його відновленою формою (Ко–QН2), активність якої на три порядки вище невідновленої:
2LOO· + Кo-QH2 → 2LООН + Ко-Q·.
· КоферментQ бере участь у підтриманні нормального функціонування імунної системи.
Прояви вітамінної недостатності та застосування
Дефіцит Ко–Q10 виникає при недостатньому надходженні його з їжею, порушенні біосинтезу в організмі, підвищеному використанні в організмі або комбінації цих факторів. Нестача убіхінону може бути причиною серйозних захворювань.
Відмічено, що у людей, які страждають на серцево-судинні патології, спостерігається зниження кількості Ко-Q. Його неста-ча має негативний вплив на перебіг захворювань, сприяє розвит-ку дистрофічних процесів у міокарді, зниженню його скорочу-вальної функції та проявам серцевої недостатності. Недос-татність убіхінону також відмічена у хворих на цукровий діабет.
Існує думка, що старіння (зниження функціональних можливостей серця та інших органів) пов′язане зі зниженням концентрації коферменту Q. Як наслідок, відбуваються зменшення інтенсивності енергетичних процесів та зниження імунітету у людей похилого віку, тому вони більшою мірою схильні до так званих «хвороб старечого віку». Міокард людей старше 60 років містить на 40–60 % менше убіхінону, ніж міокард молодих людей.
Зниження концентрації коферменту Q в організмі може відбуватися при різних захворюваннях. Вважається, що такі дегенеративні захворювання, як атеросклероз, хвороба Паркін-сона, хвороба Альцгеймера пов'язані з природною недостатніс-тю синтезу Ко-Q. Дефіцит коферменту може виникати при гіпертиреозі, гепатитах, бронхіальній астмі.
Убіхінон використовують у комплексній терапії багатьох патологій, а також як речовину, що значно гальмує процеси старіння і допомогає попереджувати та призупиняти вікові зміни. Його призначають при лікуванні всіх форм ішемічної хвороби серця, інших захворювань міокарда, серцевої недостатності, цукрового діабету.
Оскільки Ко-Q підвищує толерантність до фізичних навантажень, він використовується після перевтоми, перед виконанням значних фізичних навантажень, у спорті.
Піролохінолінхінон ( РQQ)
Синоніми:вітамін В14, метоксантин (methoxantin).
Хімічна структура та властивості
Нещодавно відкрито новий клас білків – хінопротеїни, або РQQ-ферменти, які як кофермент містять невідому раніше вітаміноподібну речовину піролохінолінхінон(РQQ).
· за хімічною структурою РQQє похідним хінону;
·  піролохінолінхінон– термостабільна речовина, яка добре розчинна у воді.
піролохінолінхінон– термостабільна речовина, яка добре розчинна у воді.
· РQQбере участь у циклічних окисно-відновних реакціях.
· За наявності амінокислот РQQутворює велику кіль-кість імідазолових та оксазо-лових похідних.
Піролохінолінхінон (РQQ)
Поширення у природі та добова потреба
Піролохінолінхінон значно поширений у мікроорганізмів, у тканинах тварин та рослин. Піролохінолінхінон може синтезу-ватися багатьма бактеріями. Винятком є більшість бактерій тонкого та товстого кишечнику, хоча для цього є всі можливості (субстрати, ферменти, умови). У той самий час бактерії використовують РQQяк вітамін.
Джерела:
· продукти рослинного походження: хліб, картопля, капуста, морква, шпинат, селера, томати, петрушка, зелений чай, зелений перець, папайя, соєві боби, кормові боби, батат, банани, апельсини.
Біологічна роль
Піролохінолінхінон входить як кофермент до складу бактері-альних ферментів – метанолдегідрогенази, алкогольдегідроге-нази. З тканин тварин, рослин, грибів, дріжджів виділений Сu-вмісний фермент метиламінооксидаза, у якому є ковалентно зв′язаний РQQяк коензим.
РQQможе одночасно проявляти властивості аскорбінової кислоти (відновлювальні), рибофлавіну (окисно-відновні реакції), піридоксальфосфату (карбонільна активність). Він здатен замінювати рибофлавіну деяких оксидоредуктазах.
Піролохінолінхінон – кофермент окисно-відновних реакцій у тварин, наприклад коензим алкогольдегідрогенази. Доведено наявність РQQу багатьох тканинах організму людини, у грудному молоці.
Тваринні та рослинні хінопротеїни входять до складу оксидазта декарбоксилаз (амінооксидаз, діамінооксидаз, монооксигеназ, діоксигеназ). Можливо, що є два коферменти – піридоксальфосфатта РQQ- у складі деяких декарбоксилаз амінокислот (глутаматдекарбоксилази, ДОФА-декарбоксилази).
РQQ-дегідрогенази та оксидазиза механізмом дії аналогічні до флавопротеїнів, які каталізують перенесення 2Н+ та 2ė, можливо безпосередньо на убіхінон.
РQQ-декарбоксилази, навпаки, подібні за механізмом дії до піридоксалевих коферментів, оскільки обидві системи містять карбонільну групу.
Піролохінолінхінон бере участь у:
· розвитку клітин та внутрішньоклітинних структур;
· репродуктивних процесах;
· імунних процесах.
· Піролохінолінхінон має антиоксидантні, протизапальні властивості.
Слід відмітити, що вітамінні властивості РQQще не вивчені до кінця.
Прояви вітамінної недостатності та застосування
Недостатність РQQсупроводжується розладами шлунка, серцево-судинними захворюваннями, дисфункцією печінки.
Ліпоєва кислота
Синоніми:вітамін N, тіоктова кислота, 6,8-дитіооктанова кислота.
Хімічна структура та властивості
За хімічною структурою α-ліпоєва кислотає 1,2-дитіолан-3-валеріановою кислотою.
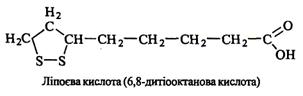
· Ліпоєва кислота– кристалічна речовина жовтого кольору із специфічним запахом та гірким смаком.
· Нерозчинна у воді, але розчинна у органічних розчинниках (етанолі, хлороформі, циклогексані).
· Руйнується при термічному обробленні.
· Під дією розчинів лугів ліпоєва кислотаполімеризується, утворюючи лінійні полімери, у яких залишки кислоти зв'язані дисульфідними містками.
· Під дією відновників ліпоєва кислоталегко перетворюється на 6,8-дигідроліпоєву.
Поширення у природі та добова потреба
Вперше ліпоєву кислоту виділено з дріжджів та тканини печінки як фактор росту молочнокислих бактерій, які не можуть його синтезувати. У природі ліпоєва кислотапоширена у тканинах тварин, рослин, мікроорганізмів.
Джерела:
· продукти рослинного походження: зелені частини рослин, боби, шпинат, броколі, картопля, морква, буряк, фрукти, дріжджі;
· продукти тваринного походження: яловичина, молоко, печінка;
· ліпоєва кислотав організмі тварин та людини синтезується в основному мікрофлорою кишечнику, що забезпечує власні потреби. З віком здатність виробляти ліпоєву кислоту зменшується.
Добова потреба у ліпоєвій кислоти для дорослих здорових людей становить у середньому 30мг/добу.
Рекомендоване добове споживання:
· дорослі: 25 – 50 мг
· вагітні жінки та період лактації: 75 мг
· діти: 12,5 – 25 мг
Потреба у ліпоєвій кислоті підвищується у людей із захворюваннями печінки.
Біологічна роль
Ліпоєва кислотабере участь в окисно-відновних процесах в організмі. Вона може існувати у відновленій (SH-) і окисненій (S-S) формах, чим зумовлені її коферментні функції:
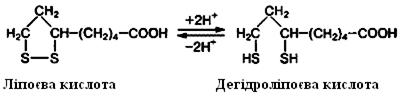
· Ліпоєва кислоташвидко відновлюється до дегідроліпоєвої з 2 активними сульфгідрильними групами (SH-), які мають редукуючі властивості.
· Ліпоєва кислотабере участь у процесах окисного декар-боксилювання α-кетокислот як переносник ацильних груп та атомів Н+ у складі мультиферментних комплексів:
1 піруватдегідрогеназного, який окиснює та декарбоксилює ПВК до ацетил-КоА;
2 α-кетоглутаратдегідрогеназного, що є компонентом циклу трикарбонових кислот;
3 дегідрогенази α-кетокислот із розгалуженими бічними лан-цюгами. Відповідні кетокислоти (ацетил-КоА, ізовалерил-КоА, сукциніл-КоА) утворюються при трансамінуванні амі-нокислот із розгалуженими бічними ланцюгами (лейцину, валіну, ізолейцину);
4 система розщеплення гліцину (СРГ) – мультиензимний комплекс, який розташований у матриксі мітохондрій гепа-тоцитів і каталізує окиснення гліцину до СО2, NН3, НАДН, (N5N10)-метилентетрагідрофолату.
· Вітамін Nбере участь у процесах аеробного окиснення вуглеводів, ліпідів, амінокислот і їх синтезі. Він сприяє засвоєнню глюкози клітинами (має інсуліноподібний ефект),
· У структурі ферменту ліпоєва кислотазв′язується з білковою частиною пептидним зв′язком, який формується за рахунок її карбоксильної групи та аміногрупи залишку лізину апоферменту.
· Ліпоєва кислотамає ліпотропний ефект, попереджаючи жирове переродження печінки. Вона зменшує використання глутатіону– важливого внутрішньопечінкового антиокси-данта;
· Знижує концентрації жирних кислот, загального холестеролу та його ефірів у сироватці крові.
· Ліпоєва кислота– «універсальний антиоксидант», підсилює дію інших антиоксидантів(вітамінів С, Е, глутатіону). Вона є компонентом каскадної системи у якій після окиснення вітамінів С, Е глутатіон відновлює їх, сам глутатіон у подальшому відновлюється ліпоєвою кислотою. Цей механізм сприяє збереженню та економному використанню запасів вітамінів.
· За рахунок антиоксидантнихвластивостей ліпоєва кислотамає радіопротекторну дію; сприяє знешкодженню важких металівта їх солей, фосфорорганічних сполук, ціанідів, сполук миш’яку, сурми, етанолу та інших токсичних сполук.
Прояви вітамінної недостатності та застосування
Специфічні прояви гіповітамінозу не описані.
Ліпоєва кислотавикористовується у медичній практиці з профілактичною та лікувальною метою:
· при порушеннях вуглеводного та ліпідного обміну;
· у терапії цукрового діабету, при інсулінорезистентності, діабетичній полінейропатії, діабетичній нефропатії;
· при гострих та хронічних захворюваннях печінки: жировому переродженні печінки, початкових стадіях цирозу, алкогольному гепатиті;
· при поліневритах, для покращання концентрації уваги та пам'яті;
· при отруєннях солями важких металівта інших інтоксикаціях;
· при коронарному атеросклерозі, серцевій недостатності;
· при деяких захворюваннях шкіри;
· для профілактики і корекції захворювань судин.
Холін
Синоніми:вітамін В4, Вр. Уперше винайдений у жовчі, звідки походить його назва.
Хімічна структура та властивості
· За хімічною структурою холін- 2-оксіетил-триметиламоній – аміноетиловий спирт, який містить у своєму складі атом азоту і три метильні групи (СН3-). Зазвичай його відносять до вітамінів групи В:
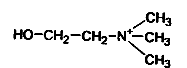 .
.
· Холін – термостабільний аміноспирт, який утворює безбарвні кристали, добре розчинні у воді, етиловому спирті, не розчинні в ефірі та бензолі.
· Холін легко утворює солі з сильними кислотами, його водні розчини мають властивості сильних лугів.
Метаболізм
Холін здатен синтезуватися в організмі людини і тварин, але при нестачі у раціоні білків, які містять амінокислоту метіонін – донора метильних груп під час утворення холіну, може розвинутися вторинна холінова недостатність. Слід зазначити, що в організмі утворюється не вільний холін, а холіну складі фосфоліпідів.
Метаболізм холінупов'язаний із метаболізмом інших вітамінів:
- вітамін В12 та фолієва кислотасприяють синтезу холінув організмі людини;
- тіамін(вітамін В1) протидіє ліпотропній дії холінуна печінку, оскільки стимулює утворення жиру з вуглеводів;
- нікотинова кислота(вітамін В3) утилізує метильні групи, які беруть участь в утворенні холіну, тим самим перешкоджаючи його синтезу.
Поширення у природі та добова потреба
Холін дуже поширений у природі – рослинах, тваринах, мікроорганізмах.
Джерела:
· продукти тваринного походження: особливо багатий на холіняєчний жовток. Він також міститься у печінці, нирках, мозку, серцевому м’язі, сирі, молоці, м'ясі;
· продукти рослинного походження: капуста, шпинат, бобові, зернові культури, соя, нерафінована рослинна олія.
· Синтезується у достатній кількості в організмі людини і тварин.
Добова потреба у вітаміні В4 залежить від раціону харчування, значною мірою визначається наявністю у ньому білків, вітамінів В12 та В6. Для дорослих вона у середньому становить від 0,5 – 1,5 г/добу.
Потреба у холіні підвищується при зниженні у їжі кількості білків, на фоні лікування сульфаніламідними препаратами, під час приймання естрогенів, вживанні великих доз алкоголю.
Біологічна роль
· Як донор метильних груп (СН3-) холінбере участь у реакціях трансметилюванняпри біосинтезі фосфоліпідів, ацетилхоліну, метіоніну, пуринових та піримідинових нук-леотидів.
· Холін є попередником ацетилхоліну– одного з основних медіаторів нервової системи.
· Вітамін В4входить до складу фосфоліпідів(фосфатидил-холіну, або лецетину, сфінгомієліну), що є основними компонентами клітинних мембран.
· Холін – це ліпотропна речовина, яка має гепатопротектор-ний ефект – запобігає розвитку жирової дистрофії печінки за рахунок стимулювання синтезу в ній фосфоліпідів. Дію холінупідсилює інозитол. Вітамін В4також сприяє накопиченню у гепатоцитах глікогену, знижує рівень холестеролу, запобігає утворення жовчних каменів.
· Холін проникає через гематоенцефалічний бар'єр і впливає на функціональний стан центральної нервової системи, сприяє покращанню розумової діяльності та пам′яті.
· Він попереджає розвиток атеросклерозу, зменшує та усуває дистрофічні зміни у міокарді та інших внутрішніх органах.
· Для холінухарактерно: антианемічна, мембранопротекторна; антиатеросклеротична, ліпотропна дія; він відновлює структуру нервової тканини, покращує її метаболізм, має ноотропну, антидепресантну, анксіолітичну дію.
Прояви вітамінної недостатності
Зниження забезпечення організму холіномвиникає при його обмеженому надходженні з їжею, дефіциті вітамінів В12 та Вс, а також надмірному надходження речовин, які утилізують метильні групи на кшталт нікотинової кислоти(вітаміну РР).
Дефіцит холінупризводить до:
· порушення обміну ліпідів в організмі;
· розвитку жирової інфільтрації печінки, цирозу;
· дегенерації канальців нирок;
· кровотеч через порушення згортання крові (зниження синтезу V фактора згортання крові);
· затримки росту;
· розвитку атеросклерозу та серцевих захворювань.
Великі дози холінутоксично впливають на організм людини, викликаючи підвищення секреції слинних залоз, зниження артеріального тиску, пригнічення серцевої діяльності, підвищення перистальтики кишок.
Застосування холіну
У медицині холінвикористовують:
· для лікування гострих і хронічних захворювань печінки: гепатиту, цирозу, жирової дистрофії печінки, жовчокам'яної хвороби;
· при атеросклерозі, гіперхолестеринемії, ішемічній хворобі серця, міокардіодистрофії, артеріальній гіпертензії;
· при анемії, порушеннях пам'яті, депресії, фобії, безсонні, хворобі Альцгеймера, поліневриті; алкоголізмі.
Ураховуючи, що холін– найважливіший компонент фосфо-ліпідівмозку, додаткове вживання його в їжу вагітними жінками (плід не може самостійно його виробляти) і дітьми перших п'яти років життя позитивно впливає на розумові здібності малюків.
В аналітичній хімії використовують здатність холіна утворю-вати погано розчинні солі з фосфорновольфрамовою та плати-нохлористоводневою кислотами, ці властивості застосовують для визначення холіну.
Карнітин (В11)
Синоніми:Вітамін В11,L-карнітин; вітамін Вт, γ-триметил-бета-гідроксибутиробетаїн. L-Карнітин уперше виділений з екстракту тканин м'язів, звідси походить його назва (від лат. «carnis» – м’ясо). Також було встановлено, що він є незамінним фактором для росту борошнистого черв’яка Tenebrio molitor, у зв'язку з чим його назвали вітаміном Вт.
Хімічна структура та властивості
· L-Карнітин(1-3-гідрокси-4-N-(триметиламоній) масляна кис-лота, за хімічною структурою є похідним масляної кислоти:
(CH3)3N+–CH2–CH(OH)–CH2–COO–.
· L-Карнітин присутній у біологічних системах як у вільному вигляді, так і у формі ефірів, включаючи ацетил-L-карнітин (рис. 15).
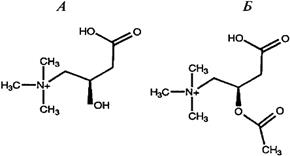
Рисунок 15 – Хімічна структура L-карнітину(А) і ацетил-L-
карнітину(Б)
Біосинтез та метаболізм
· L-Карнітин синтезується в організмі людини та тварин і знаходиться практично у всіх клітинах організму.
· Синтез L-карнітинувідбувається у печінці та нирках за участі незамінних амінокислот– лізину та метіоніну, а також за наявності вітамінів: С, В6, В3(ніацину), В12, фолієвої кислоти, Fе++.
· При нестачі хоча б одного з вищенаведених факторів власний синтез карнітинузначно знижується. Основним лімітуючим фактором є наявність аскорбінової кислоти, при дефіцити якої утворення L-карнітинуповністю припиняється і розвиваються симптоми карнітинової недостатності.
· Для синтезу карнітинупотрібно 5 ферментів.
· Проміжний продукт синтезу N-триметиллізин перетво-рюється на гідрокситриметиллізин, який у ланцюзі реакцій, що протікають як в мітохондріях так і в цитозолі клітини, далі утворює γ-бутиробетаїн. Необхідні для цих етапів біосинтезу ферменти виявлені у скелетних м'язах, серці, печінці, нирках та мозку. Перетворення γ-бутиробетаїну на L-карнітинвідбувається у реакції гідроксилювання під дією специфічної гідроксилази, яка виявлена виключно в печінці, нирках та мозку, але його немає у скелетних або серцевому м'язах.
· Установлено, що 60 % карнітинуміститься в організмі у вільному вигляді, а 40 % – у формі ацетил-L-карнітину.
· З печінки та нирок карнітинтранспортується до інших органів і тканин. Його вміст у дорослої людини становить 20–25 г, із яких 97 % знаходиться в скелетних м'язах і міокарді, тобто у тканинах, які використовують жирні кислоти як головне джерело енергії. Карнітин також міститься у жіночому молоці.
· Вміст карнітинув плазмі здорових людей дорівнює від 30 до 89 мкмоль/л.
· У мітохондріях печінки можуть утворюватися похідні L-кар-нітину з ендогенними речовинами та з ксенобіотиками.
· В організмі ссавців L-карнітинне катаболізує і не трансформується, виводиться через нирки з сечею в незмінному вигляді або у формі ацилкарнітину.
Поширення у природі та добова потреба
Основна кількість L-карнітинунадходить в організм людини з їжею тваринного походження. Фрукти і овочі містять дуже мало карнітину.
Джерела:
· продукти тваринного походження: молоко, сир, м'ясо, риба;
· продукти рослинного походження: гриби, морква, хліб, рис, банани, помідори.
· Організм людини виробляє близько 20 мг карнітинуна день. Збалансована дієта може дати ще 100–300 мг карнітинуна добу, при базовій потребі – 20 мг на 1 кг ваги тіла/добу.
Добова потреба у карнітині залежить від віку людини та його фізіологічного стану і становить приблизно від 1,0– 1,5 г/добу, при підвищених енерговитратах – 2,0–6,0 г/добу. Потреба у карнітині підвищується при вагітності, лактації, значних фізичних навантаженнях, у спортсменів, людей, які зловживають алкоголем, хворих на цукровий діабет, пацієнтів із захворюваннями серця, нирок. Карнітин у дозах більше 50 мг/кг зазвичай використовується в терапії різних захворювань.
Біологічна роль
Карнітин відіграє вирішальну роль у метаболізмі ліпідів.
1. L-карнітин виконує роль «човника» у карнітиновій транс-портній системі. Він підвищує швидкість окиснення жирів шля-хом перенесення активованих довголанцюгових жирних кислот через зовнішню мітохондріальну мембрану у матрикс для β-окиснення і використання їх як джерела енергії.
2. Контроль пулу НS-КоА у клітині. Карнітинова човникова система контролює та сприяє збереженню стабільного внутріш-ньоклітинного пулу вільного НS-КоА, який необхідний для ак-тивації карбоксиловмісних метаболітів. Тобто карнітинвключа-ється у проміжний обмін у цілому. Через регуляцію концент-рації НS-КоА у клітині L-карнітинвпливає на синтез та катаболізм жирних кислот, стероїдів, фосфоліпідів, ацетилхо-ліну, утворення кетонових тіл, функціонування ЦЛК, тобто оптимізує енергетичний метаболізм та інші процеси.
Зниження надходження L-карнітинупризводить до зменшення вмісту НS-КоА у матриксі мітохондрій, що послаб-лює не тільки β-окиснення жирних кислот, а також утилізацію вуглеводів, окремих амінокислот, енергетичні процеси, детоксикацію органічних кислот та ксенобіотиків.
3. Детоксикаційна функція L-карнітину полягає у знешкод-женні органічних кислот та ксенобіотиків, які накопичуються у мітохондріях у результаті окиснення ліпідів та екзогенних сполук. Органічні кислоти та ксенобіотики біотрансформуються через перетворення у похідні ацил-КоА, які виводяться з подальшого метаболізму. Перетворення ацил-КоА на відповідні ацилкарнітини дозволяє видалити надлишок ацильних залишків з мітохондрій у цитозоль. Ацилкарнітини здатні дифундувати через клітинні мембрани та екскретуватися з сечею.
4. Анаболічна функція. Ймовірно, ця функція L-карнітину полягає у його участі в метаболізмі мембранних фосфоліпідів.
5. Захисна дія при апоптозі. L-карнітин бере участь у енерге-тичному обміні та метаболізмі фосфоліпідів, тобто у підтриман-ні життєздатності клітини. Карнітин має захисну дію при апоп-тозі за рахунок інгібування синтезу церамідів – потужних ендо-генних промоторів клітинного апоптозу та активності специфіч-них цистеїнових протеаз (каспаз) – медіаторів апоптозу.
6. Нейрозахисний ефект. Ймовірно, цей ефект карнітинупов'язаний із підсиленням енергетичного обміну, а також зниженням утворення вільних радикалів.
У зв′язку з участю L-карнітинуу вищеназваних біохімічних процесах він виконує такі важливі функції:
· знижує рівень холестеролу, попереджаючи розвиток атеросклерозу;
· має антиоксидантнудію;
· покращує роботу серця, знижує ризик розвитку ішемічної хвороби, сприяє швидкому відновленню серцевого м′яза. Відомо, що жирні кислоти є основним джерелом енергії для кардіоміоцитів. Саме карнітинзабезпечує надходження жир-них кислот у мітохондріі клітин, їх окиснення і вивільнення енергії, яка підтримує довготривалу роботу серцевого м′яза. Дефіцит карнітинуможе стати причиною дистрофічних процесів у міокарді;
· покращує травлення, відновлює слизову ШКТ;
· активує відновлення клітин печінки;
· має анаболічну дію, насамперед в м'язовій тканині, стимулює ріст дитячого організму. Карнітин знижує накопи-чення жиру у м′язовій тканині, сприяє формуванню м'язів;
· стимулює мозкову діяльність, підвищує імунітет, сприяє сперматогенезу.
Причини та прояви вітамінної недостатності
Організм людини виробляє карнітин, а також отримує його з їжею, однак при деяких фізіологічних чи патологічних станах кількість його недостатня для підтримання нормального метаболізму, що призводить до розвитку карнітинової недостатності.
Причиною дефіциту може бути:
· неповноцінне харчування – голодування, низькокалорійна дієта, вегетаріанська дієта, оскільки фрукти та овочі вміщу-ють дуже мало карнітину. Навіть люди, які додержуються суворої дієти, повинні 2 рази на тиждень вживати м'ясо, рибу, птицю;
· порушення ендогенного синтезу карнітинуабо його всмок-тування –недостатнє надходження з їжею повноцінних білків та необхідних мікронутрієнтів для синтезу карнітину;
· уроджені та набуті порушення обміну речовин. Немож-ливість деяких хворих повною мірою синтезувати карнітинчерез порушення ферментних систем його біосинтезу внас-лідок генетичних дефектів, старіння організму або різних патологічних станів;
· захворювання печінки та нирок. Наприклад, виведення карнітинунирками у новонароджених недоношених дітей, або підвищена втрата карнітину під час гемодіалізу;
· тривале фізичне або нервово-психічне напруження;
· побічна дія ліків.
При карнітиновій недостатності порушується робота трьох основних систем організму:
1) серцевого м'яза, ушкодження якого призводить до кардіо-міопатії;
2) центральної нервової системи, порушення якої призводить до енцефалопатії;
3) скелетних м'язів, пошкодження яких призводить до міопатії.
Симптоми недостатності L-карнітинурізноманітні та несе-цифічні. Дефіцит проявляється у вигляді хронічної втоми, м′язо-вої слабості, ожиріння, дратівливості, астенії, порушень роботи серця, функцій печінки та нирок, підвищення артеріального тиску, зниження витривалості при фізичних навантаженнях.
Застосування карнітину
L-карнітинувикористовують для:
· профілактики і лікування первинного та вторинного дефіци-ту карнітину(міопатія з накопиченням ліпідів, синдром Марфана, синдром Елерса-Данлоса та ін.);
· лікування порушеннь метаболізму у міокарді при хронічній ішемічній хворобі серця, стенокардій, інфаркті міокарда;
· лікування захворювань головного мозку і фізіологічних змін ЦНС, викликаних, у тому числі, старінням;
· профілактики атеросклерозу, інфаркту, інсультів, гіпертонії;
· стабілізації оптимальної ваги тіла, насамперед у поєднанні зі спортивними тренуваннями.
· У дітей повноцінний синтез L-карнітинупочинається приб-лизно з 15 років, тому додаткове приймання продуктів, що містять карнітин,сприяє росту дитячого організму, а у випадку затримки росту є необхідним для нормального розвитку дитини.
· Вживання карнітинудозволяє досягти активного довголіття.
Оротова кислота(В13)
Синоніми:Вітамін В13,ороцид. Оротова кислотавперше виділена із сироватки коров'ячого молока (від грец. «оrоs» – сироватка), пізніше вона була знайдена в молоці інших тварин, у тому числі жіночому.
Хімічна структура та властивості
· Оротова кислота– це безколірні кристали без запаху, погано розчинні у воді та органічних розчинниках.
·  За хімічною структурою – гетероцик-лічна сполука, відома як піримідин-карбоксильна кислота, або 4-карбок-сіурацил, 2,6-ді-оксипіримідин-4-кар-бонова кислота.
За хімічною структурою – гетероцик-лічна сполука, відома як піримідин-карбоксильна кислота, або 4-карбок-сіурацил, 2,6-ді-оксипіримідин-4-кар-бонова кислота.
· Під впливом води і світла руйнується.
Біосинтез та метаболізм
· У їжі оротова кислотаміститься у вигляді слаборозчинних у воді солей магнію, калію, кальцію.
· Ці органічні солі всмоктуються у порожнині тонкої кишки шляхом простої дифузії. Абсорбція у ШКТ становить близько 10 %.
· У крові відбувається вивільнення оротової кислоти з мінеральних солей. З крові вільна оротова кислота надходить у печінку та інші органи і тканини.
· Вітамін В13метаболізує у печінці з утворенням оротидин-5-фосфату.
· Оротова кислотасинтезується переважно у печінці в процесі утворення піримідинових нуклеотидів.
· З організму оротова кислотаекскретується з сечею, близько 30 % у вигляді метаболітів. Добова екскреція становить не більше 1,5 мг.
· Вітамін В13також екскретується з грудним молоком.
Поширення у природі та добова потреба
Оротова кислотанаявна у тканинах тварин, рослин, мікроорганізмів.
Джерела:
· продукти тваринного походження: головним джерелом оротової кислоти для людини є коров′яче молоко та молочні продукти. Найбільша кількість її у козячому та овечому молоці, печінці, дріжджах.
· Вітамн може синтезуватися мікроорганізмами кишечнику.
Добова потреба у вітаміні В13 становить 0,5–1,5 г/добу. Рекомендоване добове споживання:
· дорослі: 0,5 – 2,0 г;
· жінки в період лактації: до 3,0 г;
· вагітні до 3,0 г;
· новонароджені: 0,25 – 0,5 г;
· діти: 0,5 – 1,5 г.
При деяких захворюваннях добові дози можуть бути збільшені, тому що вітамін В13 практично нетоксичний.
При неповноцінному білковому харчуванні, порушенні синтезу вітаміну В13, захворюваннях шлунка, печінки, підвище-них фізичних навантаженнях, відновленні після хвороби добова потреба зростає.
Біологічна роль
Оротова кислотає попередником у біосинтезі піримідинових нуклеотидів – уридинмонофосфату та цитидинмонофосфату, які входять до складу нуклеїнових кислот. Вітамін В13має такі біохімічні та фізіологічні функції:
· стимулює білковий обмін, бере участь у синтезі метіоніну, має анаболічний ефект;
· необхідний для нормального росту, відновлення ушкод-жених тканин, процесів регенерації;
· впливає на функціональний стан печінки, прискорює регене-рацію її клітин, знижує ризик розвитку жирового гепатозу;
· має антиатеросклеротичний вплив – сприяє зниженню рівня холестеролу крові за рахунок підтримання його колоїдного стану, тобто запобігає відкладенню холестеролу в артеріях;
· покращує скорочення міокарда;
· сприяє репродуктивній функції, сприятливо впливає на розвиток плода при вагітності, активує процеси росту;
· бере участь у перетвореннях фолієвої кислоти, вітаміну В12, пантотенової кислоти, які необхідні для кровотворення;
· підвищує скоротливу функцію м'язів, зокрема міокарда;
· створює резерви м'язового карнозину.
Прояви вітамінної недостатності
Оротова кислотазазвичай синтезується у достатній кількості в організмі людини, тому випадків гіповітамінозу у літературі до цього часу описано не було, але малобілкова дієта може приз-вести до порушення балансу вітаміну в організмі.
В окремих випадках при серйозних ушкодженнях або у підлітковому віці призначають приймання препаратів оротової кислоти через підвищення потреби в ній.
Недостатність вітаміну В13 призводить до розвитку захворю-вань шкіри – псоріазу, іхтіозу, екземи, нейродерміту.
Застосування оротової кислоти
Оротову кислоту використовують для стимулювання анабо-лічних процесів, прискорення регенерації тканин – у комплекс-ній терапії та профілактиці дистрофії у дітей, атеросклерозу, гіперліпідемії, захворювань печінки, жовчовивідних шляхів, серця, судин, м'язів, у період реконвалесценції, при лікуванні захворювань шкіри.
Анаболічну діюоротової кислоти використовують не тільки у клінічній, але й у спортивній медицині. Вона ефективно конкурує зі стероїдними анаболічними гормонами, значно підвищує працездатність спортсменів та їх результативність.
Оротову кислоту часто призначають для поліпшення переносимості лікарських препаратів: антибіотиків, сульфаніл-амідів, стероїдних гормонів.
6. Макро- та мікроелементи
Для нормального росту та розвитку, крім вітамінів, організму потрібні мінеральні речовини. У нашому організмі знаходиться близько 29 різних мінеральних елементів. Органічні речовини: вуглеводи, білки, ліпіди становлять 90 % сухої речовини і містять в основному вуглець (С), водень (Н), кисень (О), азот (N).
Усі мінеральні елементи нашого організму можна розділити на п′ять груп:
· компоненти макромолекул ( вуглеводів, білків, ліпідів та ін.) - С, Н, О, N;
· основні елементи – макроелементи. Добова потреба в них становить більше 100 мг/добу. Нестача цих елементів у організмі призводить до фатальних наслідків. До цієї групи відносять Na, K, Cl, Ca, P, Mg, S;
· мікроелементи, або незамінні елементи. Добова потреба в них не перевищує декількох міліграмів і навіть мікрограмів на добу. Дефіцит цих елементів призводить до серйозних метаболічних порушень. Група містить Cr, Co, Cu, I, Fe, Mn, Mo, Se, Zn;
· додаткові мікроелементи, які також можливо незамінні, їх роль точно не встановлена. До цієї групи відносять Cd, Ni, Si, Sn, Vn;
· елементи, які не є незамінними для метаболізмуі навіть можуть бути токсичними. Вони не виконують ніяких функ-цій, але надходять в організм із забрудненим повітрям, во-дою, їжею. Представниками цієї групи є As, CN-, Hg та ін.
Натрій(Na)
Натрій– основний електроліт позаклітинної рідини. В орга-нізмі він зазвичай зв’язаний із хлоридами у вигляді NaCl та гідрокарбонатами – NaНСО3.
Поширення у природі та добова потреба
Натрійшироко розповсюджений у природних продуктах, у більшій мірі в їжі тваринного походження, ніж у рослинах. Основним джерелом натрію у нашому раціоні залишається кухонна сіль, яка повністю забезпечує потреби організму в цьому мінералі. Зазвичай доросла людина вживає від 5 до 15 г натрію за добу. У раціоні людей, що проживають у розвинених країнах, вміст натрію зазвичай підвищений.
Джерела:
· продукти тваринного походження: сир, вершкове масло, м'ясо краба, яловичина, мозок, нирки, шинка, солонина;
· продукти рослинного походження: морква, буряк, приправи.
Добова потреба у натрії становить:
· дорослі: 1,0 – 3,5 г;
· новонароджені: 0,1 – 0,5 г;
· діти: 0,3 – 2,5 г.
Додаткове надходження Na необхідне після інтенсивних фізичних тренувань, під час важкої фізичної праці, при високій зовнішній температурі, роботі в гарячих цехах, значному потовиділенні, заняттях спортом у жаркі дні, блюванні, проносах, а також при вживанні рослинної їжі, багатої калієм.
Метаболізм
Всмоктування натрію відбувається у кишечнику шляхом активного транспорту за участю Na+-К+- АТФ-ази. Натрійтакож реабсорбується у нирах за аналогічним механізмом. Іони Na+дифундують у клітини з просвіту кішківника, його активний транспорт спряжений із перенесенням глюкози та амінокислот.
Нормальна концентрація Na+ у плазмі крові – 135 – 145 ммоль/л.
Поширення у тканинах. Загальний вміст натрію в організмі людини становить 3150 ммоль. Основна кількість йогозосереджена у позаклітинній рідині – 2900 ммоль, у внутрішньоклітинній – 250 ммоль.
Екскреція. В основному натрій виводиться з сечею. Близько 25000 ммоль його фільтрується у нирках упродовж доби, але завдяки канальцевій реабсорбції екскретується менше 1 %, тобто 100–200 ммоль/добу. Близько 70 % Na+ реабсорбується у проксимальній частині ниркових канальців, 20–30 % – у висхідній частині петлі Генле. Крім того, натрій виділяється з організму з фекаліями (2–5 г) та потом (5 г).
Біологічна роль Na+
· Підтримання балансу рідини в організмі. Метаболізм натрію тісно пов’язаний із обміном води. Натрійпідтримує осмотичний тиск позаклітинної рідини та сприяє збережен-ню води в організмі.
· Na+ поряд з іншими катіонами бере участь у нервово-м'язовому збудженні.
· Підтримання кислотно-лужного балансу. Натрій– компо-нент буферних систем крові. Іони Na+ обмінюються на Н+ у канальцях нирок, останній екскретується з сечею, підкислюючи її.
· Регулювання в'язкості крові. Солі натрію з білками крові водорозчинні. Натрійразом із калієм підтримують ступінь гідратації протеїнів крові.
· Утворення потенціалу спокою та потенціалу дії.
Причини та ознаки гіпер- та гіпонатріємії
Частіше спостерігається гіпер-, ніж гіпонатріємія. Підвищен-ня концентрації Na+ у крові – гіпернатріємія, не завжди пов′язана із загальним збільшенням його в організмі. При втраті організмом води відбувається відносне збільшення концентрації натрію у позаклітинній рідині.
Гіпернатрієміявиникає при:
· Дегідратації організму внаслідок надмірної втрати води через піт без адекватного її поповнення.
· Нецукровому діабеті за рахунок зниження секреції антидіуретичного гормону гіпофізом, або зміни чутливісті нирок до дії вазопресину.
· Осмотичному навантаженні у випадку, коли нирки повин-ні екскретувати велику кількість водорозчинних речовин, таких, як глюкоза, сечовина, амінокислоти. Осмотичний ефект цих речовин призводить до виділення з організму великого об'єму води і відносно невеликої кількості натрію.
· Надмірному споживанні натрію з їжею або введення великої кількості NaНСО3 при лікуванні ацидозу.
· Терапії стероїдами. Мінералокортикоїди збільшують кон-центрацію натрію в крові шляхом підвищення його тубулярної реабсорбції. При синдромі Кона, деяких видах пухлин надниркових залоз спостерігається гіперпродукція альдостерону, яка призводить до гіпернатріємії.
Ознаки гіпернатріємії. Підвищене споживання натрію викликає накопичення рідини в організмі, набряки, артеріальну гіпертензію, ішемічну хворобу серця, інфаркт, інсульт.
Гіпонатрієміяможе розвинутися внаслідок:
· Використання діуретиків. Це є основною причиною зниження концентрації Na+ у крові. Дія більшості діуретиків, які сьогодні використовуються у медицині, спрямована на виведення надлишків води з організму, але вони також сприяють виділенню Na+ . Гіпонатріємія спостерігається при серцевій недостатності, хронічних захворюваннях нирок, гіпертензії.
· Інтенсивного потовиділення. Втрата води Na+ та Cl- при потовиділенні та заміщенні їх вживанням води без солей.
· Захворювання нирок. При дисфункції нирок зменшується реабсорбція Na+ у канальцях, збільшується його виділення з сечею.
· Гіпофункції кори надниркових залоз, серцевої недостат-ністі, довготривалої діареї, блювання, великих опіків, обмороження.
Ознаки недостатності натрію: спазми м'язів живота, відсутність апетиту (анорексія), нудота, блювання, втрата орієнтації, порушення координації рухів, зневоднення, депре-сія, запаморочення, стомлюваність, галюцинації, головний біль, прискорене серцебиття, знижений поріг смакових відчут-тів, сонливість, знижений артеріальний тиск, ослаблення пам'яті, м'язова слабість, повторювані інфекції, втрата ваги.
Калій (К)
На відміну від натрію калій– основний внутрішньоклітин-ний іон, натрій навпаки – основний позаклітинний іон. Взаємодія цих іонів підтримує ізотонічність клітин.
Поширення у природі та добова потреба
Калій поширений у рослинних продуктах. При нормальному харчовому раціоні добова потреба у калії повністю задоволь-няється за рахунок їжі. Існують сезонні коливання надходження К+ – весною близько 3 г/добу, восени – 5–6 г/добу.
Джерела:
· продукти рослинного походження: цитрусові, листові овочі, листя м′яти, буряк, кабачки, гарбуз, помідори, банани, кура-га, чорнослив, смородина, виноград, сливи, груші, бобові, насіння соняшнику, томатний, яблучний, апельсиновий соки, печена картопля, порошок какао;
· продукти тваринного походження: риба, яловичина, телятина.
Добова потреба у калії не встановлена. Рекомендована доза для дорослої людини становить 2,0 – 3,0 г/добу, для дитини – 16–30 мг/кг маси тіла. Мінімальна кількість К+, яка має бути присутня у їжі, 1г.
Для нормального метаболізму співвідношення між К+ та Na+ у добовому раціоні повинно бути – 1:2. У зв'язку з тим, що у сучасному світі відмічено тенденцію до збільшення вживання солі, зростає потреба у калії, який може нейтралізувати згубний вплив натрію на організм людини.
Додаткове споживання калію рекомендується при недостат-ності серцевого м'яза, порушеннях ритму серця, затримці рідини в організмі, гіпертонічній хворобі.
Метаболізм
Всмоктування. Калій легко всмоктується у кишечнику та надходить у клітини.
Нормальна концентрація К+ у сироватці крові дорівнює 3,4 – 5,3 ммоль/л. Зазвичай вона відображає загальний вміст калію в організмі людини. При порушеннях кислотно-лужної рівноваги, кахексії, підвищенні проникності клітинних мембран та ін. рівень калію у крові не відображає його загальної кількості в організмі.
Поширення у тканинах. Калій значно поширений у рідинах та тканинах організму, близько 98 % його зосереджено всере-дині клітин. Середній вміст калію в організмі дорівнює 3,6 моль, але ця кількість залежить від маси клітин і може змінюватися залежно від віку, статі, конституції людини. У цільній крові кон-центрація калію становить 200 мг/дл, у плазмі – 20 мг/дл, у клі-тинах – 440/100 г, у м'язах – 250-400 мг/100 г, у нервовій тканині – 530 мг/100 г.
Внутрішньоклітинний вміст К+ еквівалентний позаклітинній концентрації Na+. Ця концентраційна рівновага підтримується роботою натрієвого насоса - Na+-К+ -АТФ-ази.
Розподіл калію в тканинах організму регулюється альдо-стероном, секрецією інсулінута тонусом симпатичної нервової системи.
Екскреція. Калій екскретується з організму з сечею. Виді-лення його залежить від споживання натрію. Чим більше Na+ надходить з їжею, тим більше К+ виводиться. Калій безперервно фільтрується у клубочках нирок, реабсорбується клітинами зви-тих проксимальних канальців та петлі Генле, секретуюється у дистальних канальцях в обмін на натрій.
Калій екскретується через ШКТ, виділяється у складі слини, шлункового соку, жовчі, підшлункового та кишкового соку. За добу виділяється стільки калію, скільки його надходить у екстрацелюлярну рідину.
Біологічна роль
Функції калію в організмі скоординовані з функціями натрію і полягають у такому:
· необхідний для м′язового скорочення;
· бере участь у підтриманні кислотно-лужного балансу;
· важливий для підтримання нормального функціонування серцевого м'яза, регуляції ритму серця;
· є кофакторомдеяких ензимів (піруваткіназа);
· бере участь у нервово-м'язовому збудженні та проведенні нервових імпульсів.
Причини та ознаки гіпер- та гіпокаліємії
У нормі механізм виведення калію з організму настільки ефективний, що отримати гіперкаліємію шляхом надмірного споживання практично неможливо. Гіперкалієміязустрічається рідше, ніж гіпокаліємія, але є дуже небезпечною для організму.
Гіперкалієміявиникає при:
· Внутрішньовенному введенні надмірної кількості солей калію.
· Нирковій недостатності зі зниженням екскреції калію з сечею.
· Швидкому вивільненні калію з внутрішньоклітинної рідини, яке спостерігається при різних захворюваннях. Іноді такий стан супроводжується нирковою недостатністю.
· Анурії – повному припиненні функцій нирок.
· Синдромі роздавлювання та масивному гемолізі, які призво-дять до вивільнення К+ з тканин.
· Інтенсивному м'язовому скороченні, яке супроводжується виходом калію з клітин і швидким підвищенням вмісту його у крові, наприклад, гіперкаліємія при епілепсії.
· Хворобі Аддісона, яка характеризується гіпонатріємією та гіперкаліємією. Через зниження секреції альдостеронунад-нирковими залозами збільшується виведення натрію і калійзатримується в організмі.
· Цукровому діабеті. Кетоацидоз, який може розвинутися, призводить до виснаження внутрішньоклітинних депо калію, гіперкалієміїчерез активацію Na+-К+ АТФ-ази, зниження вмісту інсулінута гіпертонічність позаклітинної рідини.
Ознаки гіперкаліємії. Підвищення концентрації калію в ор-ганізмі призводить до зниження збудливості і провідності серце-вого м'яза, фізичного та розумового збудження, паралічу кінцівок.
Гіпокалієміярозвивається принедостатності К+ у їжі чи надмірному виведенні його нирками та через ШКТ. Причини гіпокаліємії:
· Втрата К+ через шлунково-кишковий тракт під час дов-готривалої діареї чи блювання, при зловживанні проносними засобами, за наявності К+-секретуючих пухлин кишечнику.
· Втрата К+ з сечею спостерігається при:
o первинному та вторинному гіперальдостеронізмі;
o у хворих із застійною серцевою недостатністю;
o використанні тіазидних діуретиків;
o синдромі Кушинга– гіперпродукції стероїдних гормонів корою надниркових залоз;
o ектопічній секреції АКТГ;
o вживанні алкогольних напоїв, кави, цукру. Зазвичай у людей, які зловживають солодощами та вживанням кави, спостерігається гіпокаліємія, яка може призвес-ти до проблем із серцевим ритмом.
· Перехід екстрацелюлярного калію всередину клітин, яке спостерігається при парентеральному харчуванні, гострому алкалозі, введенні інсулінупри лікуванні цукрового діабету.
· Інші причини гіпокаліємії:
o лікування кетоацидозу при цукровому діабеті;
o гіпомагніємія;
o нирковий канальцевий ацидоз, синдром Фанконі;
o лікування стероїдними гормонами - тестостероном, кортизоном, диоксикортикостероном;
o псевдогіперальдостеронізм – отруєння лакрицею;
o гіпоглікемія, емоційний, фізичний стрес;
o голодування, низьковуглеводна дієта, муковісцидоз;
o надмірна втрата К+ з потом без його заміщення.
Ознаки недостатності калію: загальна слабкість, сухість шкіри, безсоння та сонливість, депресія, апатія, м'язова слаб-кість, тремор кінцівок, артеріальна гіпотонія, порушення сер-цевого ритму, непрохідність та атонія кишечника, нудота, блювання, затримка води в організмі, набряки, анурія, нефро-патія з порушенням концентраційної функції нирок.
Кальцій(Са)
Кальційосновний мінеральний компонент кісток і зубів, в яких він знаходиться у вигляді кристалів гідроксиапатитуі є мінеральною основою скелету.
Поширення у природі та добова потреба
Кальційшироко розповсюджений у харчових продуктах, але доступність його неоднакова. Кальцій з молочних продуктів зас-воюється лише на 30 %, а з рослинної їжі – на 50%.
Джерела:
· продукти тваринного походження: молоко, сир, молочні проти, жовток яйця, сардини, лосось;
· продукти рослинного походження: насіння кунжуту, квасоля, чечевиця, горіхи, арахіс, насіння соняшника, інжир, зелені овочі, капуста.
Одним із джерел є питна вода, яка вміщує від 350–500 г/л Са, залежно від жорсткості.
Добова потреба у кальції для дорослої людини становить близько 1 г/добу і залежить від віку та стану організму.
Рекомендована норма споживання кальцію:
· дорослі 19-70 років: 1,0–1,3 г;
· новонароджені: 0,400 г;
· діти 6 міс. – 1 року: 0,600 г;
· діти 1–3 років: 0,700 г;
· діти 4–8 років: 1,000 г;
· підлітки: 1,300 г;
· жінки у період вагітності та лактації 1,0–1,3 г.
Додаткове надходження Сa необхідне у період вагітності та лактації, інтенсивного росту. Потреба підвищується у жінок у клімактеричному періоді, при травмах та переломах кісток.
Метаболізм
Всмоктування. Кальційнадходить з їжею головним чином у формі фосфатів, карбонатів, тартратів. На відміну від натрію та калію, які легко абсорбуються у кишечнику, кальцій погано всмоктується. Близько 40 % Са++ їжі всмоктується у 12-палій кишці та верхніх відділах кишечнику проти електро- та концент-раційного градієнтів.
Розрізняють два механізми абсорбції кальцію у кишечнику:
- проста дифузія;
- активний транспорт за участі енергозалежного Са++ насоса.
Обидва процеси залежать від кальцитріолу– 1,25-(ОН)2-D3, який регулює синтез Са-зв′язувальних протеїнів, Са++–залежної АТФ-ази і транспорт кальцію.
Фактори, які впливають на абсорбцію Са у кишечнику:
1. рН середовища. У кислому середовищі Са++ краще засво-юється, оскільки його фосфати та карбонати добре розчинні у кислих розчинах. У лужному середовищі всмоктування знижується через утворення нерозчинного Са3(РО4)2.
2. Склад їжі. Продукти харчування містять речовини, які сприяють або перешкоджають абсорбції кальцію.
- Багата білками дієта сприяє засвоєнню кальцію з їжі, оскільки амінокислоти, особливо Ліз і Арг, підвищують розчинність солей Са. Низькобілкова дієта знижує зас-воєння Са з 15 % до 5 %.
- Жирні кислоти знижують засвоєння Са++. Вони утворю-ють нерозчинні кальцієві мила, які виділяються з калом.
- Цукри та органічні кислоти. Органічні кислоти, які утворюються з цукрів мікрофлорою кишечнику, підви-щують розчинність кальцієвих солей і сприяють його засвоєнню.
- Фітинова кислота(інозитол-6-фосфат),яка міститься у злаках, погіршує всмоктування Са.
- Оксалати,що є в овочах (капусті, салаті, шпинаті) утво-рюють нерозчинні оксалати кальцію, останні виводяться з фекаліями, засвоєння кальцію з їжі погіршується.
- Волокна.Наявність у їжі надмірної кількості волокон перешкоджає засвоєнню кальцію.
- Мінеральні речовини.Наявність у дієті значної кількос-ті магнію і фосфатів погіршує засвоєння Са. Оптимальне співвідношення Са:Р повино бути 1:1, зміна цієї рівнова-ги призводить до зниження доступності кальцію з їжі. Наявність залізау дієті, навпаки, покращує всмоктування кальцію. Fe3+ зв′язує фосфат у нерозчинну сіль Fe3РО4, тим самим збільшуючи співвідношення Са:Р до опти-мального.
- Вітамін D сприяє засвоєнню Са.
3. Стан здоров′я і вік людини.У здорових людей абсорбуєть-ся близько 40 % Са, який надходить з їжею. Після 60-ти років здатність до його засвоєння поступово знижується. При захворюваннях ШКТ – мальабсорбції, спру – надход-ження Са з кишечнику зменшується.
Дата добавления: 2015-04-01; просмотров: 1465;
