Билет №17.
Средние соли, их состав, названия, химические свойства (взаимодействие с металлами, кислотами, щелочами, друг с другом с учетом особенностей реакций окисления-восстановления и ионного обмена).
Соли — электролиты, в растворах которых есть катионы металлов или ион аммония и анионы кислотных остатков.
Названия: название аниона + название катиона в родительном падеже + степень окисления металла.
1.B водных растворах соли могут реагировать со щелочами. Так, хлористый магний MgCl2 взаимодействует с едким натром, образуя новую соль и новое основание:
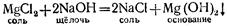
2. Соли могут реагировать с кислотами. Так, раствор азотнокислого бария Ва(гЮз)а взаимодействует с раствором серной кислоты, образуя новую кислоту и новую соль:
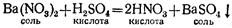
З.В водных растворах соли могут реагировать между собой.
Если слить вместе водные растворы хлористого кальция CaCl2 я углекислого натрия Na2CO3 TO тотчас же образуется белый осадок нерастворимого в воде углекислого кальция СаСО3, а в растворе — хлористый натрий:
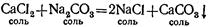
4. В водных растворах солей металл, входящий в их состав, может замещаться другим металлом, стоящим до него в ряду активности.
Если в раствор сернокислой меди опустить чистую железную проволоку или кусочек цинка, то на их поверхности выделяется медь, а в растворе образуется сернокислое железо (если было опущено железо) или сернокислый цинк (если был опущен цинк):
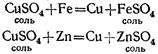
Но из сернокислого цинка нельзя вытеснить цинк медью: медь в ряду активности стоит после цинка.
Дата добавления: 2015-04-05; просмотров: 1375;
