Общие способы получения металлов.
Металлы находятся в природе преимущественно в виде соединений. Только металлы с малой химической активностью (благородные металлы) встречаются в природе в свободном состоянии (платиновые металлы, золото, медь, серебро, ртуть). Из конструкционных металлов в достаточном количестве имеются в природе в виде соединений лишь железо, алюминий, магний. Они образуют мощные залежи месторождений относительно богатых руд. Это облегчает их добычу в больших масштабах.
Поскольку металлы в соединениях находятся в окисленном состоянии (имеют положительную степень окисления), то получение их в свободном состоянии сводится к процессу восстановления:

Этот процесс можно осуществить химическим или электрохимическим путем.
При химическом восстановлении в качестве восстановителя чаще всего применяют уголь или оксид углерода (II), а также водород, активные металлы, кремний. С помощью оксида углерода (II) получают железо (в доменном процессе), многие цветные металлы (олово, свинец, цинк и др.):
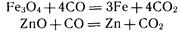
Восстановление водородом используется, например, для получения вольфрама из оксида вольфрама (VI):
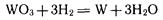
Применение в качестве восстановителя водорода обеспечивает наибольшую чистоту получаемого металла. Водород используют для получения очень чистого железа, меди, никеля и других металлов.
Способ получения металлов, в котором в качестве восстановителя применяют металлы, называют металлотермическим. В этом способе в качестве восстановителя используют активные металлы. Примеры металлотермических реакций:
алюминотермия:
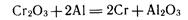
магниетермия:
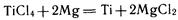
Металлотермические опыты получения металлов впервые осуществил русский ученый Н. Н. Бекетов в XIX в.
Металлы наиболее часто получают восстановлением их оксидов, которые в свою очередь выделяют из соответствующей природной руды. Если исходной рудой являются сульфидные минералы, то последние подвергают окислительному обжигу например:
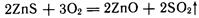
Электрохимическое получение металлов осуществляется при электролизе расплавов соответствующих соединений. Таким путем получают наиболее активные металлы, щелочные и щелочноземельные металлы, алюминий, магний.
Электрохимическое восстановление применяют также для рафинирования (очистки) «сырых» металлов (меди, никеля, цинка и др.), полученных другими способами. При электролитическом рафинировании в качестве анода используют «черновой» (с примесями) металл, в качестве электролита — раствор соединений данного металла.
Способы получения металлов, осуществляемые при высоких температурах, называют пирометаллургическими (по-гречески pyr — огонь). Многие из этих способов известны с древних времен. На рубеже XIX—XX вв. начинают развиваться гидрометаллургические способы получения металлов (по-гречески hydor—вода). При этих способах компоненты руды переводят в водный раствор и далее выделяют металл электролитическим или химическим восстановлением. Так получают, например, медь. Медную руду, содержащую оксид меди (II) CuО, обрабатывают разбавленной серной кислотой:
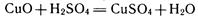
Для восстановления меди полученный раствор сульфата меди (II) либо подвергают электролизу, либо действуют на раствор порошком железа.
Гидрометаллургический способ имеет большое будущее, так как позволяет получать продукт, не извлекая руду из земли. (Сравните достоинства гидрометаллургического способа получения металлов с подземной газификацией угля.)
Дата добавления: 2015-04-05; просмотров: 1493;
