Периодический закон и периодическая система химических элементов Д. И. Менделеева на основе представлений о строении атомов. Значение периодического закона для развития науки.
В 1869 г. Д. И. Менделеев на основе анализа свойств простых веществ и соединений сформулировал Периодический закон:
Свойства простых тел... и соединений элементов находятся в периодической зависимости от величины атомных масс элементов.
На основе периодического закона была составлена периодическая система элементов. В ней элементы со сходными свойствами оказались объединены в вертикальные столбцы — группы. В некоторых случаях при размещении элементов в Периодической системе приходилось нарушать последовательность возрастания атомных масс, чтобы соблюдалась периодичность повторения свойств. Например, пришлось "поменять местами" теллур и йод, а также аргон и калий.
Причина состоит в том, что Менделеев предложил периодической закон в то время, когда не было ничего известно о строении атома.
После того, как в XX веке была предложена планетарная модель атома, периодический закон формулируется следующим образом:
Свойства химических элементов и соединений находятся в периодической зависимости от зарядов атомных ядер.
Заряд ядра равен номеру элемента в периодической системе и числу электронов в электронной оболочке атома.
Эта формулировка объяснила "нарушения" Периодического закона.
В Периодической системе номер периода равен числу электронных уровней в атоме, номер группы для элементов главных подгрупп равен числу электронов на внешнем уровне.
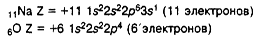
Причиной периодического изменения свойств химических элементов является периодическое заполнение электронных оболочек. После заполнения очередной оболочки начинается новый период. Периодическое изменение элементов ярко видно на изменении состава и свойств и свойств оксидов.
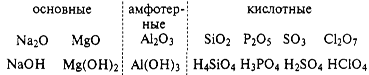
Научное значение периодического закона. Периодический закон позволил систематизировать свойства химических элементов и их соединений. При составлении периодической системы Менделеев предсказал существование многих еще не открытых элементов, оставив для них свободные ячейки, и предсказал многие свойства неоткрытых элементов, что облегчило их открытие.
Строение атомов химических элементов на примере элементов второго периода и IV-A группы периодической системы химических элементов Д. И. Менделеева. Закономерности в изменении свойств этих химических элементов и образованных ими простых и сложных веществ (оксидов, гидроксидов) в зависимости от строения их атомов.
При перемещении слева направо вдоль периода металлические свойства элементов становятся все менее ярко выраженными. При перемещении сверху вниз в пределах одной группы элементы, наоборот, обнаруживают все более ярко выраженные металлические свойства. Элементы, расположенные в средней части коротких периодов (2-й и 3-й периоды), как правило, имеют каркасную ковалентнуто структуру, а элементы из правой части этих периодов существуют в виде простых ковалентных молекул.

Атомные радиусы изменяются следующим образом: уменьшаются при перемещении слева направо вдоль периода; увеличиваются при перемещении сверху вниз вдоль группы. При перемещении слева направо по периоду возрастает электроотрицательность, энергия ионизации и сродство к электрону, которые достигают максимума у галогенов. У благородных же газов электроотрицательность равна 0. Изменение сродства к электрону элементов при перемещении сверху вниз вдоль группы не столь характерны, но при этом уменьшается электроотрицательность элементов.
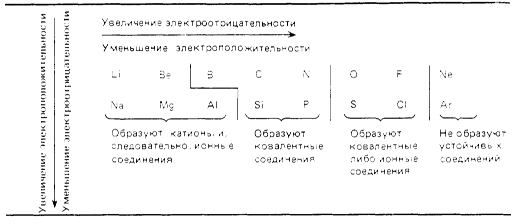
В элементах второго периода заполняются 2s, а затем 2р-орбитали.
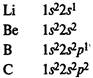
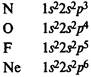
Главная подгруппа IV группы периодической системы химических элементов Д. М. Менделеева содержит углерод С, кремний Si, германий Ge, олово Sn и свинец Pb. Внешний электронный слой этих элементов содержит 4 электрона (конфигурация s2p2). Поэтому элементы подгруппы углерода должны иметь некоторые черты сходства. В частности, их высшая степень окисления одинакова и равна +4.
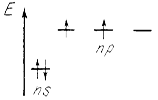
А чем обусловлено различие в свойствах элементов подгруппы? Различием энергии ионизации и радиуса их атомов. С увеличением атомного номера свойства элементов закономерно изменяются. Так, углерод и кремний — типичные неметаллы, олово и свинец — металлы. Это проявляется прежде всего в том, что углерод образует простое вещество-неметалл (алмаз), а свинец типичный металл.
Германий занимает промежуточное положение. Согласно строению электронной оболочки атома p-элементы IV группы имеют четные степени окисления: +4, +2, – 4. Формула простейших водородных соединений — ЭН4, причем связи Э—Н ковалентны и равноценны вследствие гибридизации s- и р- орбиталей с образованием направленных под тетраэдрическими углами sp3 -орбиталей.
Ослабление признаков неметаллического элемента означает, что в подгруппе (С—Si—Ge—Sn—Pb) высшая положительная степень окисления +4 становится все менее характерной, а более типичной становится степень окисления +2. Так, если для углерода наиболее устойчивы соединения, в которых он имеет степень окисления +4, то для свинца устойчивы соединения, в которых он проявляет степень окисления +2.
А что можно сказать об устойчивости соединений элементов в отрицательной степени окисления —4? По сравнению с неметаллическими элементами VII—V групп признаки неметаллического элемента р-элементы IV группы проявляют в меньшей степени. Поэтому для элементов подгруппы углерода отрицательная степень окисления нетипична.
Виды химической связи и способы ее образования в неорганических соединениях: ковалентная (полярная, неполярная, простые и кратные связи), ионная, водородная.
Ковалентная связь образуется за счет перекрывания электронных облаков двух атомов. Каждый атом предоставляет один неспаренный электрон для образования одной химической связи, при этом происходит образование общей электронной пары. Если ковалентная связь образуется между двумя одинаковыми атомами, она называется неполярной.
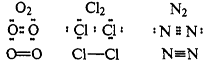
Если ковалентная связь образуется между двумя различными атомами, общая электронная пара смещайся к атому с большей электроотрицательностью (электроотрицательностью называется способность атома притягивать электроны). В этом случае возникает полярная ковалентная связь.
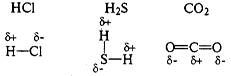
Частным случаем ковалентной связи является донорно-акцепторная связь. Для ее образованья у одного атома должна быть свободная орбиталь на внешнем электронном уровне, а у другого — пара электронов. Один атом (донор) предоставляет другому (акцептору) свою электронную пару, в результате она становится общей, образуется химическая связь. Пример — молекула СО:
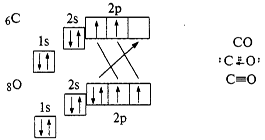
Ионная связь образуется между атомами с сильно отличающейся электроотрицательностью. При этом один атом отдает электроны и превращается в положительно заряженный ион, а атом, получивший электроны, в отрицательно заряженный. Ионы удерживаются вместе за счет сил электростатического притяжения.
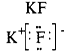
Водородная связь образуется между полярными молекулами (вода, спирты, аммиак) за счет притяжения разноименных зарядов.
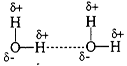
Прочность водородной связи существенно (~20 раз) меньше, чем ионной или ковалентной связи.
Дата добавления: 2015-04-05; просмотров: 3089;
