Электропроводность растворов.
Под прохождением электрического тока через вещество понимают движение (перенос) электрических зарядов от одного полюса к другому под действием внешнего электрического поля. Способность вещества проводить электрический ток называется электропроводностью.
Различают две основные формы проводимости: электронную и ионную. Электронной проводимостью обладают, например, металлы в твердом и расплавленном состоянии. Электрический ток по этим проводникам передается потоком электронов аналогично потоку газов в трубе в направлении от катода цепи к аноду.
В растворах электролитов перенос электричества осуществляется за счет перемещения ионов. Анионы в электрическом поле движутся к положительно заряженному электроду — аноду, катионы—к отрицательному электроду — катоду. Скорость движения ионов в растворах по сравнению со скоростями движения электронов в металлах мала, поэтому электропроводность, например, меди и серебра примерно в 1 000 000 раз больше электропроводности растворов.
Проводник, по которому течет электрический ток, представляет для него определенное сопротивление. За единицу сопротивления, как известно, принят ом,который представляет собой сопротивление столба ртути длиной 106,3 см и площадью сечения 1 мм2 при 0°С.
Согласно закону Ома сопротивление R прямо пропорционально длине проводника l, обратно пропорционально площади сечения S и зависит от материала: 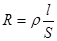
В этом уравнении r (греч. «ро») — удельное сопротивление, т.е. сопротивление проводника, имеющего длину 1 см и сечение в 1 см2 (при t = const), которое зависит исключительно от качества материала.
Значения удельных сопротивлений приведены в таблицах для одной и той же температуры, поскольку сопротивление проводников зависит от температуры. Эта зависимость для металлов и электролитов противоположна: если сопротивление металлов с повышением температуры увеличивается, то сопротивление растворов электролитов, наоборот, уменьшается (примерно на 1 – 2,5% на каждый градус).
Когда речь идет о растворах электролитов, обычно говорят не о сопротивлении растворов, а об их электропроводности. Мерой электропроводности является количество электричества, выраженное в кулонах, которое за единицу времени проходит через электролит. Таким образом, для растворов электролитов справедливо следующее соотношение:
I=LE
где I — сила тока, Е — электродвижущая сила (э дс), в; L, — электропроводность электролита. В том случае, когда Е =1, I = LL, как и I, есть сила тока, измеряемая в амперах. Из курса физики известно, что 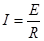
где R — сопротивление.
Объединив два последних уравнения, получим:
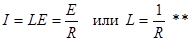
Таким образом, электропроводность раствора можно характеризовать как величину, обратную его сопротивлению. Подставив в уравнение (**) значение R из закона Ома, будем иметь:
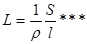
Дата добавления: 2015-05-13; просмотров: 1589;
