ФЛУОРЕСЦЕИН
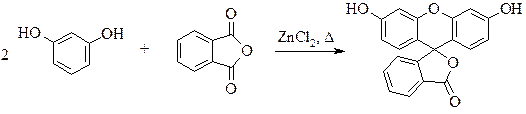
Работу проводят в вытяжном шкафу!
В фарфоровой ступке тщательно растирают 1,5 г фталевого ангидрида с 2,2 г резорцина. Смесь помещают в металлический или фарфоровый тигель и нагревают на песчаной бане до 180 °С. Предпочтительно следует использовать металлический (никелевый) тигель, так как фарфоровый тигель легко может быть разбит при извлечении застывающего в плотную массу расплава. В расплавленную массу в течение 10 минут при помешивании вносят небольшими порциями 1 г безводного хлорида цинка (получение – см. приложение 2), температуру повышают до 210 °С и нагревают 1‑2 часа до тех пор, пока густая масса не затвердеет. Охлажденный хрупкий сплав извлекают из тигля, тщательно измельчают и кипятят 10 минут в стакане с 20 мл воды, к которой прибавлен 1 мл соляной кислоты. При этом происходит растворение хлорида и гидроксида цинка. Флуоресцеин отфильтровывают на воронке Бюхнера, промывают водой до исчезновения кислой реакции промывных вод и сушат при 80‑90 °С. Выход около 3,0 г. Т. пл. 312-318 °С (с разложением).
1-(ДИФЕНИЛМЕТИЛ)-4-МЕТИЛБЕНЗОЛ
(п-толилдифенилметан)
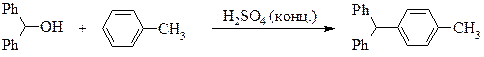
К раствору 1,7 г дифенилметанола[‡‡‡‡‡‡‡‡‡] и 8,5 г толуола в 67,5 мл ледяной уксусной кислоты по каплям при перемешивании и охлаждении добавляют 12,5 мл концентрированной серной кислоты. Реакционную смесь оставляют при комнатной температуре на 8 дней, затем выливают в ледяную воду и нейтрализуют 40 г гидрокарбоната натрия.
Непрореагировавший толуол и уксусную кислоту отгоняют с водяным паром, остаток экстрагируют диэтиловым эфиром (или этилацетатом). Эфирный экстракт сушат хлоридом кальция, эфир отгоняют. Остаток растворяют в толуоле, добавляют 2‑3 г активированного угля и кипятят 5 минут в колбе с обратным холодильником. Горячий раствор фильтруют (работу проводят под тягой!), осадок на фильтре промывают толуолом. Толуол отгоняют, получают 1,4 г сырого продукта, который дважды перекристаллизовывают из толуола. Выход около 1,4 г. Т. пл. 70-70,5 °С.
2-(ДИФЕНИЛМЕТИЛ)-1,4-ДИМЕТИЛБЕНЗОЛ
(2,5-диметилтрифенилметан)
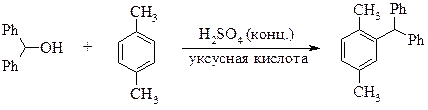
Синтез проводят в трехгорлой колбе объемом 100 мл, снабженной механической мешалкой и капельной воронкой. К раствору 1,7 г дифенилкарбинола[§§§§§§§§§] и 9,5 г п‑ксилола в 67,5 мл ледяной уксусной кислоты по каплям при перемешивании и охлаждении добавляют 12,5 мл конц. серной кислоты. Реакционную смесь оставляют при комнатной температуре на 8 дней, затем выливают в ледяную воду и нейтрализуют 40 г гидрокарбоната натрия.
Непрореагировавший п-ксилол и уксусную кислоту отгоняют с водяным паром, остаток экстрагируют диэтиловым эфиром (или этилацетатом). Эфирный экстракт сушат хлоридом кальция, эфир отгоняют. Остаток растворяют в толуоле, добавляют 2‑3 г активированного угля и кипятят 5 минут в колбе с обратным холодильником. Горячий раствор фильтруют (работу проводят под тягой!), осадок промывают на фильтре толуолом. Растворитель отгоняют, получают 2,3 г сырого продукта, который дважды перекристаллизовывают из толуола. Выход около 1,7 г. Т. пл. 70 °С.
Вопросы для самоподготовки.
1. Какие реагенты для алкилирования ароматических соединений Вы знаете? Какие катализаторы используются в реакциях алкилирования аренов? Приведите примеры реакций.
2. Рассмотрите механизм реакции алкилирования на примере проведенного Вами синтеза.
3. В реакциях алкилирования анизола используют в качестве катализатора металлическое железо. Предложите механизм его действия. Как Вы думаете, всегда ли его можно использовать вместо традиционных катализаторов – кислот Льюиса?
4. Какими побочными процессами осложняются реакции алкилирования аренов? Какие из них возможны в ходе осуществленного Вами синтеза?
5. Как определяют окончание выделения хлороводорода из реакционной смеси?
6. Аналогично синтезу бисфенола (см. методику), из хлораля (трихлоруксусного альдегида) и хлорбензола получают ДДТ, а из бензальдегида и N,N‑диметиланилина – лейкооснование красителя малахитового зеленого. Напишите соответствующие схемы и поясните, почему в первом случае реакцию проводят в присутствии олеума или хлорсульфоновой кислоты, и выход целевого продукта невелик, а во втором случае требуется лишь соляная кислота или хлорид цинка.
7.[**********] Водно-щелочные растворы флуоресцеина имеют желтовато-красный цвет с сильной зеленой флуоресценцией. Что такое флуоресценция и чем обусловлено ее наличие у флуоресцеина?
8.* Флуоресцеин относится к красителям трифенилметанового ряда. Приведите еще примеры красителей трифенилметанового ряда, имеющих широкое практическое применение (например, в качестве рН индикатора).
9.* Сам флуоресцеин труднорастворим в воде. При обработке флуоресцеина содой или водной щелочью образуется хорошо растворимая двунатриевая соль – уранин. Напишите формулу уранина.
Дата добавления: 2015-04-03; просмотров: 2323;
