Методы инвазивных манипуляций
Пункция и катетеризация периферических вен.Наиболее распространенной методикой в клинической практике является пункция или катетеризация поверхностных вен верхней конечности. Однако нередко используют вены и нижней конечности.
Наиболее типично введение лекарственных сред путем венепункции в локтевом сгибе. Несмотря на широкое распространение, этот путь имеет свои недостатки. Возможны подтекание раствора в подкожную клетчатку, инфицирование и тромбоз вены, исключается введение концентрированных растворов, препаратов калия, раздражающих сосудистую стенку и т.д. Поэтому целесообразна смена места пункции через 48 ч или с появлением признаков воспаления. Необходимо избегать сдавления руки ниже пункции (фиксация руки), чтобы не препятствовать току крови по ходу вены, избегать введения гипертонических растворов.
Чрескожная пункция с введением микрокатетеров в вены руки обеспечивает достаточную подвижность конечности и значительно повышает надежность введения лекарственных препаратов. Незначительный диаметр катетеров исключает возможность массивных инфузий, но при его применении сохраняются недостатки пункционного пути.
Венесекция, катетеризация с обнажением вены позволяют вводить катетеры в верхнюю и нижнюю полые вены. При этом имеется опасность инфицирования раны и тромбоза вен на протяжении, ограничен срок пребывания катетеров в сосудах. Катетеризация обладает преимуществами инфузионной терапии в центральные вены.
Специальные методики. Катетеризация пупочной вены и ин-траумбиликальные инфузий облада-
ют свойствами инфузий в центральные вены; при этом используется преимущество внутриорганного введения при патологии печени, отсутствует возможность измерения ЦВД.
Метод катетеризации кровеносных сосудов по Сельдингеру.Катетеризация по Сельдингеру состоит из двух моментов: проведения в иглу мандрена-проводника и проведения катетера в сосуд по проводнику (рис. 23.9). После пункции сосуда шприц отсоединяется от иглы и через иглу в сосуд вводят проводник. Однако введение мандрена-проводника зачастую сопряжено с трудностями, которые зависят от того, что он может упираться в заднюю стенку сосуда из-за перпендикулярного направления иглы. Для устранения этого затруднения необходимо моделировать положение иглы в сосуде до устранения препятствия. Насильственное проведение мандрена-проводника недопустимо, движение его должно быть свободным, без сопротивления. В противном случае упругий проводник может перфорировать стенку сосуда или, свернувшись в клубок у его стенки, не позволит ввести в сосуд катетер. Извлечение свернувшегося проводника может представлять известные сложности. После того как в сосуд введен проводник, игла извлекается и по нему вводится катетер. Катетер вводят, придавая ему поступательно-вращательное движение, в вену на 5—12 см, а в аорту до 40 см. После извлечения проводника необходимо проверить правильность нахождения катетера в сосуде. Для этой цели присоединяют к катетеру шприц и потягивают за поршень: кровь должна свободно поступать в шприц. Далее к катетеру присоединяют систему для переливания (или же после заполнения катетера раствором гепарина его закрывают заглушкой). При присоединении к катетеру системы для переливания жидкости или за-
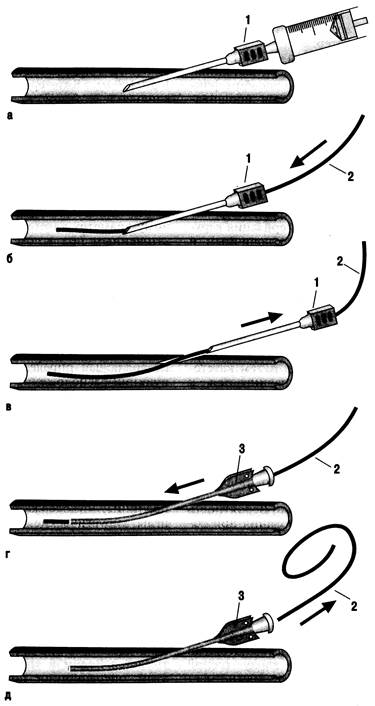
Рис. 23.9. Последовательность манипуляций при введении венозного катетера по методу Сельдингера (а, б, в, г, ц).
1 - игла для пункции вены; 2 — проводник; 3 — катетер.
крытия его заглушкой необходимо помнить о возможности попадания воздуха в катетер.
Фиксация катетера — один из ответственных этапов всей методики. Наиболее надежным способом фиксации катетера является прошива-ние кожи шелковой нитью в 2 см от места пункции, после чего нить завязывают непосредственно на катетере, надев на него муфточку из лейкопластыря. Асептическая наклейка вокруг катетера фиксируется полосками лейкопластыря.
Катетеризация верхней полой вены. Чрескожная катетеризация верхней полой вены подключичным и надключичным доступами из подключичной и внутренней яремной вены обладает несомненными преимуществами для инфузионной терапии. Возможны самое длительное функционирование из всех доступных путей, близость сердца и информация о ЦВД. Введение фармакологических средств путем катетеризации вены приравнивается к внутрисердечным инъекциям. При реанимации обеспечен высокий темп инфузий. Этот путь позволяет осуществить эндокардиальную эле-ктрокардиостимуляцию. Ограничений в применении инфузионных сред нет. Создаются условия для активного поведения больного, облегчается уход за ним. Вероятность тромбоза и инфицирования при соблюдении всех правил асептики и ухода за катетером минимальна.
Чаще всего катетеризация верхней полой вены осуществляется через подключичную или внутреннюю яремную вены. Подключичная вена отличается своим постоянным местонахождением, определяемым четкими топографоанатомическими ориентирами. Вена ввиду тесной связи с мышцами и фасциями имеет постоянный просвет и не спадается даже при выраженной гиповолемии. Значительная скорость кровотока в вене препятствует тромбообразова-нию.
Инструментарий и принадлежности:
1) набор катетеров из пластика одноразового применения длиной 18—20 см с наружным диаметром от 1 до 1,8 мм. Катетер должен иметь канюлю и заглушку;
2) набор проводников из капроновой лески длиной 50 см и толщиной, подобранной соответственно диаметру внутреннего просвета катетера;
3) иглы для пункции подключичной вены длиной 12—15 см с внутренним диаметром, равным наружному диаметру катетера, и острием, заточенным под углом 35°, клиновидной формы и отогнутым к основанию среза иглы на 10—15°. Такая форма иглы позволяет легко и не-травматично прокалывать кожу, связки и вену и защищает просвет иглы от попадания жировой ткани [Журавлев В.А. и др., 1981]. На канюле иглы должна быть насечка, позволяющая определить во время пункции расположение острия иглы и ее среза. Игла должна иметь канюлю для герметичного соединения со шприцем;
4) шприц емкостью 10 мл;
5) иглы инъекционные для подкожных и внутримышечных инъекций;
6) скальпель остроконечный, ножницы, иглодержатель, пинцет, иглы хирургические, шелк, лейкопластырь.
Весь материал и инструментарий должен быть стерильным.
Техника пункции вен. Манипуляцию проводит врач, соблюдая все правила асептики. Врач надевает маску, обрабатывает руки, надевает стерильные перчатки. Кожа в месте пункции широко обрабатывается йодом и спиртом, йодон-атом, операционное поле обкладывается стерильным полотенцем. Положение больного горизонтальное. Под лопатки подкладывается валик высотой 10 см, голова должна быть повернута в сторону, противопо-
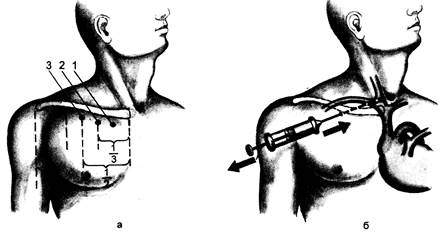
Рис. 23.10.Пункция подключичной вены.
а - пунктиром обозначены анатомические ориентиры места пункции, точки: 1 — Giles, 2 — Aubaniac, 3 — Wilson; б — направление иглы.
ложную пункции. Ножной конец стола приподнимают под углом 15— 20° для предотвращения воздушной эмболии в случае отрицательного венозного давления. Чаще всего применяют местную анестезию раствором новокаина. У детей процедуру выполняют под общей анестезией — масочным наркозом фторо-таном.
Катетеризация верхней полой вены состоит из двух моментов: пункции подключичной вены и введения в полую вену катетера. Пункцию вены можно осуществлять как подключичным, так и надключичным доступом. Целесообразнее использовать правую подключичную вену, поскольку при пункции левой подключичной вены имеется опасность повреждения грудного лимфатического протока, впадающего в венозный угол у места слияния внутренней яремной и левой подключичной вен [Савельев B.C. и др., 1972].
Пункция подключичной вены может быть произведена из разных точек: точка Aubaniac расположена на 1 см ниже ключицы по линии, разделяющей внутреннюю и сред-
нюю треть ключицы; точка Wilson находится на 1 см ниже ключицы по срединно-ключичной линии; точка Giles расположена на 1 см ниже ключицы и на 2 см кнаружи от грудины; точка Yoffa лежит у верхушки ключично-грудино-сосцевидного угла, образуемого верхним краем ключицы и латеральной ножкой грудино-ключично-сосцевидной мышцы (рис. 23.10).
Чаще пунктируют подключичную вену из точки Aubaniac. После анестезии оператор надевает на шприц пункционную иглу и набирает в него раствор новокаина. В месте пункции кожу прокалывают либо скальпелем, либо иглой. Иглу продвигают по направлению вверх и внутрь, причем конец ее должен скользить по задней поверхности ключицы. Продвигая иглу, слегка оттягивают поршень шприца. Появление крови в шприце свидетельствует о том, что игла попала в просвет подключичной вены. Отделяют шприц от иглы и проводят катетеризацию вены по методу Сельдинге-ра. Для этого через просвет иглы в вену вводится проводник. Если он не проходит в вену, то нужно изме-
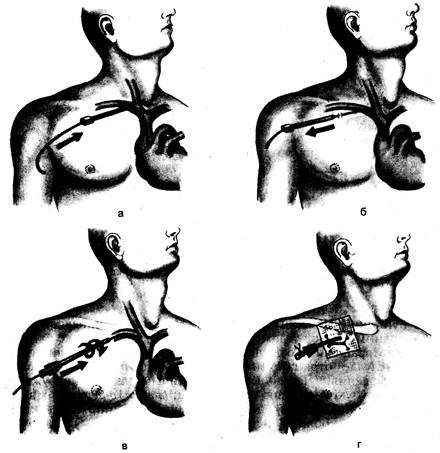
Рис. 23.11.Катетеризация подключичной вены по Селъдингеру.
а — проведение проводника через иглу; б — извлечение иглы; в — проведение катетера по проводнику; г — фиксация катетера.
нить положение иглы, расположить ее параллельно ключице или повернуть вокруг своей оси. Недопустимо насильственное введение проводника. Иглу удаляют, проводник остается в вене. Затем по проводнику мягкими вращательными движениями вводят полиэтиленовый или теф-лоновый катетер на 10-15 см. Проводник извлекают. Проверяют правильность нахождения катетера — подсоединяют к нему шприц и осторожно потягивают поршень. При правильном положении катетера кровь свободно входит в шприц. Катетер заполняют раствором гепари-
на — 1000 ЕД на 5 мл изотонического раствора натрия хлорида. Канюля катетера закрывается заглушкой. Катетер оставляют в вене и фиксируют швом к коже (рис. 23.11).
Неудачи катетеризации верхней полой вены через подключичную вену чаще всего обусловлены нарушением техники процедуры. Для введения катетера следует применять методику Сельдингера, т.е. введение катетера по проводнику. Введение катетера через просвет широкой иглы сопровождается большей травматизацией вены и поэтому нецелесообразно.
Варианты расположения подключичной вены часто встречаются у гиперстеников, у лиц с хорошо развитой мускулатурой и ожирением. Точка Aubaniac у этих больных является наиболее удобной. У детей младшего возраста иглу следует вводить в средней точке линии, условно проведенной между верхушкой подмышечной впадины и верхним краем грудинного конца ключицы по направлению к его задней поверхности.
Пункция и катетеризация внутренней яремной вены.Катетеризация внутренней яремной вены находит все большее распространение. Ее можно применять после неудачной попытки катетеризации подключичной вены. Частота и тяжесть осложнений при этом способе меньше, чем при подключичном доступе.
Внутренняя яремная вена располагается под грудино-ключично-со-сцевидной мышцей и покрыта шейной фасцией. Вену можно пунктировать из трех точек, но наиболее удобен нижний центральный доступ. Больного укладывают в горизонтальное положение, голову поворачивают в противоположную сторону. Определяют треугольник между медиальной (грудинной) и латеральной (ключичной) ножками грудино-ключично-сосцевидной мышцы у места их прикрепления к грудине и ключице. Основанием треугольника служит верхний край ключицы. Терминальная часть внутренней яремной вены лежит позади медиального края латеральной (ключичной) ножки кивательной мышцы. Пункцию производят у места пересечения медиального края латеральной ножки мышцы с верхним краем ключицы под углом 30—45° к коже. Иглу вводят параллельно сагиттальной плоскости на 3—3,5 см, нередко удается ощутить момент прокола вены. По методу Сельдингера катетер проводят на глубину 10—12 см.
Осложнения катетеризации верхней полой в е-н ы: воздушная эмболия, гемоторакс, гидроторакс, пневмоторакс, повреждение грудного лимфатического протока, гематомы вследствие пункции артерий, тромбозы, тромбофлебиты, сепсис. Следует заметить, что частота наиболее грозных осложнений (гемо-, гидро-, пневмоторакс) значительно меньше при катетеризации внутренней яремной вены. Главное преимущество катетеризации внутренней яремной вены по сравнению с катетеризацией подключичной вены — меньший риск пункции плевры.
Пункция и катетеризация бедренной артерии и аорты.Внутриаорталь-ные инфузии после чрескожной катетеризации бедренной артерии показаны в реанимационной ситуации для нагнетания сред, улучшения ре-гионарного кровотока и подведения лекарственных препаратов к органам брюшной полости. Внутриаорталь-ное введение предпочтительно при массивной инфузионной терапии, а в случаях высокого ЦВД и необходимости продолжения инфузионной терапии — при синдроме дыхательных нарушений. Ограничений в применении инфузионных сред нет.
Бедренная артерия пунктируется у пупартовой связки. Для катетеризации используют крупную иглу диаметром 1,2 мм. Для удобства манипуляции иглу с самого начала насаживают на одно- или двуграммовый шприц. Это позволяет избежать излишнего кровоизлияния. Пальцами левой руки (средним и указательным) прощупывается пульсация стенки сосуда. Игла вводится между пальцами, фиксирующими стенку артерии. Срез иглы лучше держать обращенным вниз, чтобы избежать прокола противоположной стенки, а иглу направить под небольшим углом по отношению к коже.
Как только игла проникает в просвет артерии, кровь под сильным давлением поступает в шприц. Пос-
ле этого шприц отсоединяют и проводят катетеризацию артерии или аорты по методу Сельдингера.
Техника пункции артерий. Артериальный путь позволяет получать точную информацию о газовом составе крови и КОС, возможны мониторное наблюдение за АД и определение MOC методом циркулографии.
Для пункции локтевой или лучевой артерии берется тонкая игла. Указательным и средним пальцем левой руки прощупывается пульсация артерии в месте ее проекции на коже. Артерия фиксируется средним и указательным пальцами левой руки, между которыми делается пункция. Появление в игле алой крови с пульсирующим током свидетельствует о наличии иглы в артерии. С целью многократного исследования проб крови, а также для постоянного мониторного наблюдения можно прибегнуть к катетеризации артерии. Из-за опасности тромбоза лучше использовать лучевую артерию: нарушение кровообращения в ней обычно не изменяет кровоснабжения кисти.
За артериальными катетерами требуется тщательный уход: абсолютная стерильность, соблюдение правил асептики. После прекращения инфу-зий катетер должен быть заполнен раствором гепарина. Для этого 5000 ЕД гепарина растворяют в 50 мл изотонического раствора натрия хлорида и 5—10 мл этой смеси заполняют катетер, после чего закрывают катетер резиновой пробкой.
Пункция перикарда (по Ларрею).Показания: травматический ге-моперикард, тампонада сердца, гидроперикард, экссудативный перикардит.
Положение больного — на спине. Под местной анестезией 0,25 % раствором новокаина иглу вкалывают на 1 см ниже и слева от конца мечевидного отростка или в области угла, образованного основанием отростка и хрящом VII ребра. Иглой
прокалывают кожу, подкожную клетчатку и внутренний край левой прямой мышцы живота с ее апоневрозами на глубину до 2 см. Затем павильон иглы приближают к коже, а конец ее проводят кверху и медиально под углом 45° к фронтальной плоскости, параллельно задней поверхности грудины. По ходу иглы вводят новокаин и постоянно потягивают поршень. На глубине 3— 5 см, в зависимости от телосложения больного, конец иглы проникает в полость перикарда, что определяется по исчезновению сопротивления тканей и появлению в шприце крови или жидкости. При излишней глубине введения игле будут передаваться толчки сердца.
Когда пункция через диафрагму невозможна (воронкообразная грудь, вздутие живота, увеличение печени), ее проводят через грудную стенку. Слева прокол делают в чет-вертом-шестом межреберье у края грудины, справа — в четвертом-пятом межреберье. Когда игла достигнет межреберного промежутка, ее павильон максимально отклоняют кнаружи, а конец проводят позади грудины на 1—2 см, чтобы избежать повреждения плевры.
Осложнения: повреждение полостей сердца, коронарных сосудов, плевры и легкого с появлением пневмоторакса, прокол стенки желудка (предварительно следует эвакуировать его содержимое через зонд).
Измерение ЦВДпозволяет оценивать преднагрузку сердца и ОЦК, осуществлять контроль за проводимой инфузионной терапией.
Для измерения ЦВД катетер вводят в верхнюю полую вену (через внутреннюю яремную или подключичную вену) и соединяют его с подключенной для инфузии системой. Ноль шкалы устанавливается на уровне правого предсердия по средней подмышечной линии на пересечении ее с IV ребром, или на 5 см ниже угла, образованного со-
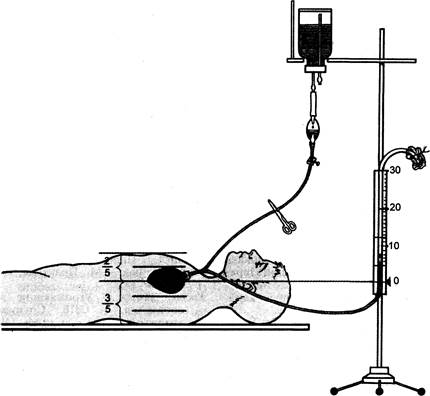
Рис. 23.12.Измерение ЦВД. Пояснение в тексте.
единением между рукояткой и телом грудины (рис. 23.12). После этого система для инфузий, содержащая переливаемую жидкость, отсоединяется от флакона с раствором, снимается зажим и контролируется поступление жидкости в кровеносное русло до тех пор, пока не прекратится дальнейшее ее движение. Величина ЦВД соответствует высоте уровня жидкости в трубке системы над уровнем правого предсердия (средняя подмышечная линия). Нормальная величина ЦВД — 0,58—1,17 кПа (6—12 см вод.ст.).
Слабозаметные колебания ритма дыхания указывают на его нормальное функционирование. Высокий уровень ЦВД с большими размаха-ми колебаний свидетельствует о слишком глубоком введении катетера. Когда катетер достигает полости правого желудочка, его необходимо подтянуть. Низкое ЦВД (0—3 см вод.ст.) свидетельствует о гиповоле-мии. Критической величиной ЦВД является 15—20 мм вод.ст. ЦВД более 1,47 кПа (15 см вод.ст.) расценивается как признак вероятной недостаточности сердца.
Список литературы
Александров В.H., Бобри некая И.Г., Зверев В.В. Значение градиента колло-
идно-осмотического давления в диагностике и лечении отека легких у
больных инфарктом миокарда// Анест. и реаниматол. — 1982. — № 3. - С. 45-49.
Альберт P.К. Отек легких: Пер. с англ.// Неотложные состояния в пульмонологии. — M.: Медицина, 1986. — С. 175-224.
Арабидзе Г.Г., Белоусов Ю.Б., Варакин Ю.Я. и др. Диагностика и лечение артериальной гипертонии/Методические рекомендации.— M., 1997.— С. 44-48.
Арабидзе ГГ., Белоусов Ю.Б., Карпов Ю.А. Артериальная гипертония. — M.: Ремедиум, 1999. - С. 83-90.
Артамошина M.П. Применение опиоид-ных анальгетиков в комплексной терапии болевого синдрома на догос-питальном этапе: дисс. канд. мед. наук. — M, 1997.
Барташевич Б.И. Эпидуральная блокада как компонент интенсивной терапии и анестезии у больных ишеми-ческой болезнью сердца: дисс. канд. мед. наук. — Воронеж, 1998.
Браунвалъд E. и др. Брадиаритмии. Тахи-аритмии. Острый инфаркт миокар-да//Внутренние болезни: Пер. с англ. — Кн. 5. — Болезни сердечнососудистой системы. — M.: Медицина, 1995. - С. 125-181, 286-311.
Бунятян А.А., Шитиков И.И., Флеров E.В. Некоторые аспекты повышения безопасности во время анестезиологического пособия//Клин. вести. — 1996. - № 2. - С. 25-28.
Бунятян А.А., Флеров E.В., Саблин Я. Я. и др. Интраоперационный компьютерный мониторинг в кардиоанесте-зиологии//Материалы III Всероссийского съезда сердечно-сосудистых хирургов. Грудная и сердечнососудистая хирургия. — M., 1996. — С. 193.
Быстрое В. И., Бутров А. В., Бридж P. С., Захарочкина E. P. Современные методы защиты миокарда при остром инфаркте миокарда//Вестн. интенс. тер. - 1995. - № 1. - С. 35-38.
Глезер M.Г., Соболев К.Э. Активная орто-статическая проба в практике врача кардиолога//Матери алы конференции «Клинические и физиологические аспекты ортостатических расстройств». — M., 1999. — С. 2—8.
Городецкий В. В. Инфаркт миокарда. Consilium Medicum. — 2000. — T. 2, № 9. - С. 356-362.
Алперт Дж., Френсис Г. Лечение инфаркта миокарда. — M.: Практика, 1994.-С. 134-136.
Зильбер А.П., Шифман E.M. Терапия при тяжелых формах артериальной ги-пертензии, обусловленных беремен-ностью//Алест. и реаниматол. — 1993. - № 3. - С. 37-40.
Иванов Г.Г., Сыркин А.А., Дворников В.E., Николаев Д.В. Мультичастотный сегментарный биоимпедансный анамнез в оценке изменений обьема водных секторов организма//Рос. журн. анест. и интенс. тер.— 1999.— № 2. - С. 41-47.
Инструментальные методы исследования в кардиологии.//Под ред. проф. Г.И. Сидоренко. — Минск, 1994. — С. 200.
Кардиология в таблицах и схемах: Пер. с англ. Под. ред. M. Фрида и С. Грайнс. — M.: Практика, 1996. — С. 728.
Костюченко А.Л. Угрожающие жизни состояния. — СПб.: Специальная литература, 1999. — С. 144—149.
Куишковский M. С. Гипертоническая болезнь. — M.: Медицина, 1997. — С. 129-138.
Лазебник Л.Б., Верткин А.А., Дроздова С.Л. и др. Антиишемический эффект НАПФ при лечении стенокардии напряжения у больных пожилого и старческого возраста//Тер. арх. — 1996. - № 4, T. 68. - С. 40-42.
Лебединский К.М. Анестезия и системная гемодинамика. — СПб.: Человек, 2000. -С. 199.
Леей Дж.Х. Анафилактические реакции при анестезии и интенсивной терапии: Пер. с англ. — M.: Медицина,
1990. - с. 96-105.
Лоуренс Д.Р., Бенитт Я. Я. Клиническая фармакология. — M.: Медицина,
1991. -T. 2. - С. 382-383.
Люсов B.C. Инфаркт миокарда (вчера, сегодня, завтра)//Рос. кардиол. журн. - 1999. — № ι. — С. 6-15.
Малышев В.Д. Отек легких//Интенсив-ная терапия. Реанимация. Первая помощь. — M.: Медицина, 2000. — С. 114-120.
Марино П. Интенсивная терапия: Пер. с англ. - M.: ГЭОТАР, 1998. -С. 640.
Мархасин B.C., Изаков В.Я., Шумаков В.И. Физиологические основы нарушения сократительной функции миокарда. — СПб., 1994. — С. 243.
Машковский М.Д. Лекарственные средства. В двух томах. — M.: Медицина, 1993.
Международная комиссия по радиологической защите (МКРЗ). Публикация № 23. Медико-биологические данные. — M.: Медицина, 1977.
Международные направления в исследовании артериальной гипертензии. — 1998, №5. -С. 14-15.
Методические рекомендации: оперативная оценка показателей центральной гемодинамики на основе компьютерной реографии//Фролов А.В., Полонецкий А.З., Воробьев А.П. и др. — Минздрав Республики Беларусь. — 1992. — 17с.
Мишунин Ю.В., Касьянов А.А., Назаров Н.А., Решедъко О.А. Об информативности некоторых показателей гемо-динамики//Материалы V Всероссийского съезда анестезиологов-ре-аниматологов. — M., 1996. — T. 1. — С. 21.
Николаев Д.В., Хеймец Г.И., Тарнакин А. Г. ,Аверьянов Д. В. Аппаратное и программное оснащение ортостати-ческих проб//В сб.: Клинические и физиологические аспекты ортоста-тических расстройств. — M.: Главный госпиталь ГУВД, 2000. -С. 123-131.
Ортостатическая гипотензия (этиология, патогенез, клиника, диагностика, лечение)//Методические рекомендации. - M., 2000. - С. 49.
Практическое руководство по анестези-ологии./Под ред. В.В. Лихванце-ва.- M.: МИА, 1998.- С. 128-137.
Привес M.Г., Лысенков И.К., Бушкович В.И. Анатомия человека. — M.: Медицина, 1985.
Пушкарь Ю.Т., Большое В. M., Елизаров H.А. Определение сердечного выброса методом тетраполярной грудной реографии и его методологические возможности//Кардиология. — 1977. - № 7. - С. 85-90.
Реушкин В.H., Реушкина Г.Д., Николаев Д.В., Королев А.В. Методологические основы ортостатической устойчи-БОСТИ//В сб.: Клинические и физиологические аспекты ортостатичес-ких расстройств. — ML: Главный госпиталь ГУВД, 2000. — С. ISO-187.
Руда М.Я., Зыско А.П. Инфаркт миокарда. — Изд. 2-е. — M.: Медицина, 1976. - 200 с.
Рябов Г.А. Гипоксия критических состояний. — M.: Медицина, 1988. — С. 462-463.
Синельников Р.Д. Атлас анатомии человека. В 3 томах. — M.: Медицина, 1996.
Сыркин А.Л. Инфаркт миокарда. — M.: Медицина, 1991. — 301 с.
ТарроуА.Б., Эриксон Д.К. Теоретические и клинические основы анестезиологии: Пер. с англ. — M.: Медицина, 1977. - С. 436.
Тюренков И. H., Тихонов В. П. Средства современной фармакотерапии гипертонической болезни. — M.: Фар-мединфо, 1993. - С. 125-150.
Фильтрационные и комбинированные методы экстракорпоральной деток-сикации при перитоните//Под ред. А.В. Ватазина.— M.: М-Око, 1998.— С. 58-68.
Фомина И, Г. Неотложная терапия в карг диологии. — M.: Медицина, 1997. — 256 с.
Хеймец Г.И. Исследование точности и совершенствование неинвазивных методов контроля сократительной функции сердца и центральной гемодинамики: Автореф. дис. канд. биол. наук. — M.: Институт кардиологии им. А.Л. Мясникова.— 1991.— 24с.
Цимпфер M., Колее H. (Zimpfer M., Kolev N.) Применение вазоактивных и инотропных препаратов для терапии периоперативной сердечной недо-статочности//Актуальные проблемы анестезиологии и реаниматоло-гии.— Архангельск: Тромсе, 1995.— С. 43-44.
Чазов E. И. Очаговые дистрофии и некрозы миокарда (инфаркт миокар-да)//Руководство по кардиологии.— T. 2. — Болезни сердца/Под ред. E. И. Чазова. — M.: Медицина, 1992. - С. 24-74.
Benumof J. L. Anesthesia for thoracic surgery. — W.B. Saimders Co., Phil. — 1987. - 716 p.
Berhard G.R., Brigham K. L. Pulmonary edema pathophysiologic mechanisms and new approaches to therapy// Chest.- 1986.- Vol. 89.- P. 594-600.
Bernstein D.P. A new stroke volume equation for thoracic electrical bioimpe-dance: theory and rationale//Crit. Care Med. - 1986. - Vol. 14. - P. 904-909.
Castor G., Klocke R. K., Stoll M. et aL Simultaneous measurement of cardiac output by thermodilushion thoracic electrical bioimpedans and Doppler ultrasound//B YA. - 1994. - Vol. 72. -P. 133-138.
Hall J., Schmidt G., Wood L. Principles of Critical Care. McGraw Hill, Phil. — 1992. - P. 323-342.
Herling LM. Intravenous nitroglicerin: Clinical pharmacology and therapeutic cj-naiderations//Amer. Heart J. — 1984.— Vol. 108. - P. 141-149.
Hoyt J.W., Tonnesen AS., Alien SJ. Critical Care Practice. — W. B. Saunders Company, Phil. - 1991. - P. 201.
Gottdiener J. Left ventricular mass, diastolic dysfunction, and hypertension//Adv. Int. Med. - 1993. - Vol. 38. -P. 35-56.
Gropper M., Wiener-Kronish J., Hashimoto S. Acute cardiogenic pulmonary ede-ma//Clin. Chest Med. - 1994. -Vol. 15(3). - P. 501-516.
Leier CK, Unverferth D. K Dobutamine// Ann. intern. Med.— 1983.— Vol. 99.— P. 490-496.
Litwin S., Grossman W. Diastolic dysfunction ac a cause of heart failure//J. Amer. Coll Cardiol. — 1993. — Vol. 22(4). - P. 49A-55A.
Kubicek M., Karnegis J., Patterson J. Development and evaluation of impedance cardiac output system//Aerospace Med. J. - 1966. - Vol. 37. -P. 1208-1215.
Marino P. The ICU Book. - The Williams & WilkinsCo., Phil. - 1997.
Marini J.J., Wheeler A. P. Critical Care Medicine. — The Williams & Wilkins Co., Phil. - 1997. - P. 670.
Nyboer J. Electrical impedance Plethys-mography. — Springfield, 1959. — P. 390.
Setaro J., Cabin H. Right ventricular in-farction//Cardiol. Clin. — 1992. — Vol. 10(1). - P. 69-90.
Shoemaker W.C., Wo CC, Bischop M.N. Multisentiv trial of a new thoracic electrical bioimpedance device for cardiac output estimation//Crit. Care Med. — 1994. - Vol. 22. - P. 1907-1912.
Sramek B.B. Thoracic electrical bioimpedance measurement of cardiac out-pat//Crit. Care Med. — 1994. — Vol. 22. -P. 1337-1339.
Thoracic anaesthesia/Ed, by J.A. Kaplan.— Churchill Livingstone. — New York, 1983. - P. 230-246.
West J. B. Respiratory Physiology. The Essentials. 2nd edition. — The Williams SL Wilkins Co., Phil.- 1979.- P. 40-45.
Раздел IV
Шок
Одним из признаков острых нарушений гемодинамики является снижение АД. Это может быть быстро преходящий эпизод, но часто артериальная гипотензия прогрессирует и приводит к другому качественно новому состоянию, резидентному к проводимой терапии, т.е. шоку.
Шок — это остро возникающая несостоятельность кровообращения с критическим расстройством тканевой перфузии, которое ведет к дефициту кислорода в тканях, повреждению клеток и нарушению функции органов.
Мы далеки от мысли считать ги-потензию главным критерием шока (известны варианты шока с высоким АД), однако этот симптом как никакой другой обычно принимается во внимание, а состояние, предшествующее неблагополучному развитию процесса, нередко просматривается и становится очевидным лишь при глубокой гипотензии.
Несмотря на то что пусковые механизмы шока могут быть различными, общим для всех форм шока является критическое снижение перфузии в тканях, приводящее к нарушению функции клеток, а в далеко зашедших случаях — к их гибели. Важнейшее патофизиологическое звено шока — расстройство капиллярного кровообращения, ведущее к тканевой гипоксии, ацидозу и в конечном итоге — к необратимому состоянию.
Следует подчеркнуть, что MOC не может быть показателем перфу-
зии тканей: это подтверждается высокими цифрами CB при септическом шоке. Выраженная вазокон-стрикция, артериовенозное шунтирование могут так распределить минутный кровоток, что большая часть органов и тканей пострадает от дефицита перфузии при относительно нормальной или даже увеличенной работе сердца как насоса. Таким образом, шок может быть с низким или высоким MOC. Последнюю форму шока принято называть гиперкинетической.
Диагностика проводится на основании клинической картины.
Критерии шока: а) симптомы критического нарушения периферического кровообращения (бледные, цианотичные, мраморного вида, холодные, влажные кожные покровы, симптом «бледного пятна» ногтевого ложа); б) симптомы нарушенного центрального кровообращения (малый и частый пульс, иногда брадикардия, снижение систолического АД и уменьшение амплитуды последнего); в) полиорганная недостаточность (нарушения функций легких, ЦНС, олигу-рия).
Важнейшие механизмы развития шока:
• резкое снижение ОЦК;
• уменьшение производительности сердца;
• нарушение сосудистой регуляции.
Каждый из этих механизмов рассматривается в последующих разделах. Указанные причины могут вызвать глубокую артериальную
гипотензию. Следует также указать на возможность сочетания причин, вызывающих шоковое состояние.
Клинические формы:
• гиповолемический шок (возникает в результате абсолютной или относительной гиповолемии);
• кардиогенный шок (снижение сократительной способности миокарда, аритмии, механическая обструкция — тампонада сердца, стенозы клапанов, эмболии);
• септический шок (специфическая реакция на инфекцию);
• анафилактический шок (дисто-ния сосудов в результате воздействия гистамина и других медиаторов).
Установление причины шока очень важно для правильной терапии. В процессе лечения шока возникают постоянные изменения ге-модинамики. Изменения гемодина-мического профиля могут быть диагностированы при мониторинге сердечно-сосудистой системы.
Причины гипотензии:
• уменьшение ОЦК (кровопотеря, потеря плазмы, воды и электролитов) — абсолютная гиповолемия;
• вазодилатационной и перераспределительной — относительная гиповолемия (дистония сосудов любой этиологии, например анафилактический шок; применение средств, воздействующих на сосудистый тонус; недостаточность функции коры надпочечников; сепсис; повреждения ЦНС и спинного мозга);
• снижение нагнетательной функции миокарда (первостепенные причины — инфаркт миокарда, кардиомиопатии, миокардиты и др., второстепенные — тампонада сердца, легочная эмболия, синдром верхней полой вены, воздействие лекарственных агентов, увеличение венозного притока);
• нарушения Ч CC (синусовая бра-дикардия, предсердно-желудоч-ковая блокада, синусовая тахц-кардия, мерцание и фибрилляция предсердий, пароксизмальная су-правентрикулярная тахикардия).
Дата добавления: 2015-03-09; просмотров: 1624;
