Сердечно-сосудистая система.
Сердечно-сосудистая и дыхательная системы тесно взаимосвязаны в обеспечении основной функции — доставки кислорода к тканям. Кровообращение в организме человека представляет собой две функционально разобщенные части: правую, или легочную, и левую, системную. Насосная функция сердца, обеспечивающая адекватную циркуляцию крови, в основном осуществляется левым и правым же-
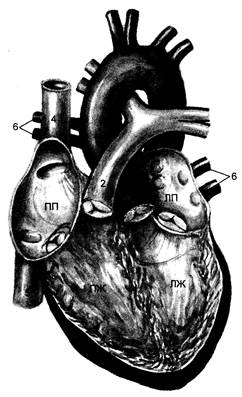
Рис. 2.1.Сердце.
1 — аорта; 2 — легочная артерия; 3 — дуга аорты; 4 — верхняя полая вена; 5 — нижняя полая вена; 6 — легочные вены. Π Π — правое предсердие; ПЖ — правый желудочек; Л Π — левое предсердие; ЛЖ — левый желудочек.
лудочками, которые должны проталкивать одинаковое количество крови, чтобы предупредить застой в артериальной и венозной системах. Предсердия в большей степени (за исключением случаев застойной сердечной недостаточности) играют роль резервуара и в меньшей — осуществляют насосную функцию.
Строение правого и левого желудочков различно (рис. 2.1). Вследствие малого сопротивления легочных сосудов правый желудочек в норме должен нагнетать кровь под давлением, составляющим в среднем Vo-V? давления, создаваемого левыми отделами сердца, для достижения такого же эффекта. Левый желудочек, обладающий мощной мускулатурой, должен создавать более высокое давление для проталкивания крови, преодолевая сопротивление значительно большей сосудистой сети. При достаточной оксигенации он легко приспосабливается к внезапным требованиям увеличения сердечного выброса (CB). Правый желудочек, стенки которого обычно тонкие и чувствительные к предна-грузке, не может адекватно функционировать при внезапном увеличении сопротивления (постнагрузки). У правого и левого желудочков общие межжелудочковая перегородка, циркулярные мышечные волокна и перикардиальное пространство; такая общность морфологического строения играет важную функциональную роль. Взаимозависимость желудочков является главной детерминантой сердечной деятельности при развитии легочной гипертензии. Повышение конечного диастолического объема (КДО) правого желудочка ведет к снижению растяжимости левого желудочка, что влияет на левожелудочковую преднагрузку и УО, усиливает легочную гипертензию и приводит к увеличению постнагрузки правого желудочка. Взаимодействие желудочков проявляется также за счет общего перикардиального пространства: при увеличении объема крови в системе легочного кровотока и в полостях сердца происходит пропотевание жидкости в полость перикарда [Фекс П., 1993; Marini J.J., Wheeler А.Р., 1997].
Коронарный кровоток.Поступление кислорода и питательных веществ в ткани сердца осуществляется по коронарным артериям: системам левой коронарной (огибающая и левая передняя нисходящая артерии) и правой коронарной артерий, отходящих от аорты. Венозная кровь поступает в коронарный синус, который открывается в правое предсердие.
Поступление крови в систему коронарного кровотока зависит от разницы между средним значением АД и давлением в коронарном синусе. Перфузия коронарных артерий заметно различается в каждой фазе сердечного цикла. Разница давлений, возникающая во время диастолы при расслаблении желудочков сердца, обеспечивает наилучшие условия поступления крови в коронарные сосуды. В нормальных условиях коронарный кровоток соответствует метаболическим потребностям миокарда, а при стрессе, гиперметаболизме он возрастает. К сожалению, медиаторы, обеспечивающие эту взаимосвязь, еще мало изучены.
При тахикардии сокращается время диастолической перфузии при одновременном увеличении потребности сердца в кислороде. Подобное сокращение средней величины коронарного кровотока в норме преодолевается за счет вазодилатации. Однако поражение коронарных артерий и внезапно возникающие эпизоды ишемии миокарда препятствуют проявлению этой компенсации. При брадикардии время диастолической перфузии, напротив, увеличивается, а потребность сердца в кислороде снижается. Тем не менее, выраженная брадикардия может привести к снижению, как среднего АД, так и коронарного кровотока.
Деление сосудов по их функциональному значению.Все сосуды организма можно разделить на две большие группы: сосуды сопротивления и емкостные. Первые регулируют общее периферическое сосудистое сопротивление (ОПСС), АД и кровоснабжение отдельных органов и систем организма; вторые вследствие большей емкости участвуют в поддержании венозного возврата к сердцу, а следовательно, и MOC. При этом левые отделы сосудистой системы имеют анатомические и физиологические отличия от правых отделов.
Левые отделы сосудистой системы.Сосуды «компрессионной камеры» — аорта и ее крупные ветви — поддерживают градиент давления за счет растяжимости во время систолы. Это смягчает пульсирующий выброс и обеспечивает более равномерное поступление крови на периферию. В промежутке между сердечными сокращениями адекватный кровоток от сердца к периферическим сосудам происходит за счет эластической тяги последних, претерпевающих растяжение во время систолы. Тогда как аорта представляет собой в основном эластическое образование, стенки периферических артерий содержат гладкие мышечные волокна.
Прекапиллярные сосуды сопротивления — мелкие артерии и артериолы — поддерживают гидростатическое давление в капиллярах и тканевый кровоток.
Артериолы — это элементы, обеспечивающие основное сопротивление. За счет четко отрегулированного калибра эти «крошечные» сосуды способны менять кровоток и под-
держивать АД. Прекапиллярные сфинктеры, регулирующие число функционирующих капилляров, меняют площадь обменной поверхности. В них расположены α-рецепторы, которые под влиянием катехол-аминов вызывают спазм этих сфинктеров, нарушение кровотока и гипоксию клеток. а-адреноблокаторы являются фармакологическими средствами, снижающими раздражение α-рецепторов и снимающими спазм сфинктеров.
Капилляры считаются наиболее важными сосудами обмена. В них осуществляются процессы диффузии и фильтрации — абсорбции. Растворенные вещества проходят через их стенку в обоих направлениях. Капилляры отходят от артериол в большом количестве, и скорость кровотока на этом участке относительно мала. В связи с особенностями строения этих сосудов (они короткие и узкие) в них находится очень незначительная часть общего объема крови (в нормальных условиях только 5—7 %). В то же время емкость капиллярной сети может быть значительно увеличена. При патологических состояниях сеть может вмещать до 90 % крови.
Посткапиллярные сосуды сопротивления — мелкие вены и венулы — регулируют гидростатическое давление в капиллярах, вследствие чего осуществляется транспорт жидкой части крови и межтканевой жидкости. Гуморальный фактор является основным регулятором микроциркуляции. Нейрогенные раздражители также оказывают влияние на пре- и посткапиллярные сфинктеры.
Венозные сосуды не играют значительной роли в создании сопротивления, они выполняют функцию емкости и подвержены симпатическим влияниям. Основными емкостными сосудами являются венулы и небольшие вены. Они вмещают до 85 % объема крови. Общее охлажде-
ние, гиперадреналемия и гипервентиляция приводят к венозному спазму, влияющему на распределение объема крови. За счет изменения емкости венозного русла регулируется венозный возврат к сердцу.
В каждый момент времени бывает задействована лишь малая часть системы кровотока. Точное распределение объема циркулирующей крови (ОЦК) между органами и тканями определяется конкретными метаболическими и функциональными потребностями и достигается за счет артериальной вазоконстрикции.
Шунтовые сосуды — артериовенозные анастомозы во внутренних органах функционируют только в условиях патологии (например, при септическом шоке), а в коже выполняют терморегулирующую функцию.
Правые отделы сосудистой системы.Давление в легочных сосудах очень низкое. Центральные сосуды тоньше, а в стенках артериол содержится очень незначительное количество мышечных волокон. Строение артерий и вен мало различается.
Сопротивление легочных сосудов, будучи очень низким, в нормальных условиях, становится еще ниже при повышении внутрисосудистого давления. В нормальных условиях некоторые легочные капилляры закрыты. При повышении давления по ним возобновляется кровоток, что снижает сопротивление легочных сосудов. Такой механизм называется вовлечением.
Итак, легкие играют роль резервуара крови: легочные сосуды уменьшают свое сопротивление при повышении внутрисосудистого давления за счет механизма вовлечения и расширения сосудов [Уэст Дж., 1988].
Работа капиллярной сети здесь, возможно, даже более интенсивная, чем в большом круге кровооб-
Таблица 2.1. Основные показатели кровообращения и их физиологические колебания
| Обозначения | Характеристика | ·· Физиологические колебания |
| мое | Минутный объем сердца | 5—7 л/мин |
| СИ | Сердечный индекс | 2,3-3,5 л/(мин-м2) |
| УО | Ударный объем | 70—80 мл |
| ВПК | Время полного кругооборота крови | 40-69 с |
| чсс | Частота сердечных сокращений | 60—80 уд/мин |
| РЛЖ | Работа левого желудочка | 6—7 кгм/мин |
| оцк | Объем циркулирующей крови | 65—70 мл/кг |
| ДЗЛА (ДЗЛК) | Давление заклинивания легочной артерии (легочных капилляров) | 5—12 мм рт.ст. |
| САД | Среднее артериальное давление | 90—95 мм рт.ст. |
| цвд | Центральное венозное давление | 6—12 см вод. ст. |
| опсс | Общее периферическое сопротивление сосудов | 1200-2500 дин-с/(см5-м2) |
| слс | Сопротивление легочных сосудов | 100 дин-с/(см5-м2) |
ращения. Распределение потока зависит от силы тяжести, внутриплеврального давления, парциального давления кислорода, рН и других факторов [Marini JJ., Wheeler А.Р., 1997].
Параметры центральной гемодинамики.Основными факторами, характеризующими состояние кровообращения и его эффективность, являются MOC, ОПСС и ОЦК. Эти факторы взаимообусловлены и взаимосвязаны. Измерение только АД и частоты пульса не может дать полного представления о состоянии кровообращения. Определение MOC, ОЦК, ЦВД, ДЗЛА и вычисление некоторых косвенных показателей позволяют получить необходимую информацию (табл. 2.1).
Минутный объем сердца (сердец-ный выброс).MOC определяется объемом крови, которая выбрасывается левым желудочком в 1 мин. CB, определяемый с помощью многих методик, составляет 5—7 л/мин.
В здоровом организме основным регуляторным фактором MOC являются периферические сосуды.
Спазм и расширение артериол определяют динамику артериального кровообращения, регионарного и органного кровоснабжения. Венозный тонус, изменяя емкость венозной системы, обеспечивает возврат крови к сердцу [Гайтон А., 1977].
При заболеваниях сердца или его функциональной перегрузке MOC практически полностью зависит от эффективности работы сердца как насоса, т.е. функциональной способности миокарда.
Способность к увеличению сердечного выброса в ответ на повышение потребности тканей в кровоснабжении называется сердечным резервом. У взрослых здоровых людей он равен 300—400 % и значительно снижается при различных заболеваниях сердца.
В регуляции CB основную роль играют закон Франка—Старлинга и нервно-вегетативная регуляция силы и частоты сердечных сокращений. Указанный закон отражает способность сердца увеличивать силу сокращения при увеличении
наполнения его камер. Согласно этому закону, сердце перекачивает количество крови, равное венозному притоку без значительного изменения ЦВД. В целостном организме нервно-рефлекторные механизмы делают регуляцию кровообращения более тонкой и надежной, непрерывно приспосабливаясь к изменениям внутренней и внешней среды.
Энергия, необходимая для сокращения миокарда, образуется при достаточном поступлении кислорода в клетки. Коронарный кровоток обеспечивает кровоснабжение миокарда в соответствии с потребностями сердечной деятельности. В норме он составляет 5 % CB, в среднем 250— 300 мл/мин. Наполнение коронарных артерий пропорционально среднему давлению в аорте. Коронарный кровоток возрастает при уменьшении насыщения крови кислородом, при увеличении концентрации углекислоты и адреналина в крови. В условиях стресса CB и коронарный кровоток увеличиваются пропорционально. При значительной физической нагрузке CB может достигать 37—40 л/мин, коронарный кровоток — 2 л/мин. При нарушении коронарного кровообращения сердечный резерв значительно снижается.
В критических состояниях возрастающие метаболические потребности покрываются за счет сердечного выброса, нередко поддерживаемого инотропными агентами или при помощи седативных препаратов, анальгетиков и других средств, уменьшающих потребность тканей в кислороде.
Важно помнить, что ближайший послеоперационный период, травма, шок, сепсис сопровождаются, как правило, повышенной потребностью тканей в кислороде, что достигается путем длительной и чрезвычайно интенсивной нагрузки на сердечно-сосудистую систему («гемодинамический марафон»). При этом величина CB может оказаться недостаточной для удовлетворения потребностей тканей в кислороде, что приводит к анаэробному обмену веществ.
Зная основные факторы, определяющие величину MOC, врач отделения интенсивной терапии может активно воздействовать на них, улучшая гемодинамические показатели [Marini JJ., Wheeler A.P., 1997]. К таким факторам относятся:
• состояние венозного возврата и преднагрузки, обеспечивающей необходимую растяжимость сердечной мышцы;
• состояние постнагрузки, т.е. давления, создаваемого миокардом в систолу;
• сократимость миокарда.
Всегда необходимо учитывать общие физиологические условия регуляции MOC, т.е. возбудимость, проводимость и сократимость.
Измерение ДЗЛА позволило сделать огромный шаг вперед в оценке функции сердечно-сосудистой системы. Рассматривая варианты пред-и постнагрузки, нельзя не учитывать величину ДЗЛА, которая в норме составляет 5—12 мм рт.ст. Освоение метода катетеризации (Свана—Ганца) открыло новые возможности гемодинамического мониторинга. Стало возможным определение внутрипредсердного давления, CB, степени насыщения и парциального давления кислорода в смешанной венозной крови.
Несмотря на всю важность измерения ДЗЛА и CB, нельзя считать, что эти показатели являются абсолютными критериями адекватности тканевой перфузии. Однако применение этого метода позволяет реаниматологам контролировать величину преднагрузки и создавать условия для наиболее экономичного режима работы сердца.
Дата добавления: 2015-03-09; просмотров: 1307;
