Влияние на ферменты активаторов и ингибиторов.
Активаторами ферментов являются катионы многих металлов, так, ионы кальция активируют липазу. Некоторые анионы также способны активировать ферменты: ионы хлора активируют a-амилазу слюны.
Активаторами ферментов могут являться различные органические вещества (желчные кислоты пувеличивают активность фермента панкреатической липазы).
Ингибиторы тормозят действие ферментов.
По характеру своего действия ингибиторыподразделяются на обратимыеи необратимые.В основе такого деления лежит прочность связи, образуемой между ингибитором и ферментом.
Обратимые ингибиторы- соединения, которые нековалентновзаимодействуют с ферментом и могут отделяться от фермента.
Обратимое ингибирование может быть конкурентным. Конкурентный ингибитор имеет структуру, похожую на структуру субстрата, но несколько от нее отличающуюся. Он конкурирует с субстратом за связывание в субстратсвязывающем участке активного центра. Конкурентный ингибитор увеличивает Кm.
Пример: фермент сукцинатдегидрогеназа катализирует дегидририрование сукцината; продуктом реакции является фумарат. Малонат,структурно сходный с сукцинатом, связывается в активном центре фермента, но не способен дегидрироваться (рис. 24).
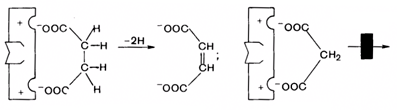
Рис. 24. Схема конкурентного ингибирования
Степень торможения определяется соотношением концентраций малоната и сукцината. При высокой концентрации субстрата последний может полностью вытеснять ингибитор из активного центра, поэтому umax не изменяется.
Метод конкурентного торможения широко применяется в медицинской практике. Парааминобензойная кислота – соединение, участвующее в метаболизме бактерий. Сульфаниламиды – препараты, используемые для лечения инфекционных болезней, – являются ее структурными аналогами. Сульфаниламид вытесняет пара-аминобензойную кислоту из комплекса с ферментом, что приводит к гибели микроорганизмов.
При обратимом неконкурентном ингибировании субстрат и ингибитор связываются с разными центрами. Увеличение концентрации субстрата не препятствует связыванию ингибитора. Неконкурентный ингибитор уменьшает umax, а Кm не меняется.
Известно бесконкурентное ингибирование: ингибитор связывается с ферментом не в каталитическом центре только с ES-комплексом в виде тройного комплекса. Бесконкурентный ингибитор увеличивает Кm и уменьшает umax.
Необратимые ингибиторы- соединения, которые могут специфически связывать функционально важные группы активного центра, образуя ковалентные прочные связис ферментом.
Любые агенты, вызывающие денатурацию белка, приводят к необратимой инактивации фермента, но она не связана с механизмом действия ферментов.
Неконкурентное необратимое ингибирование вызывается солями тяжелых металлов (ртуть, свинец и др.), которые блокируют HS-группы полипептидной цепи, оксидом углерода (II), цианидами и др.
При конкурентном необратимом торможении ингибитор, обладающий структурным сходством с субстратом, соединяется с ферментом, подменяя собой субстрат.
Диизопропилфторфосфат является структурным аналогом нейромедиатора ацетилхолину и способен присоединяться к активному центру фермента ацетилхолинэстеразы, гидролизующего ацетилхолин. Он блокирует активный центр фермента, и в результате утрачивается способность нейронов проводить нервные импульсы.
Дата добавления: 2015-02-10; просмотров: 1930;
