ВЗАИМНОЕ ВЛИЯНИЕ АТОМОВ В МОЛЕКУЛАХ БИООРГАНИЧЕСКИХ СОЕДИЕНИЙ. ЭЛЕКТРОННЫЕ ЭФФЕКТЫ ЗАМЕСТИТЕЛЕЙ. КИСЛОТНЫЕ И ОСНОВНЫЕ СВОЙСТВА БИООРГАНИЧЕСКИХ МОЛЕКУЛ
Содержание лекции.
2.1. Взаимное влияние атомов в молекулах биоорганических соединений
2.1.1. Электронные эффекты заместителей. Индуктивный и мезомерный эффект. Донорные и акцепторные группы-заместители.
2.1.2. Распределение электронной плотности в биоорганических молекулах.
2.2. Кислотно-основные свойства органических соединений.
2.2.1. Теория Бренстеда-Лоури. Определения « кислоты и основания» в соответствии с теорией Бренстеда-Лоури.
2.2.2. Биоорганические соединения- кислоты. Влияние типа кислотного центра и
заместителей кислотные свойства.
2.2.3. Биоорганические соединения- основания. . Влияние типа основного центра и
заместителей основные свойства. свойства
2.3.Медико- биологическое значение изучения темы « Кислотно-основные свойства биоорганических соединений»
Исходный уровень знаний для усвоения темы
Гибридизация орбиталей и пространственная ориентация орбиталей элементов 2 периода., виды химических связей, особенности образования ковалентных σ- и π –связей, полярные и неполярные ковалентные связи, изменение электроотрицательности элементов в периоде и группе, функциональные группы, сопряженные системы, делокализация .
2.1. Взаимное влияние атомов в молекулах биоорганических соединений.
Электронные эффекты заместителей
Ключевые слова к разделу 2.1.
Заместитель донорный, акцепторный, электроотрицательность, распределение электронной плотности в молекуле биоорганического соединения, эффект индуктивный, мезомерный
Смещение электронной плотности в биоорганических соединениях связано с различной электроотрицательностью атомов. Электронная плотность смещается всегда в сторону более электроотрицательного атома.
Ряд электроотрицательности:
F > O > N > C1 > Br > I ~ S > C > H
Функциональные группы, смещающие электронную плотность в свою сторону, являются акцепторами, а группы, «отталкивающие» от себя электронную плотность- донорами.
Для демонстрации этих явлений составляют диаграммы распределения электронной плотности, которые помогают понять направление органической реакции и объяснить , почему они именно так протекают, а не иначе. На основании распределения электронной плотности можно высказать предположение о механизме реакции и строении образующихся веществ.
Смещение электронной плотности вдоль σ –связей носит название индуктивного эффекта Атомы или функциональные группы, «отталкивающие» от себя электронную плотность, проявляют положительный ( +I ) а смещающие в свою сторону – отрицательный (- I ) эффекты.
Индуктивный эффект обозначают стрелкой вдоль связи, которая направлена от атома с частичным положительным зарядом (б + ) в сторону того атома, на котором возникает избыточный отрицательный заряд ( частичный заряд б- )
Индуктивный эффект распространяется на соседние 2-3 атома по отношению к группе, вызывающей этот эффект, и по мере удаления от группы убывает.
Пример:
Распределение электронной плотности в молекуле бутановой кислоты.
б + б + б +
СН3 —> СН2 —> СН2—>СН2 —>СООН
<—————— заряд б + убывает по направлению стрелки
Смещение электронной плотности в системе сопряженных связей носит название мезомерного эффекта ( М-эффект).Мезомерный эффект охватывает всюациклическую сопряженную систему, частичные заряды возникают на крайних атомах в сопряженной системе, а в бензольном кольце – изменение электронной плотности происходит в положениях 2,4,6 ( по отношению к группе, проявляющей эффект).
Атомы галогенов, гидрокси- и аминогруппы содержат неподеленные пары электронов, которые смещаются в сторону π -связи, образуя общую сопряженную систему. Они проявляют +М-эффект. Карбоксильная, карбонильная, нитро-группы обладают –М-эффектом, и они смещают π-электронную плотность в свою сторону.
Примеры: пропеновая (акриловая) кислота
б+ 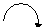
 б-
б-
СН2 == СН— С ==О
\
ОН
Хлорвинил (хлорэтен)
б+ 
 б-
б-
С1 —СН ==СН2
Если в ароматической системе бензола присутствует заместитель – донор, то возникает частичный( избыточный) заряд δ- в положениях 2,4,6 Донорными группами. Проявляющими положительный мезомерный эффект, следует считать гидрокси, амино группы, атомы галогенов фтора и хлора.
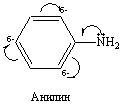
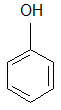
– если заместитель – акцептор, то частичный заряд δ+ в положениях 2,4,6


Акцепторные группы: карбоксильная, альдегидная., нитро, циано.
Донор проявляет положительные + I и + М –эффекты, а акцептор - отрицательные - I и – М –эффекты.
В сопряженной системе главным считается мезомерный М-эффект.
Атом азота в шестичленных ароматических гетероциклических соединениях пиридине и пиримидине имеет отрицательный мезомерный эффект, поэтому снижается общая электронная плотность в ароматической системе( вспомните понятие π-недостаточные циклы) и по отношению к атому азота в положениях 2, 4, 6 цикла возникает недостаток электронной плотности и появляется частичный заряд б + . В никотиновой кислоте введение карбоксильной группы в молекулу пиридина увеличивает недостаток электронной плотности. Атом азота и карбоксильная группа действуют « согласованно» и создают недостаток электронной плотности в одних и тех же положениях 2,4,6 по отношению к ним.
δ+
δ+
δ+ 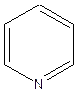 δ+
..
Пиридин
\ δ+
..
Пиридин
\
| δ+ 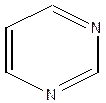 δ+
..
Пиримидин δ+
..
Пиримидин
|
δ +
δ + 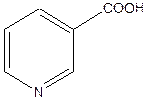
Никотиновая кислота
В таблице представлены значения( направления) эффектов функциональных групп.
Дата добавления: 2015-03-26; просмотров: 2090;
