Поляризация ковалентных связей
Ковалентная полярная связь характеризуется неравномерным распределением электронной плотности. Для обозначения направления смещения электронной плотности используют два условных изображения.
Полярная σ – связь. Смещение электронной плотности обозначают стрелкой вдоль линии связи. Конец стрелки направлен в сторону более электроотрицательного атома. Появление частичных положительных и отрицательных зарядов указывают с помощью буквы « б» « дельта» с нужным знаком заряда.
б + б- б+ б + б- б + б-
СН3 — > О<— Н СН3 — > С1 СН3 — > NН2
метанол хлорметан аминометан ( метиламин)
Полярная π -связь. Смещение электронной плотности обозначают полукруглой ( выгнутой) стрелкой над пи-связью также направленной в сторону более электроотрицательного атома. ( 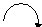 )
)
б +  б- б+
б- б+  б-
б-
Н 2 С = О СН3— С ===О
метаналь |
СН3 пропанон -2
Для проверки усвоения раздела рекомендуем ответить на вопросы:
1.Определите тип гибридизации атомов углерода, кислорода , азота в соединениях А, Б, В . Назовите соединения , используя правила номенклатуры IUPAC .
А. СН3-СН2- СН2-ОН Б. СН2 = СН – СН2- СН=О
В. СН3- N Н– С2 Н5
2. Сделайте обозначения, характеризующие направление поляризации всех указанных связей в соединениях ( А – Г )
А. СН3 – Вr Б. С2 Н5– О- Н В. СН3-NН- С2 Н5
Г. С 2 Н5 – СН= О
Дата добавления: 2015-03-26; просмотров: 1500;
