Развитие сердечной недостаточности
Несмотря на то что клиническая диагностика синдрома сердечной недостаточности, характеризуемого хорошо известными симптомами, не вызывает больших сложностей, тонкие физиологические и биохимические сдвиги, происходящие в этом случае, значительно труднее поддаются изучению. Тем не менее, с клинической точки зрения, сердечную недостаточность можно рассматривать как состояние, при котором нарушенная функция миокарда служит причиной неспособности сердца нагнетать кровь в сосудистое русло в объеме и со скоростью, соизмеримыми с метаболическими потребностями тканей, или же эти потребности обеспечиваются только благодаря патологически высокому давлению наполнения полостей сердца. При сердечной недостаточности страдать может как систола, так и диастола (рис. 181-7). При так называемой систолической, или классической, сердечной недостаточности нарушение сократимости приводит к ослаблению сокращения миокарда в систолу, а следовательно, к снижению ударного объема и расширению полостей сердца. Идиопатическая дилатационная кардиомиопатия является типичным примером систолической сердечной недостаточности. В случае диастолической сердечной недостаточности происходит неполное расслабление желудочков, приводящих к повышению диастолического давления в желудочке при нормальном его объеме. Невозможность полного расслабления может быть функциональной, как, например, при транзиторной ишемии, или вызванной потерей эластичности и утолщением стенок желудочка. Чаще всего диастолическая недостаточность возникает при вторичных рестриктивных кардиомиопатиях, при таких инфильтративных поражениях, как амилоидоз или гемохроматоз (гл. 192). У многих больных с гипертрофией и дилатацией миокарда систолическая и диастолическая формы сердечной недостаточности сосуществуют. В этом случае нарушается как процесс опорожнения, так и процесс наполнения желудочков. Даже при дилатации полостей сердца сдвиг кривой «давление — объем» позволяет достичь повышения диастолического давления в желудочке при любом его объеме.
Характерным признаком систолической сердечной недостаточности служит нарушение сократимости миокарда. Однако этот дефект может быть следствием как первичного поражения сердечной мышцы, например при кардиомиопатии, так и вторичного повреждения ее вследствие длительной чрезмерной нагрузки, например при артериальной гипертензии или клапанном пороке сердца, а также при многих вариантах врожденных заболеваний сердца. При ишемической болезни сердца систолическая сердечная недостаточность представляет собой результат уменьшения количества нормально сокращающихся клеток. Очень важно дифференцировать сердечную недостаточность от циркуляторной недостаточности, при которой функция миокарда страдает вторично, например при тампонаде сердца или геморрагическом шоке; от состояний, характеризующихся застоем кровообращения вследствие патологической задержки солей и жидкости в организме (в подобных случаях серьезных расстройств функции сердца не наблюдают); от состояний, при которых нормально сокращающийся миокард внезапно сталкивается с нагрузкой, превосходящей его возможности, например вследствие обострения артериальной гипертензии или разрыва створки клапана при инфекционном эндокардите.
Собственную сократимость миокарда изучали в эксперименте на изолированном сердце, взятом у здоровых животных, у животных с гипертрофией миокарда и у животных с сердечной недостаточностью. Как при гипертрофии миокарда желудочков, так и при сердечной недостаточности было выявлено снижение максимального изометрического напряжения миокарда и скорости укорочения волокон миокарда до субнормальных значений. Эти изменения были более выражены у животных, страдавших сердечной недостаточностью, чем у животных с изолированной гипертрофией миокарда. Однако гипертрофия миокарда желудочков даже при отсутствии сердечной недостаточности также сопровождалась угнетением сократимости единицы массы миокарда, несмотря на то, что абсолютное увеличение общей мышечной массы обеспечивало поддержание функции сердца в целом. Исследование сосочковых мышц, взятых из левого желудочка больных с сердечной недостаточностью, также продемонстрировало невозможность достижения ими максимального активного напряжения. Электронно-микроскопическое исследование сосочковых мышц кошек, страдавших сердечной недостаточностью, в состоянии, соответствовавшем верхней точке кривой «длина — активное напряжение», показало, что длина саркомера в среднем составляла 2,2 мкм. Таким образом, нарушение сократимости, видимо, не было связано с изменением взаимоотношений филаментов внутри саркомера.
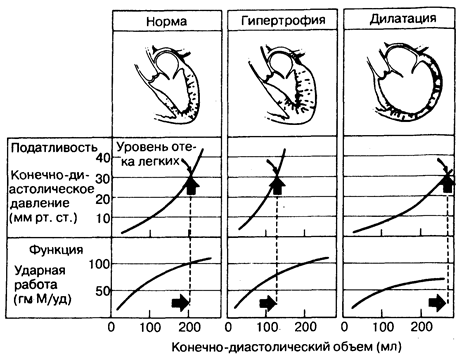
Рис.181-7. Нарушение работы сердца при сердечной недостаточности. Взаимоотношения между конечно-диастолическим объемом левого желудочка и 1) конечно-диастолическим давлением (верхняя часть), что отражает податливость левого желудочка, т. е. его диастолические свойства; 2) ударной работой левого желудочка (нижняя часть), что характеризует кривую систолической функции желудочка. Здоровый левый желудочек (слева) создает конечно-диастолическое давление в 30 мм рт. ст. (уровень, выше которого развивается отек легких), когда его конечно-диастолический объем достигает 200 мл. Систолическая функция левого желудочка при его концентрической гипертрофии (в центре) остается в нормальных пределах, поскольку взаимосвязь конечно-диастолического объема левого желудочка и его ударной работы не меняется. Однако при этом имеет место «диастолическая недостаточность», характеризующаяся тем, что конечно-диастолическое давление, при котором начинается отек легких (30 мм рт. ст.), возникает при меньших значениях конечно-диастолического объема (130 мл). При дилатации желудочка (справа) развивается «систолическая недостаточность», характеризующаяся тем, что максимальная ударная работа и ударный объем понижены при любом значении конечно-диастолического объема. При этом у левого желудочка повышается диастолическая податливость, т. е. растяжимость, при значительно более высоких, чем требуется для развития отека легких, величинах конечно-диастолического объема (280 мл). (С разрешения из: R. Gorlin—Prim. Cardiol., 1984, 6, 84.)
При нарушении сократимости миокарда желудочек может продолжать выбрасывать в сосудистое русло нормальное или почти нормальное количество крови, несмотря на существенное угнетение его функции, за счет увеличения конечно-диастолического объема, т. е. благодаря действию механизма Франка — Стерлинга. Как отмечалось выше, увеличение исходного объема желудочка сопровождается растяжением саркомера. В результате этого увеличивается количество точек взаимодействия нитей актина и миозина и/или повышается их чувствительность к ионам кальция. Более того, гипертрофию желудочков можно рассматривать как процесс формирования дополнительных контрактильных единиц, что представляет собой важный механизм компенсации в условиях угнетения собственной сократимости миокарда.
Оценка сердечной деятельности. Для оценки степени нарушения функции сердца у человека существует несколько методов. Даже в состоянии покоя сердечный выброс и ударный объем могут быть снижены, но нередко эти показатели остаются в пределах нормы. Более чувствительным показателем является фракция выброса, т. е. отношение ударного объема к конечно-диастолическому объему, определяемое в процессе стандартной рентгенологической или радиоизотопной ангиографии (гл. 179 и 180). При сердечной недостаточности величина фракции выброса, как правило, снижается, даже если ударный объем остается в пределах нормы. Недостатком показателей фракции выброса и сердечного выброса при оценке функции сердца можно рассматривать тот факт, что они существенно зависят от величин желудочковой пред- и постнагрузки. Таким образом, угнетение фракции выброса и снижение сердечного выброса можно наблюдать у больных с сохраненной функцией желудочков, но при сниженной преднагрузке, как, например, в случае гиперволемии, или при резком повышении артериального давления. Регистрация циркуляторных изменений во время стрессовых ситуаций, например физической нагрузке или увеличении постнагрузки, представляет собой еще более чувствительный метод выявления нарушенной функции желудочков. Для этого функцию левого желудочка оценивают по величинам конечно-диастолического давления в левом желудочке, сердечного выброса и общего потребления кислорода организмом в покое и при нагрузке. У здорового человека сердечный выброс увеличивается не менее чем на 500 мл/мин при возрастании потребления кислорода на 100 мл/мин. В покое конечно-диастолическое давление в левом желудочке не превышает 12 мм рт. ст. При физической нагрузке оно может остаться на прежнем уровне, немного повыситься или снизиться; ударный объем обычно повышается. С другой стороны, нарушение функции левого желудочка характеризуется возрастанием конечно-диастолического давления при физической нагрузке более 12 мм рт. ст., что сопровождается отсутствием увеличения или даже снижением ударного объема и субнормальным повышением сердечного выброса в ответ на усиление минутного потребления кислорода тканями. Было установлено, что между нормальным ответом на физическую нагрузку и реакцией на нее больного с левожелудочковой недостаточностью имеется целый ряд промежуточных ступеней.
Ценность изучения функции левого желудочка в условиях стресса подтверждается тем фактом, что величины конечно-диастолического давления в левом желудочке, сердечного индекса и ударной работы желудочков в покое могут не различаться у больных с угнетением желудочковой функции и у здоровых лиц. Исследование реакции на физическую нагрузку позволяет не только выявить нарушение функции миокарда, но и количественно оценить ее выраженность.
Функциональная активность левого желудочка у человека может быть охарактеризована также с помощью данных о мгновенных взаимоотношениях силы и скорости сокращения миокарда и о степени укорочения его волокон во время каждого отдельного сердечного цикла. Ангиокардиографические и эхокардиографические исследования (гл. 179) и анализ скорости изменения внутрижелудочкового давления (dp/dt) при одновременной регистрации давления во время изоволюметрического сокращения показали, что у больных с сердечной недостаточностью наблюдается угнетение процессов укорочения и напряжения мышечных волокон. У лиц с ишемической болезнью сердца эти нарушения чаще имеют определенную локализацию и реже бывают диффузными. Так, они нередко проявляются регионарными нарушениями движения стенки желудочка при нормальной общей функции левого желудочка. Соотношение конечно-систолических значений давления и объема является чрезвычайно ценным показателем, отражающим состояние желудочковой функции, поскольку он учитывает как пред-, так и постнагрузку. Большую помощь при клинической оценке функции миокарда оказывают неинвазивные методы получения изображения, в частности эхокардиография и радиоизотопная ангиография (гл. 179).
Метаболизм миокарда при сердечной недостаточности. Наиболее часто встречающиеся формы сердечной недостаточности с низким сердечным выбросом, вызванные атеросклерозом, артериальной гипертензией, поражением клапанов и врожденными заболеваниями, характеризуются абсолютным или относительным уменьшением полезной внешней работы сердца. Механизмы, лежащие в основе этого уменьшения, в настоящее время активно изучаются.
Были получены объективные доказательства того, что при сердечной недостаточности нарушается сопряжение процессов возбуждения и сокращения, в результате чего снижается доставка ионов кальция к контрактильным элементам, что и обусловливает ухудшение сердечной деятельности. Молекулярные изменения, лежащие в основе этих дефектов, а также их локализация в клетке (сарколемма, Т-канальцы и/или саркоплазматическая сеть) требуют уточнения.
Большое внимание также было уделено вопросу о том, является ли сердечная недостаточность следствием нарушения продукции, консервации или утилизации энергии. Однако лишь в отдельных случаях, как, например, при бери-бери, сердечная недостаточность сопровождается отчетливыми расстройствами продукции энергии в миокарде. Основные пути, по которым пируват входит в цикл лимонной кислоты, и некоторые реакции внутри самого цикла зависят от наличия адекватного количества тиамина (гл. 76). Недостаток тиамина приводит к снижению утилизации пировиноградной кислоты тканями сердца и к патологическому снижению коэффициента экстракции пирувата у исходно здоровых собак и людей.
На втором этапе миокардиального метаболизма, этапе консервации энергии, энергия окисления субстрата трансформируется в энергию концевых связей креатинфосфата (КФ) и АТФ, непосредственных источников химической энергии, потребляемой сердечной мышцей. Этот процесс, известный как окислительное фосфорилирование, происходит в митохондриях. Эффективность механизма сопряжения продукции и консервации энергии можно исследовать, измеряя запасы АТФ и КФ в миокарде. При этом консервацию энергии можно оценивать по величине отношения Ф/К, т. е. отношения количества продуцируемого высокоэнергетического фосфата к количеству потребляемого митохондриями кислорода, а также по степени сопряжения транспорта электронов и образования высокоэнергетических фосфатов. Существует много противоречивых сведений о значении этой фазы метаболизма при сердечной недостаточности. В настоящее время есть данные о том, что тяжелое нарушение сердечной деятельности может иметь место и без повреждения функции митохондрий или сокращения запасов высокоэнергетических фосфатов. Тем не менее при некоторых формах экспериментальной сердечной недостаточности поломка этих процессов действительно присутствует.
Отсутствие убедительных доказательств расстройства образования или консервации энергии в пораженном миокарде, естественно, заставило обратить внимание на возможность нарушения утилизации энергии при развитии сердечной недостаточности. Патологическое высвобождение энергии могло бы иметь место, если бы контрактильные протеины были повреждены. При некоторых формах экспериментальной сердечной недостаточности, в частности вызванной механической перегрузкой, действительно был выделен изоэнзим миокарда, характеризующийся иммунологическими и электрофоретическими свойствами и низкой кальцийзависимой АТФазной активностью. Возможно, что эта низкая активность и лежит в основе патологического распада АТФ, процесса, ведущего к сокращению сердечной мышцы.
Адренергическая нервная система и сердечная недостаточность. Ввиду чрезвычайной важности адренергической нервной системы для стимуляции сократимости здорового миокарда ее активность изучали у больных с застойной сердечной недостаточностью. Активность этой системы в покое и при физической нагрузке оценивали по концентрации норадреналина в артериальной крови. У здоровых лиц при физической нагрузке происходит относительно небольшое повышение уровней норадреналина. У больных же с сердечной недостаточностью уровни циркулирующего норадреналина даже в покое могут быть заметно повышены. Причем прогноз заболевания тем хуже, чем выше концентрации нейротрансмиттера. Кроме того, у больных с застойной сердечной недостаточностью при физической нагрузке содержание норадреналина в крови повышается в значительно большей степени, чем у здоровых людей. Это также объясняют существенно более высокой активностью адренергической нервной системы v данной группы больных, которая сохраняется и во время физической нагрузки.
Важность повышения активности адренергической нервной системы для поддержания сократимости желудочков в условиях угнетения функции миокарда при застойной сердечной недостаточности подтверждается данными о том, что блокада адренорецепторов может усугубить нарушение насосной функции. Таким образом, адренергическая нервная система играет важную модулирующую роль в поддержании кровообращения у больных с застойной сердечной недостаточностью. В связи с этим следует с большой осторожностью использовать антиадренергические препараты, в частности адреноблокаторы, при лечении больных с ограниченным резервом миокарда (гл. 182).
В то же. время концентрация и содержание норадреналина в тканях сердца у больных с сердечной недостаточностью понижены, составляя в ряде случаев лишь 10 % от нормальных значений. Механизм, лежащий в основе этого явления, полностью неизвестен. Однако считают, что длительное сохранение высокого тонуса симпатических нервов сердца играет решающую роль, вмешиваясь определенным образом в биосинтез норадреналина. Кроме того, имеются доказательства, что при хронической тяжелой сердечной недостаточности плотность адренорецепторов в сердце и концентрация циклической АМФ в миокарде существенно понижены.
Учитывая мощный положительный инотропный эффект норадреналина, выделяемого этими нервами, адренергическую нервную систему можно рассматривать в качестве важного потенциального источника поддержания функции страдающего миокарда. Однако увеличение частоты и силы сердечных сокращений у животных с экспериментальной сердечной недостаточностью и истощением запасов норадреналина в сердце практически отсутствует или выражено минимально при стимуляции симпатических нервов сердца. Таким образом, складывается впечатление, что в тех случаях, когда застойная сердечная недостаточность сопровождается истощением запасов норадреналина в сердце, количество его, выделяемое симпатическими нервными окончаниями в сердце, мало по отношению к той импульсации, которая передается по этим нервам. Более того, даже выделившийся норадреналин не может оказать на миокард должного воздействия вследствие угнетения эффективного адренергического механизма миокарда.
В то же время наличие запасов норадреналина в миокарде не является обязательным условием поддержания его сократимости. Однако, поскольку уменьшение запасов норадреналина в миокарде при сердечной недостаточности сочетается со снижением выброса этого нейротрансмиттера, можно предположить, что указанное истощение последнего лежит в основе утраты такой необходимой адренергической поддержки нарушенной функции миокарда. На более поздних стадиях сердечной недостаточности, когда уровни циркулирующих катехоламинов повышены, а содержание норадреналина в миокарде понижено, миокард становится во многом зависимым от более генерализованной адренергической стимуляции, исходящей из внекардиальных источников, главным образом из мозгового вещества надпочечников. Данный факт объясняет ухудшение деятельности сердца, возникающее у больных с сердечной недостаточностью, получающих адреноблокаторы. Это генерализованная адренергическая стимуляция, являющаяся результатом циркуляции большого количества катехоламинов в крови, может, однако, оказывать и неблагоприятные побочные эффекты, связанные с повышением сосудистого сопротивления, а следовательно, и постнагрузки, которая значительно превышает оптимальные значения.
Заключая анализ механизмов сердечной недостаточности, следует отметить, что основные нарушения кроются в угнетении взаимоотношений силы и скорости сердечных сокращений и сдвиге кривой «длина — активное напряжение сердечных волокон». Это отражает уменьшение сократимости миокарда (см. рис. 181-6, кривые 1, 3). Во многих случаях сердечный выброс и внешняя работа желудочков у этих больных в покое сохраняются в пределах нормы, что, однако, обеспечивается только лишь за счет увеличения конечно-диастолической длины мышечных волокон и повышения конечно-диастолического объема желудочка, т. е. за счет механизма Франка — Старлинга (см. рис. 181-6, точки А—Г). Повышение преднагрузки левого желудочка сопровождается аналогичными изменениями давления в легочных капиллярах, вызывая одышку у больных с сердечной нeдостаточностью. Сократительная способность миокарда вследствие повышенной симпатической активности при физической нагрузке у больных с тяжелой сердечной недостаточностью не возрастает или возрастает в незначительной степени, что обусловлено истощением запасов норадреналина в миокарде (см. рис. 181-6, кривые 3 и 3'). Механизмы, поддерживающие наполнение желудочков кровью во время физической нагрузки у здоровых лиц, приводят к дальнейшему ухудшению функции миокарда при его недостаточности, в результате уплощается кривая «длина — активное напряжение волокон». И несмотря на то, что левый желудочек после их включения может несколько улучшить свою деятельность, этот эффект достигается исключительно благодаря чрезмерному повышению конечно-диастолического объема и давления левого желудочка, а следовательно, и давления в легочных капиллярах. Последний фактор ведет к усилению одышки, которая в свою очередь играет важную роль в ограничении интенсивности выполняемой пациентом физической нагрузки. Левожелудочковая недостаточность становится необратимой, когда кривая «длина — активное напряжение мышечных волокон» угнетается настолько, что сердечная деятельность не способна удовлетворить метаболические потребности периферических тканей в покое (см. рис. 181-6, кривая 4), и/или конечно-диастолическое давление в левом желудочке и давление в легочных капиллярах повышается в такой степени, что приводит к развитию отека легких (см. рис. 181-6, точка Д).
Дата добавления: 2015-03-17; просмотров: 671;
